 |
Главная |
Кислорода по методу Винклера
|
из
5.00
|
Метод определения кислорода по методу Винклера основан на способности гидроксида марганца (II) окисляться в щелочной среде до гидроксида марганца (IV), количественно связывая при этом кислород. В кислой среде гидроксид марганца (IV) вновь переходит в двухвалентное состояние, окисляя при этом эквивалентное связанному кислороду количество йода, выделяющегося из щелочного раствора йодида калия. Полученный йод титруется тиосульфатом натрия. Предел обнаружения растворенного кислорода составляет 0,05 мг/л.
Цель работы – определить растворенный в воде кислород по методу Винклера.
Оборудование и реактивы:
– склянки с притертой пробкой вместимостью 100-200 мл;
– колбы конические плоскодонные вместимостью 500 мл;
– раствор МnСl2;
– щелочной раствор йодида калия;
– тиосульфат натрия, 0,01н раствор NaS2O3;
– крахмал, 0,5%-ный раствор;
– серная кислота (1:4).
Ход работы
1. В склянку (под водой!) 200 – 300 мл с притертой пробкой вводится 1 мл раствора МnСl2и 1 мл щелочного раствора KI.
2. Склянка закрывается пробкой, содержимое перемешивается. После появления осадка вводится 3 мл серной кислоты (1:4).
3. Содержимое перемешивается до полного растворения осадка, после чего переливается в коническую колбу вместимостью 500 мл и титруется 0,01 н раствором тиосульфата натрия (крахмал вводится в конце титрования).
4. Содержание кислорода в мг/л, растворенного в воде, рассчитывается по формуле:
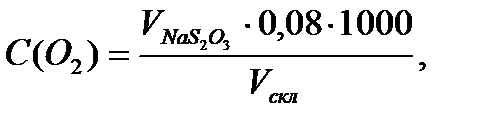
| (3.4) |
где V 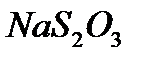 – объем раствора тиосульфата, израсходованный на титрование пробы;
– объем раствора тиосульфата, израсходованный на титрование пробы;
0,08 – количество кислорода, соответствующее 1 мл 0,01н раствора тиосульфата натрия, мг;
Vскл. – объем пробы, мл.
Таблица 5.3. Форма записи результатов анализарастворенного
в воде кислорода
| Проба | Место отбора | V NaS2O3, мл | Vскл, мл | С (О2), мг/л |
| Среднее |
5. Сделать выводы и предложить проект улучшения качества воды.
МИНЕРАЛЬНЫЙ СОСТАВ ВОДЫ
Лабораторная работа № 6.1
Определение сульфат-ионов тубидиметрическим методом
Сульфаты – распространенные компоненты природных вод. Их присутствие в воде обусловлено растворением некоторых минералов – природных сульфатов (гипс), а также переносом с дождями содержащихся в воздухе сульфатов.
Наличие сульфатов в промышленных сточных водах обычно обусловлено технологическими процессами, протекающими с использованием серной кислоты (производство минеральных удобрений и др. химических веществ). Сульфаты в питьевой воде не оказывают токсического воздействия на человека, однако ухудшают вкус воды: ощущение вкуса сульфатов возникает при их концентрации 250–400 мг/л. Сульфаты могут вызывать отложение осадков в трубопроводах при смешении двух вод с разным минеральным составом, например сульфатных и кальциевых (в осадок выпадает СаSO4).
Метод определения сульфатов основан на осаждении сульфат-ионов в кислой среде хлоридом бария в виде сульфата бария.
Оборудование и реактивы:
пробирки колориметрические;
соляная кислота (1:5);
хлорид бария, 5%-ный раствор.
Ход работы
1. В пробирку наливают 10 мл исследуемой воды.
2. Добавляют 0,5 мл соляной кислоты.
3. Затем приливают 2 мл 5%-ного раствора хлорида бария и перемешивают.
Приближенное значение содержания сульфатов определяется визуально по характеру выпадающего осадка (табл. 6.1), затем заполняется таблица итоговых результатов (табл. 6.2).
Таблица 6.1. Определение сульфатов
| Характер осадка | Концентрация сульфатов, мг/л |
| Отсутствие мути | |
| Слабая муть, появляющаяся через несколько минут | 5-10 |
| Слабая муть, появляющаяся сразу после добавления хлорида бария | 10-100 |
| Сильная муть, быстро оседающая |
Таблица 6.2. Форма записи результатов анализа
| Проба | Место отбора | Характер осадка | Концентрация сульфатов, мг/л |
| Среднее |
4. Сделать выводы и предложить проект улучшения качества воды.
Лабораторная работа № 6.2
|
из
5.00
|
Обсуждение в статье: Кислорода по методу Винклера |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

