 |
Главная |
С сульфосалициловой кислотой
|
из
5.00
|
Железо (III) образует с сульфосалициловой кислотой в зависимости от кислотности раствора ряд окрашенных комплексов. В практике молекулярного абсорбционного анализа применяют лишь комплексы, образующиеся в кислой и щелочной среде. При рН 1,8 – 2,5 образуется красно-фиолетовый катионный комплекс (I), имеющий полосу поглощения lмакс = 510 нм и eмакс = 1,8×103.
В щелочных средах (9 < pH <11,5) образуется комплекс желтого цвета с полосой поглощения lмакс = 416 нм и eмакс = 5,8×103.
Моносульфосалицилатный комплекс (I) используют для определения Fe(III) в присутствии Fe(II), Mg, Mn, Cu, Al, редкоземельных элементов. Определению мешают F- - ионы. В щелочной среде вследствие легкой окисляемости Fe(II) в Fe(III) с помощью сульфосалициловой кислоты можно определить суммарное железо в растворе. При этом F- - ионы не мешают определению.
Оборудование и реагенты:
- Fe2(SO4)3 × 9H2O, чда;
- сульфосалициловая кислота, 10% раствор;
- серная кислота, 1 М раствор;
- мерная колба вместимостью 50 см3 – 1 шт.;
- мерная колба вместимостью 100 см3 – 6 шт.;
- градуированная пипетка вместимостью 5 см3 – 1 шт.;
- медицинский шприц на 2 см3 – 1 шт.;
- мерная пробирка или цилиндр объемом 10 (15) см3 – 1 шт.;
- фотоэлектроколориметр «Эксперт 003»;
- кюветы с l = 1 см – 2 шт.;
- весы лабораторные аналитические 2 кл. точности;
- набор разновесов
Построение градуировочного графика
1. Навеску Fe2(SO4)3 × 9H2O массой 0,16 – 0,17 г, взвешенную с точностью до четвертого знака после запятой, количественно переносят в мерную колбу вместимостью 50 см3. В мерной колбе вместимостью 100 см3 готовят 10%-ный раствор сульфосалициловой кислоты.
2. В пять мерных колб вместимостью 100 см3 вводят 1, 2, 3, 4, 5 см3 стандартного раствора Fe(III), добавляют 2 см3 серной кислоты, 10 см3 сульфосалициловой кислоты и объем доводят до метки дистиллированной водой.
3. Растворы фотометрируют относительно воды в кюветах
l = 1 см при l = 510 нм, полученные данные заносят в таблицу 6.5:
Таблица 6.5. Форма записи результатов определения
оптической плотности градуировочных растворов
| Объем стандартного раствора, см3 | Оптическая плотность | Концентрация рабочего раствора, мг/ см3 |
4. Строят градуировочный график. При этом по оси абсцисс откладывают содержание Fe(III) в мг, а по оси ординат – оптическую плотность полученных растворов.
5. Определение содержания Fe(III) в природной или сточной воде. Цилиндром отмеряют 100 см3 природной или сточной воды, помещают в колбу вместимостью 200 см3 , добавляют 10 см3 сульфосалициловой кислоты и доводят до метки дистиллированной водой.
Полученный раствор фотометрируют относительно воды в тех же условиях, что и при построении градуировочного графика.
По градуировочному графику находят содержание Fe(III) в анализируемом растворе.
Содержание Fe(III) в выданном (контрольном) растворе находят по формуле:
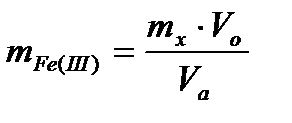 , где
, где
 - масса Fe(III) в контрольном растворе;
- масса Fe(III) в контрольном растворе;
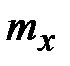 - масса Fe(III), найденная по графику;
- масса Fe(III), найденная по графику;
 - объем раствора неизвестной концентрации, л
- объем раствора неизвестной концентрации, л
 - объем аликвоты контрольного раствора, л.
- объем аликвоты контрольного раствора, л.
|
из
5.00
|
Обсуждение в статье: С сульфосалициловой кислотой |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

