 |
Главная |
Величина адсорбции растворенного вещества тем больше, чем больше разность полярностей между адсорбентом и растворителем.
|
из
5.00
|
В случае ионной адсорбции один из ионов часто адсорбируется избирательно. Правила избирательной адсорбции были сформулированы Песковым и Фаянсом:
На поверхности твердого адсорбента преимущественно адсорбируются ионы, имеющие с этим адсорбентом общую атомную группировку.
Если поверхность адсорбента имеет заряд, то, преимущественно, будут адсорбироваться ионы с ионы с противоположным зарядом, а также ионы, образующие с поверхностью нерастворимые соединения.
11. Взаимодействие между частицами адсорбата и адсорбента может иметь различный характер, в зависимости от этого различают несколько видов адсорбции.
Физическаяадсорбция обусловлена силами Ван-дер-Ваальса, возникающими между частицами адсорбата и адсорбента. Она обратима и уменьшается с ростом температуры.
Химическая адсорбция (хемосорбция) обусловлена химическими силами. Она необратима и увеличивается с ростом температуры (например, адсорбция кислорода на поверхности металла)
Адсорбция происходит на поверхности раздела газ/твердое тело, раствор/твердое тело, газ/жидкость, жидкость/жидкость.
Причиной адсорбции являются неспецифические (то есть не зависящие от природы вещества) Ван-дер-Ваальсовы силы. Адсорбция, осложнённая химическим взаимодействием между адсорбентом и адсорбатом, является особым случаем. Явления такого рода называют хемосорбцией и химической адсорбцией. «Обычную» адсорбцию в случае, когда требуется подчеркнуть природу сил взаимодействия, называют физической адсорбцией.
Физическая адсорбция является обратимым процессом, условие равновесия определяется равными скоростями адсорбции молекул адсорбтива P на вакантных местах поверхности адсорбента S* и десорбции — освобождения адсорбата из связанного состояния S − P:
 ;
; 
12. уравнение изотермы адсорбции Ленгмюра: 
 , где Г - величина адсорбции газа, Г∞ - максимально возможное количество адсорбированного вещества при образовании мономолекулярного слоя адсорбата, т. е. предельная адсорбция, в - константа адсорбционного равновесия, Р - равновесное давление газа.
, где Г - величина адсорбции газа, Г∞ - максимально возможное количество адсорбированного вещества при образовании мономолекулярного слоя адсорбата, т. е. предельная адсорбция, в - константа адсорбционного равновесия, Р - равновесное давление газа.
Наряду с изотермами адсорбции для количественного описания закономерностей адсорбции применяются изобары и изостеры адсорбции.
Изобара адсорбции – зависимость количества адсорбированного вещества (или степени заполнения поверхности) от температуры при постоянном давлении адсорбата в газовой фазе.
Изостера адсорбции – зависимость равновесного давления адсорбата от температуры для определенного количества адсорбированного газа.
Изостеры адсорбции используются для определения теплоты адсорбции графическим методом. Для этого строят несколько изотерм для разных температур, а затем находят значения соответствующих давлений адсорбата при постоянной величине адсорбции. После этого строят зависимость lnP от 1/Т при постоянной степени заполнения поверхности. Тангенс угла наклона прямой равен –Qадс/R.
13.способность к электрофорезу-явление перемещения ДФ относительно наподвижной ДС под действием внешнего эл.поля. причина эк-реза-наличие двойного эл.слоя на поверхности частиц ДФ.Адсорбция лежит в основе клинического анализа крови на СОЭ.Так, принфекционных заболеваниях в крови происходит обменная адсорбция: вместо ионов электролитов поверхность эритроцитов занимают молекулы белков. При этом заряд эритроцитов понижается и они быстрее объединяются и оседают. Адсорбционная терапия применяется для удаления токсинов и вредных веществ из пищеварительного тракта. Такие адсорбенты, как гидроксид алюминия, оксид магния, фосфат алюминия, входят в состав препаратов альмагель, фосфалюгель. Активированный уголь давно применяется как адсорбент газов (при метеоризме), токсинов (при пищевых токсикоинфекциях), алкалоидов и тяжелых металлов (при травлениях).Хорошей адсорбирующей способностью обладает клетчатка. Содержание клетчатки у больных сахарным диабетом должно быть не меньше 25 г/1000 ккал: клетчатка замедляет всасывание сахаров, компенсируя повышение концентрации глюкозы в плазме после приема пищи.На основе оксида кремния создан препарат полисорб – неселективный полифункциональный энтеросорбент. Его применяют для выведения из организма патогенных бактерий и их токсинов, пищевых аллергенов, солей тяжелых металлов, радионуклидов, этанола, а также ядов различного происхождения.
14.Хроматография – метод разделения веществ при прохождении раствора или газа через колонку с адсорбентом. длинные тонкие капилляры с пористыми стенками или заполняют более широкие трубки зернами пористого адсорбента. Это приводит к возникновению большой поверхности раздела фаз, следовательно, при медленном прохождении газа осуществляются многократно повторяющиеся процессы адсорбции. Это позволяет получить разные времена выходов компонентов.Такой вид хроматографии называют газоадсорбционной хроматографией.Если же крупные поры адсорбента заполнить неподвижной жидкостью, то вместо различий в адсорбируемости можно использовать различия в растворимости отдельных компонентов газовой смеси – газожидкостная хроматография. Хроматографическое разделение смесей веществ может осуществляться разными способами:1 способ:в колонку с адсорбентом вводят газовую смесь с постоянной концентрацией компонентов. У выхода из колонки появляются наименее адсорбирующийся или наименее растворимый компонент, затем смесь этого компонента с несколько более легко адсорбирующимся компонентом, затем смесь двух компонентов с еще более легко адсорбирующимся и т.д. вплоть до исходной газовой смеси. Такой анализ называют фронтальным. Недостатком его является то, что в чистом виде можно получить только первый компонент.2 способ: через колонку с адсорбентом пропускают непрерывный поток практически неадсорбирующегося газа (газ-носитель), в который у входа в колонку вносят небольшую порцию анализируемой смеси. В этом случае у выхода из колонки в токе газа-носителя сначала появляется наименее адсорбирующийся компонент газовой смеси, затем газ-носитель, затем смесь первого компонента с более легко адсорбирующимся газом, затем газ-носитель и т.д. Таким образом, зоны выхода компонентов на хроматограмме оказываются разделенными газом-носителем. Такой анализ называется проявительнойхроматографией.
15.Комплексное соединение — вещество, в состав которого входят комплексные частицы. В молекуле любого КС один из ионов (обычно катион) занимает центральное место и называется комплексообразователем или центральным ионом.Вокруг него координировано некоторое число противоположно заряженных ионов или электронейтральных молекул – лигандовили аддендов. Лиганды образуют внутреннюю координационную сферу соединения.Ионы, находящиеся на более далеком расстоянии от центрального иона, составляют внешнюю координационную сферу. Число лигандов, окружающих центральный ион, - координационное число.Во внутренней сфере ионы связаны неионогенно,а во внешней - ионогенно.пр.K2[PtCl6] Внутренняя сфера..Комплексообразователь ион Pt+4..Лиганды ионы Cl-..Внешняя сфера..ион К+
Лиганды, занимающие во внутренней координационной сфере 1 место, - монодентатные.Лиганды, занимающие во внутренней координационной сфере 2 и более мест, - би- и полидентатные.номенклатура1.Число лигандов (ди- (бис-), три- (трис-), тетра- (тетраксис-) и т.п.)
2. Названия лигандов (для анионов добавляется гласная -о- , исключения – меркапто-, тио-; для нейтральных лигандов названия не модифицируются, исключения вода - аква-, аммиак - аммин-, СО – карбонил-, NO – нитрозил)
3. Центральный атом (в анионных КС - лат. корень + -ат, в остальных - как в ПСЭМ)
1. кл-ция по принадлежности к определенному классу соединений:
комплексные кислоты – Н2[SiF6]
комплексные основания – [Ag(NH3)2OH]
комплексные соли – K2[HgI4]
2. По природе лигандов: аквакомплексы, аммиакаты. Цианидные, галогенидные и т.д.
Аквакомплексы - комплексы, в которых лигандами служат молекулы воды, например [Ca(H2O)6]Cl2 - хлорид гексааквакальция. Аммиакаты и аминаты - комплексы, в которых лигандами являются молекулы аммиака и органических аминов, например: [Cu(NH3)4]SO4 - сульфат тетрамминмеди(II).
3.по знаку заряда комплекса: катионные, анионные, нейтральные
4. по внутренней структуре КС: по числу ядер, составляющих комплекс:
моноядерные - Н2[SiF6], двухядерные – [Cr2(OH)(NH3)10]Cl5 и т.д.,
5. по отсутствию или наличию циклов: простые и циклические КС.
Циклические или хелатные (клешневидные) комплексы. Они содержат би- или полидентатный лиганд, который как бы захватывает центральный атом М подобно клешням рака:Примеры: Na3[Fe(C2O4)3] - триоксалато-(III)феррат натрия, [PtEn3](NO3)4 - нитрат триэтилендиамино-платины(IV).
16. При растворении КС в воде происходит распад, причем внутренняя сфера ведет себя как единое целое.
K[Ag(CN)2] = K+ + [Ag(CN)2]-
 Наряду с этим процессом в незначительной степени происходит диссоциация внутренней сферы комплекса:
Наряду с этим процессом в незначительной степени происходит диссоциация внутренней сферы комплекса:
[Ag(CN)2]- = Ag+ + 2CN-
Для характеристики устойчивости КС вводится константа нестойкости, равная:Константа нестойкости – мера прочности КС. Чем меньше Кнест, тем более прочно КС.
Изомерия комплексных соединений.
1. Сольватная изомерия обнаруживается в изомерах, когда распределение молекул воды между внутренней и внешней сферами оказывается неодинаковой.
[Cr(H2O)6]C [Cr(H2O)5Cl]Cl2H2O [Cr(H2O)4Cl2]Cl(H2O)2
Фиолетовый светло-зеленый темно-зеленый
2. Ионизационная изомерия связана с различной легкостью диссоциации ионов из внутренней и внешней сферы комплекса.
[Pt(NH3]4Cl2]Br2 [Pt(NH3]4Br2]Cl2
[Co(NH3)5Br]SO4 и [Co(NH3)5SO4]Br - сульфат бромо-пентаммин-кобальта(III) и бромид сульфато-пентаммин-кобальта(III).
[Co(en)2NO2Cl]Cl и [Co(en)2Cl2]NO2 - хлорид нитро-хлоро-диэтилендиамино-кобальта(III) и нитрит дихлоро-диэтилендиамино-кобальта(III). 3. Координационная изомериявстречается только у бикомплексных соединений
[Со(NH3)6][Fe(CN)6] [Fe(NH3)6][Со(CN)6]
Координационная изомерия встречается в тех комплексных соединениях, где и катион и анион являются комплексными.
Например, [Cr(NH3)4][PtCl4] - тетрахлоро-(II)платинат тетраммин-хрома(II) и [Pt(NH3)4][CrCl4] - тетрахлоро-(II)хромат тетраммин-платины(II) являются координационными изомерами
4. Изомерия связи возникает только тогда, когда монодентатные лиганды могут координироваться через два разных атома.
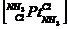
 5. Пространственная изомерия обусловлена тем, что одинаковые лиганды располагаются вокруг КО либо рядом (цис), либо напротив (транс).
5. Пространственная изомерия обусловлена тем, что одинаковые лиганды располагаются вокруг КО либо рядом (цис), либо напротив (транс).
6.Зеркальная (оптическая) изомерия, например в катионе дихлоро-диэтилендиамино-хрома(III) [Cr(en)2Cl2]+:
6. Изомерия лигандов, например, для (NH2)2(CH2)4 возможны следующие изомеры:
(NH2)—(CH2)4—NH2,CH3—NH—CH2—CH2—NH—CH3, NH2—CH(CH3) —CH2—CH2—NH2
|
из
5.00
|
Обсуждение в статье: Величина адсорбции растворенного вещества тем больше, чем больше разность полярностей между адсорбентом и растворителем. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

