 |
Главная |
Фазовые эффекты и уравнение Ван-дер-Ваальса для гетероазеотропных смесей.
|
из
5.00
|
На рисунках 3.10 – 3.13 редставлены диаграммы объем – состав фаз и энтропия – состав фаз гетероазеотропных бинарных смесей. В этих смесях в треугольнике расслоения наблюдается следующая закономерность

При этом уравнения Ван-дер-Ваальса выглядят следующим образом
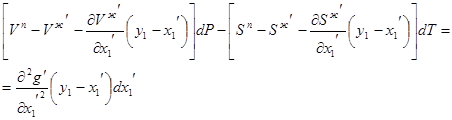 3.21
3.21
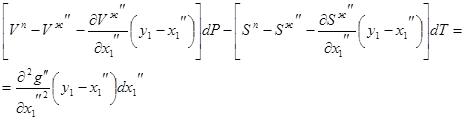 3.22
3.22
 3.23
3.23
Из этих трех уравнений два независимы. При постоянном давлении имеем:
 3.24
3.24
 3.25
3.25
или
 3.26
3.26
 3.27
3.27
Аналогичные уравнения можно получить для паровой фазы. В этом случае при Р = const
 3.28
3.28
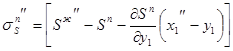 3.29
3.29
 3.30
3.30
Следовательно, получаем
 3.31
3.31
 3.32
3.32
Уравнение Ван-дер-Ваальса в терминах общих и частных фазовых эффектов.
Используя общие и частные фаэовые эффекты можно представить уравнение Ван-дер-Ваальса в форме:
для жидкой фазы  3.33
3.33
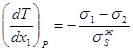 3.34
3.34
для паровой фазы  3.35
3.35
 3.36
3.36
В азеотропных точках  3.37
3.37

 ,
,  ,
,  ,
,  3.38
3.38
Заключение.
1. Определены частные фазовые эффекты для бинарных азеотропных смесей при постоянных давлении и температуре.
2. Определены общие и частные фазовые эффекты в азеотропной точке, а также слева и справа от азеотропного состава.
3. Представлено уравнение Ван-дер-Ваальса в терминах общих и частных фазовых эффектов.
Список использованной литературы:
1. Сторонкин А.В. Термодинамика гетерогенных систем. Изд. ЛГУ. 1967г.
ч.1и 2. 448с.
2. Серафимов Л.А., Фролкова А.К. Общие закономерности классификации бинарных жидких растворов в терминах избыточных термодинамических функций. АО Росвузнаука 1992г. 40с.
3. Серафимов Л.А., Фролкова А.К., Раева В.М. Термодинамический анализ пространства избыточных функций смешения бинарных растворов.//ТОХТ – 1996. Т. 30, №6. С.611-617.
4. Findley A. The phase rule and its applications, seventh edition. Longmans, green and Co, London, New York, Toronto 1931. Перевод Раковского А.В. ОНТИ 1935г.
5. Палатник Л.С., Ландау А.И.. Фазовые равновесия в многокомпонентных системах. Изд. Харьковского университета 1961г. 407с.
6. Биттрих Г.И., Гайле А.А., Лемпе Д., Проскуряков В.А., Семенов Л.В. Разделение углеводородов с использованием селективных растворителей. Химия 1987г. 192с.
7. Коган В.Б. Гетерогенные равновесия. Химия Л.:1968г. 432с.
8. Пригожин И.Р., Дефэй. Химическая термодинамика. Наука. Новосибирск. 1966 г. 510с.
9. Партингтон Д.Р., Раковский А.В. Курс химической термодинамики. Пер. с англ. Герасимова Я.И. Издание второе.1932г. Гос. науч. техн. изд-во. 384с.
10. Аносов В.Я., Озерова М.И., Фиалков Ю.Я. Основы физико-химического анализа. Наука 1976г. 504с.
11. Касаткин А.Г. Основные процессы и аппараты химической технологии. Химия 1971г., 784с.
12. Древинг В.П., Калашников П.А. Правило фаз с изложением основ термодинамики. Изд. МГУ 1964г. 456с.
13. Гиббс Д.В. Термодинамика, статистическая механика. Наука. М. 1982г. 584с.
14. Мюнстер А. Химическая термодинамика. Пер. с нем. под ред. Герасимова Я.Ч. Мир 1971. 296с.
15. Серафимов Л.А. Преобразование Лежандра и его роль в химической технологии. //Ученые записки МИТХТ 2001г., в. 3. С.4-12
16. Львов С.В. Рукопись лекций по технологии Основного органического синтеза. 1956г. 105с.
17. Гельперин Н.И. Дистилляция и ректификация. Госхимиздат. 1947 г. 312с.
18. Кириллин В.А., Шейндлин. Термодинамика растворов. Госэнергоиздат. 1980 г. 288 с.
Обозначения.
| Vп | Мольный объем паровой фазы |
| Vж | Мольный объем жидкой фазы |
| Sп | Мольная энтропия паровой фазы |
| Sж | Мольная энтропия жидкой фазы |
| yi | Концентрация компонента i в паровой фазе |
| xi | Концентрация компонента i в жидкой фазе |

| Состав паровой фазы, вектор |

| Состав жидкой фазы, вектор |

| Химический потенциал компонента i |
| Hм | Энтальпия смешения |
| Sм | Энтропия смешения |
| Gм | Изобарно-изотермический потенциал смешения |
| R | Газовая постоянная |
| P | Давление |
| T | Температура |
| m | Число молей |
| Ki | Коэффициент равномерного распределения компонента i между паровой и жидкой фазами |
| t | Параметр, равный d lnm |

| Вектор нода |

| Вектор ренода |

| Вектор состояния паровой фазы |

| Вектор состояния жидкой фазы |

| Общий фазовый эффект в паровой фазе компонента i |

| Общий фазовый эффект в жидкой фазе компонента i |

| Частный объемный фазовый эффект в паровой фазе |

| Частный объемный фазовый эффект в жидкой фазе |
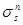
| Частный энтропийный фазовый эффект в паровой фазе |

| Частный энтропийный фазовый эффект в жидкой фазе |
|
из
5.00
|
Обсуждение в статье: Фазовые эффекты и уравнение Ван-дер-Ваальса для гетероазеотропных смесей. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

