 |
Главная |
Требования, предъявляемые к качеству питьевой и технической воды.
|
из
5.00
|
Качество воды - это характеристика состава и свойств воды, определяющая пригодность её для конкретных видов водопользования.
Природная вода не всегда пригодна для использования её в питьевых и промышленных целях из-за присутствия вредных для объекта водоснабжения веществ, поэтому различные примеси в ней нормируются. В соответствии с ГОСТ 2874-82 к питьевой и технической воде предъявляются определённые требования. Например, на наличие ионов в питьевой воде (табл. 8).
 |

Допустимое содержание ионов в питьевой воде
Загрязнение вод обусловлено поступлением в водный объект загрязняющих веществ, микроорганизмов, а также теплоты (тепловое загрязнение).
Под загрязнённостью природных вод понимают содержание в них загрязняющих веществ, микроорганизмов и теплоты, что вызывает нарушение (превышение) установленных норм (требований) качества воды.
Загрязнение вод в результате поступления патогенных и санитарно- показательных микроорганизмов называется микробным загрязнением вод.
Загрязнение вод в результате поступления теплоты называется тепловым загрязнением вод.
Под загрязнением вод понимают накопление в водных объектах посторонних объектов.
Жёсткость питьевой воды во избежание ухудшения её органолептических свойств не должна превышать 7 ммоль*экв/л и в исключительных случаях 10 ммоль*экв/л. При этом сухой остаток составляет до 1000 мг/л, сульфатов не более 500 мг/л, хлоридов до 350 мг/л, а pH находится в пределах от 6 до 9. Количество взвешенных частиц и мутность до 20 см по Снеллену, вкус, привкус и запах до 2 баллов.
По медицинским показаниям строго регламентируется и содержание фтора (0,7-1,5 мг/л). 'Как избыток, так и недостаток фтора влияет на состояние зубов у человека.
Вкус питьевой воды определяется в первую очередь присутствием гидрокарбонатов кальция и магния. Содержание этих солей до 10 мг/л делает воду вкусной, освежающей, что отличает родниковую воду от дистиллированной. Однако присутствие в воде большего количества катионов магния придает ей горьковатый вкус. Катионы Са2+ образуют с белками пищевых продуктов нерастворимые соединения, поэтому в воде с высокой жёсткостью плохо развариваются мясо и овощи. Такая вода не пригодна для питья и приготовления напитков. В ней плохо заваривается чай и при этом ухудшаются его вкусовые качества. Регулярное употребление жёсткой воды вызывает нарушение осмотического давления жидких сред организма человека.
При добавлении мыла в жёсткую воду образуются осадки и плёнки. Они представляют собой нерастворимые кальциевые и магниевые соли, являющиеся продуктами замещения ионов натрия и калия в растворимых солях высших жирных кислот (RCOOH): стеариновой (R – C17H35), пальмитиновой (R – C15H31), миристиновой (R – C13H27) и других, например:
Са2+(р.р) + 2C17H35COONa(р.р) = (С17Н35СОО)2Са(т) + 2Na+(р.р)
По этой причине ухудшается качество тканей при их стирке в жёсткой воде, а мыло в ней плохо пенится.
Вода, применяемая в качестве охлаждающего агента в системах циркуляционного водоснабжения, не должна содержать ионов НС03-, С032-, OН-, S042-, Р043-, Si032-, Са2+, Mg2+, Fe2+, Fe3+, Al3+, Zn2+, которые способствуют образованию солевых отложений. Наиболее часто встречающимся компонентом солевых отложений является СаС03. Хлорид натрия и некоторые другие примеси в котлах переходят в водяной пар и затем, осаждаясь на лопатках турбин, изменяют их профиль и соответственно снижают КПД. Вода, используемая в паровых котлах высокого давления, не должна сдержать большого количества метакремниевой кислоты. Растворённые в воде газы (О2, СО2, Н2S) повышают её коррозионную активность и придают неприятный привкус и запах (H2S, СН4), поэтому и питьевую, и техническую воду дегазируют. Содержание О2 в воде, из которой генерируется водяной пар, не должно превышать 5-40 мкг/кг (в зависимости от типа парогенератора).
Обработка воды, или водоподготовка, - это чаще всего комплекс технологических процессов по приведению её качества в соответствие с требованиями потребителей. В него входят процессы осветления и обесцвечивания, обеззараживания, стабилизации, фторирования (или обесфторивания), умягчения, опреснения, обессоливания, дегазации; \ главным среди них является умягчение.
Критерием качества воды является признак или комплекс признаков,которым производится оценка качества воды.
Обобщённая числовая оценка качества воды по совокупности основных показателей для конкретных видов водопользования называется индексом качества воды.
Уровень качества воды, установленный в интервале числовых значений свойств и состава воды, характеризующих её пригодность для конкретного вида пользования определяется классом качества воды.
Проверка соответствия показателей качества воды установленным нормам и требованиям называется контролем качества воды.
Признак, характеризующийся наименьшей безвредной концентрацией вещества в воде называется лимитирующим признаком вредности вещества в воде.
9.Технические жидкости
При эксплуатации различных транспортных средств, машин и установок, снабжённых двигателями внутреннего сгорания, кроме топлив и смазочных материалов, применяются различные технические жидкости. К ним относятся жидкости, заливаемые в системы охлаждения двигателей (охлаждающие жидкости), а также гидравлические и амортизаторные жидкости, используемые для заполнения гидроподъёмных, тормозных и амортизационных систем; различные промывочные жидкости для очистки масляных систем двигателей без их разборки и др.
9.1.Требования, предъявляемые к жидкостям для бхлаяедения двигателей
В процессе работы двигателей внутреннего сгорания детали подвергаются нагреванию, что снижает их механическую прочность. Многие узлы (камера сгорания, клапаны, цилиндры, поршни) необходимо охлаждать, чтобы поддерживать нормальное тепловое состояние двигателя. В процессе работы двигателя должен обеспечиваться отвод избытка теплоты от чрезмерно нагреваемых деталей так, чтобы их температура не превышала максимально допустимых значений. Однако большой отвод теплоты нежелателен, так как при этом ухудшается испарение топлива, что нарушает процесс сгорания, увеличивает потери энергии на преодоление трения смазочных материалов и приводит к другим нежелательным явлениям. Следовательно, перегрев и переохлаждение деталей двигателя вредны, то есть должна поддерживаться оптимальная рабочая температура.
Существует два вида охлаждения: воздушное и жидкостное. В первом случае теплота от сильно нагретых деталей двигателя отводится непосредственно в атмосферу, а во втором теплота сначала передаётся охлаждающей жидкости (охладитель), омывающей нагретые детали, а от неё отдаётся в окружающий воздух. Охладитель - жидкость, используемая для охлаждения в промышленности или быту. Обычно жидкость забирает теплоту в одном месте и переносит его в другое. На атомных электростанциях, например, охладитель переносит теплоту от ядерного реактора к парогенераторам, где теплота используется для производства пара, который вращает турбины и вырабатывает электричество.
При жидкостном охлаждении головка блоков и стенки цилиндров двигателя, окружены рубашкой, которая заполнена циркулирующей жидкостью. Эта жидкость омывает чугунные, стальные, алюминиевые, латунные детали двигателя, а также дюритовые и резиновые соединения и уплотнения. Циркуляция жидкости осуществляется с помощью насоса-помпы. Охлаждающая жидкость, перемещаясь внутрь рубашки, отбирает теплоту от стенок цилиндров и головки блоков, нагревается и поступает в радиатор, в котором часть теплоты передаётся в окружающую среду. Жидкость охлаждается и опять поступает в рубашку двигателя, В процессе работы охлаждающая жидкость нагревается до 85—100 °С, а иногда и до 105 °С. Надёжность работы системы охлаждения зависит от физико-химических свойств охлаждающих жидкостей.
Для обеспечения надёжной и длительной работы системы охлаждения, а, следовательно, эффективной и экономичной работы двигателя охлаждающая жидкость должна удовлетворять следующим требованиям:
- обеспечивать лёгкую циркуляцию по системе охлаждения (для этого жидкость должна иметь оптимальную вязкость и высокую meплоёмкость, причём вязкость жидкости должна быть такой, чтобы, с одной стороны, обеспечивалась лёгкая циркуляция, а с другой, чтобы потери жидкости через различные соединения и уплотнения были минимальными);
- иметь температуру кипения на 15—25 °С выше возможной температуры нагревания жидкости в системе охлаждения (если температура кипения жидкости ниже рабочей температуры нагревания, то в системе охлаждения образуются паровые пробкй, нарушающие нормальную циркуляцию, а также происходят большие потери жидкости от испарения);
- иметь температуру застывания на 5—10 °С ниже той возможной температуры окружающего воздуха, при которой производится эксплуатация машин;
- иметь небольшой коэффициент объёмного расширения при повышении температуры, так как температурные интервалы работы очень велики (от -20-30 °С до 100-110 °С);
- быть возможно более дешёвой, недефицитной;
- иметь невысокую вспениваемостъ;
- быть пожаробезопасной и безвредной для здоровья;
- не вызывать коррозию металлов и сплавов, не разъедать резиновые шланги и герметики;
- не вызывать н акопл ения накипи и шламов в системе охлаждения, что резко ухудшает теплоотдачу стенок и нарушает циркуляцию.
Вода как охлаждающая жидкость, в широкой практике эксплуатации двигателей внутреннего сгорания в качестве охлаждающей жидкости применяется вода, хотя она и не обеспечивает всех вышеперечисленных требований.
Вода замерзает при О °С и при этом примерно на 10 % увеличивается в объёме. Образующийся лёд оказывает большое давление на стенки системы охлаждения, что может привести к разрушению двигателя и радиатора. Поэтому при эксплуатации двигателей в холодное время года во время остановок периодически приходится прогревать двигатель, а при длительных стоянках - сливать воду из системы охлаждения.
Вода при нормальном давлении кипит при 100 С. Небольшая разница между температурой кипения воды и оптимальной температурой в системе охлаждения (80-85 °С) создаёт ряд дополнительных трудностей при эксплуатации двигателей, так как происходят большие потери воды при её испарении. Это особенно сильно сказывается при перегрузках двигателя и его работе в высокогорных районах, где из-за снижения барометрического давления вода кипит при несколько более низких температурах.
Наличие в воде растворённых газов и некоторых солей вызывает коррозийное разрушение металлов и сплавов. Высокой коррозийной активностью обладают кислород О2, углекислый газ СО2 и сероводород H2S, поэтому применять воду для охлаждения двигателей из сернистых и углекислых источников нельзя. Основное, наиболее неприятное свойство воды - возможность образования накипи и шламов в системе охлаждения.
Накипь уменьшает сечение каналов, что нарушает циркуляцию воды. Очень низкая теплопроводность накипи (в 10-15 раз меньше, чем металла) ухудшает отвод теплоты и вызывает перегрев двигателей, следовательно, повышается расход топлива и смазочного масла, усиливается детонация, снижается мощность. Интенсивность этих негативных явлений связана с химическим составом отложений и их толщиной. Чем плотнее и твёрже слой накипи, чем больше её толщина, тем больше нарушается тепловой режим двигателя и, следовательно, тем больше перерасход нефтепродуктов и падение мощности.
Несмотря на существенные отрицательные свойства воды как охлаждающей жидкости, дешевизна, недефицитность, безвредность и высокая теплоёмкость способствуют широкому использованию её в системах охлаждения.
12. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Задача 1.
Найти эквивалентные массы: H2S04, Аl(ОН)3, Fe2(S04)3 и С02.
Решение. Эквивалентная масса вещества находится по формуле:

где f – фактор эквивалентности;
М - молярная масса вещества.
Фактор эквивалентности является величиной не постоянной и
зависит от класса соединения. В условии задания представлены все
классы неорганических веществ:
H2S04 - кислота А1(ОН)3 - основание
Fe2(S04)3 - соль С02 - оксид
Для каждого из них фактор эквивалентности находится:
- для кислоты

где nН* - основность кислоты, то есть число ионов Н+ в молекуле кислоты.
- для основания

где nOН- - кислотность основания, число ионов ОН- в формульной единице основания.
- для соли

где n – число катионов (анионов) в соли;
z – модуль заряда катиона (аниона) в соли.
- для оксида

где nO – число атомов кислорода в формульной единице оксида
Исходя из этого найдём эквивалентные массы предложенных
веществ:
1) H3SO4 - серная кислота, двухосновная (содержит два иона Н+)
Молярная масса кислоты равна 1 . 2 + 32 + 16 . 4 = 98 г/моль
Эквивалентная масса равна:

2) А1(ОН)3 - гидроксид алюминия, трёхкислотное основание
(содержит три гидроксильные группы ОН-)
Молярная масса основания равна 27 + (16 + 1) . 3 = 78 г/моль
Эквивалентная масса равна:

3) Fe2(SO4)3 - сульфат железа (III), соль трехвалентного железа
(n = 2, z = 3)
Молярная масса соли равна 56 . 2 + (32 + 16 . 4) . 3 = 400 г/моль
Эквивалентная масса равна:

4) СО2 - диоксид углерода (nO = 2)
Молярная масса оксида равна 12 + 16 . 2 = 44 г/моль
Эквивалентная масса равна:

Задача 2.
Определить сколько грамм H2SO4 содержится в
а) санти- и двумолярном растворе,
б) милли- и децинормальном растворе.
Решение. Для нахождения массы растворенного вещества необходимо воспользоваться формулами:


где См - молярная концентрация (молярность), моль/л;
Сн - молярная концентрация эквивалента (нормальность), моль/л;
М - молярная масса, г/моль;
Мэ - молярная масса эквивалента, г/моль;
V - объём, л.
а) сантимолярный раствор - раствор, содержащий 0,01 моль
растворённого вещества в 1 л, соответственно концентрация раствора
(См) равна 0,01 моль/л.
Выразим из формулы (1) массу:

где См - молярная концентрация, равная 0,01 моль/л;
М - молярная масса H2SO4, равная 1 . 2 + 32 + 16 . 4 = 98 г/моль;
V - объём, равный 1 л.

Двумолярный раствор, соответственно содержит 2 моль
растворённого вещества в 1 л, то есть концентрация равна 2 моль/л.

б) миллинормальиый раствор - раствор, содержащий 0,001 моль
растворённого вещества в 1 л, соответственно концентрация раствора
(Сн) равна 0,001 моль/л.
Выразим из формулы (2) массу:
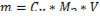
где Сн - молярная концентрация эквивалента (нормальность), равная
0,001 моль/л;
Мэ - молярная масса эквивалента H2S04, равная  .
.
nH+ - основность кислоты, то есть число ионов Н+ в формуле
молекулы кислоты.
М - молярная масса H2SO4 равная 98 г/моль;
Mэ 98/2 = 49 г/моль
V - объём, равный 1 л.

Децинормальный раствор, соответственно содержит 0,1 моль
растворённого вещества в 1 л, то есть концентрация равна 0,1 моль/л.
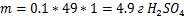
Задача 3.
Чему равен водородный показатель рН, гидроксилыгый показать
рОН, концентрация ионов водорода [H+] и концентрация гидроксид-
ионов [ОН-] в 0,025 М растворе серной кислоты.
Решение. Серная кислота является одной из сильнейших неорганических
кислот, которая в растворе практически полностью распадается на ионы:

В результате диссоциации кислоты образуется 2 моль ионов Н+ и
1 моль ионов S042-. Таким образом, концентрация ионов водорода в
растворе будет в два раза больше, чем концентрация H2S04. По условию
концентрация кислоты равна 0,025 моль/л. соответственно концентрация
ионов водорода равна 0,05 моль/л, а концентрация сульфат-ионов будет
такой же, как и концентрация кислоты:

Концентрации ионов водорода [Н+] равна 0,05 моль/л.
Водородный показать зависит от концентрации ионов водорода и
равен его отрицательному логарифму:

Подставляя в формулу (3) найденную концентрацию, получаем:

|
из
5.00
|
Обсуждение в статье: Требования, предъявляемые к качеству питьевой и технической воды. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

