 |
Главная |
Образец выполнения работы
|
из
5.00
|
| 
|
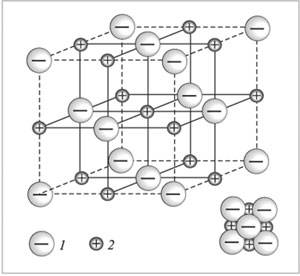
| Ионная кристаллическая решетка NaCl: 1 – хлорид-ион Cl–; 2 – катион натрия Na+ | Молекулярная кристаллическая решетка |

| 
|
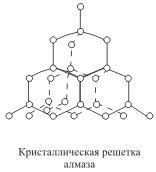
| Атомная кристаллическая решетка графита | Атомная кристаллическая решетка алмаза |
Ответьте на вопросы:
- почему для изготовления моделей требуются шарики разных размеров и цветов?
- почему для изготовления моделей требуются стержни разной длины?
Зарисуйте собранные вами модели, сделайте вывод.
Общий вывод:____________________________________________________________________ _____________________________________________________________________________
Практическая работа № 4.
Ионная химическая связь. Ковалентные полярная и неполярная связи
Цели: Повторить и систематизировать знания о строении веществ;закрепить знания о химической связи и причине ее образования.
! Внимательно изучите теоретическую часть работы. Это поможет вам правильно выполнить практическую часть работы и сделать выводы.(Учебник химии или Интернет.
Практическая часть
Задание 1. Просмотрите видеосюжет о типах химической связи. При просмотре обратите внимание на электронные конфигурации атомов при различных химических связях.
Следующие задания выполните на отметку.
Задание 2. Постройте электронно-графические формулы натрия и хлора. На их основе докажите тип связи, определив ее.
Задание 3. Постройте электронно-графические формулы двух атомов хлора. На их основе докажите тип связи, определив ее.
Задание 4. Постройте электронно-графические формулы атома серы и кислорода. На их основе докажите тип связи, определив ее.
Сделайте выводы по работе
Лабораторная работа № 5
Чистые вещества и смеси. Разделение смесей
Цель: уметь определять чистые вещества и смеси, выделять отличительные признаки; практически осуществлять разделение однородной и неоднородной смеси.
Оборудование: вещества: масло, вода, сахар, соль, песок; фильтры.
Прежде чем перейти к практической части, повторите теоретические основы темы.
Теоретическая часть
Чистое вещество содержит частицы только одного вида. Примерами могут служить серебро (содержит только атомы серебра), серная кислота и оксид углерода (IV) (содержат только молекулы соответствующих веществ). Все чистые вещества имеют постоянные физические свойства, например, температуру плавления (Тпл) и температуру кипения (Ткип).
Вещество не является чистым, если содержит какое-либо количество одного или нескольких других веществ – примесей.
Загрязнения понижают температуру замерзания и повышают температуру кипения чистой жидкости. Например, если в воду добавить соль, температура замерзания раствора понизится.
Смеси состоят из двух или болеевеществ. Почва, морская вода, воздух – все это примеры различных смесей. Многие смеси могут быть разделены на составные части – компоненты – на основании различия их физических свойств.
Различают гомогенные (однородные) и гетерогенные (неоднородные) смеси. Особенностью гомогенной смеси является то, что между компонентами такой смеси не наблюдается поверхности раздела. В этом случае говорят, что данная смесь является однофазной (фаза часть системы отделенная от других частей видимой поверхностью раздела). В пределах одной фазы физические свойства компонентов сохраняются постоянными. К гомогенным системам относятся истинные растворы (размер частиц растворенного вещества соотносится с размерами частиц растворителя и составляет ≤10-9м).
Особенностью гетерогенной смеси является то, что мы можем наблюдать поверхность раздела между ее компонентами. При переходе из одной фазы компонента в другую его свойства резко изменяются. Гетерогенные смеси иначе называются дисперсные системы. Дисперсные системы состоят из дисперсионной среды (растворитель, непрерывная фаза) и дисперсной фазы (растворенного вещества или прерывистой фазы)
К гетерогенным смесям относятся дисперсные системы (размер частиц растворенного вещества значительно превышает размер частиц растворителя и составляет ≥10-9м). Смеси, в которых размер частиц вещества составляет 10-7 -10-9 м, относятся к коллоидным системам.
К дисперсным системам относятся:
- суспензии, смесь, состоящая из твердой и жидкой фазы (обозначение Т/Ж; Т- дисперсная фаза, Ж – дисперсионная среда)
- эмульсии, смесь из 2-х и более несмешивающихся жидкостей (обозначение – Ж/Ж. Дисперсная фаза и дисперсионная среда жидкости различающиеся по плотности и температурам кипения).
Более подробно данные системы будут рассмотрены в теме растворы и дисперсные системы.
|
из
5.00
|
Обсуждение в статье: Образец выполнения работы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

