 |
Главная |
Закон Бойля — Мариотта (1659г)
|
из
5.00
|
Произведение давления на объем при неизменной температуреесть величина постоянная

Плотность газа при данной неизменнойтемпературе пропорциональна давлению.
Закон Гей-Люссака— Шарля (1802 г.)
Принеизменном давлении объем газа увеличивается при возрастании температуры.



Из уравнения следует, чтоесли понизить температуру t до —273,15°С, объем газа Vо станет равен нулю, а при ее дальнейшем понижении должен стать отрицательной величиной. Томсон (лорд Кельвин) предложил принять эту температуру за абсолютный нуль, вводя понятие термодинамической температуры:






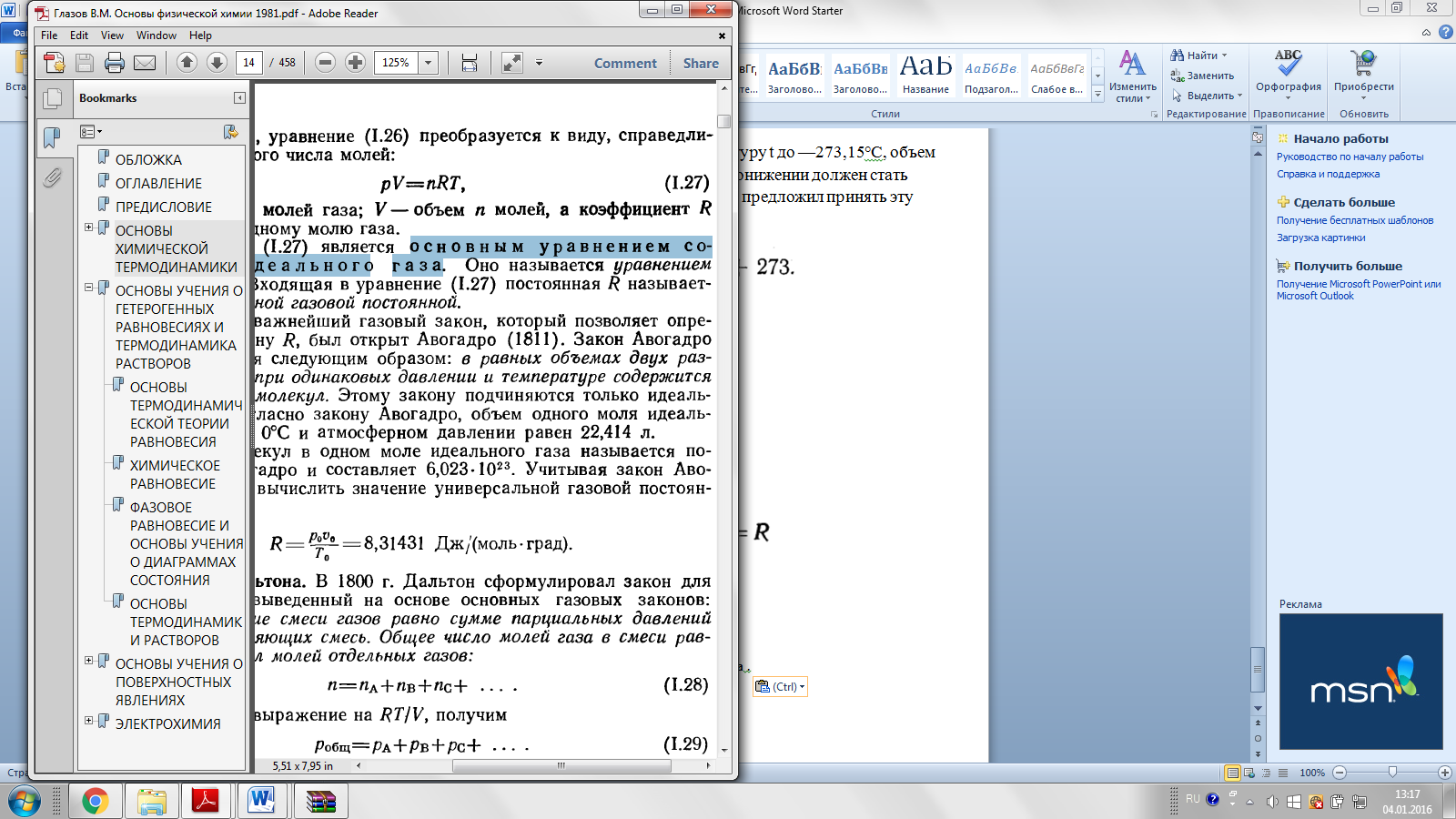
основное уравнение состояния идеального газа, Клайперона-Менделеева

- универсальная газовая постоянная
Закон Дальтона (1800 г.)
Общее давление смеси газов равно сумме парциальных давленийгазов, составляющих смесь. Общее число молей газа в смеси равносумме чисел молей отдельных газов:



где ХА— молярная доля газа А.
Число молей газа



Уравнение состояния реального газа – уравнение Ван-дер-Ваальса – общий случай, если V и m необходимо учесть для каждой частицы.
Термодинамические процессы
Если состояние системы не изменяется с течением времени, т. е. параметры состояния сохраняют постоянное значение, то такая система находится в состоянии равновесия.
При термодинамическом равновесии постоянное значение имеют только параметры, характеризующие данную систему в целом. Понятия «абсолютного» равновесия и «равновесия с учетом всех мыслимых изменений» не имеют физического смысла.
Системы, находящиеся в термодинамическом равновесии являются термодинамическими.
Выведенная из равновесия система в течение определенного времени — время релаксации — вновь приходит в равновесие.
Любые изменения хотя бы одного из параметров, характеризующих данную термодинамическую систему, обусловливают течение термодинамического процесса. Последовательность изменения параметров состояния системы, возвращающая систему в исходное состояние, формирует циклический (круговой) процесс, или цикл.
Процесс называется квазистатическим или равновесным, если он проходит через непрерывную последовательность состояний равновесия. Квазистатический процесс проходит бесконечно медленно и не являетсяфункцией времени. Любое другое изменение состояния будет нестатическим, или неравновесным.
4 базовых типа процессов .
1) изобарический или изопьезический (P=const, ΔР = 0)

2) изотремический (T=const, ΔТ = 0)

3) изохорный (V=const, ΔV = 0)

4) адиабатный (не происходит теплообмена с окружающей средой, ΔQ = 0)

|
из
5.00
|
Обсуждение в статье: Закон Бойля — Мариотта (1659г) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

