 |
Главная |
Химизм, механизм, кинетика процесса
|
из
5.00
|
Содержание
Введение
1 Выбор и обоснование метода производства 1,2 – дихлорэтана
2 Химические и физико-химические основы производства
1,2 – дихлорэтана
3 Характеристика сырья, продуктов и вспомогательных материалов
3.1 Характеристика сырья
3.2 Характеристика готовой продукции
3.3 Характеристика побочной продукции
4 Описание технологической схемы получения 1,2 – дихлорэтана
5 Материальный баланс
6 Расчет теплового баланса реактора прямого хлорирования этилена
7 Технологические расчеты
7.1 Определение основных размеров реактора
7.2 Определение диаметра основных патрубков
7.3 Расчет теплообменника Т-1
8 Механические расчеты
8.1 Расчет реактора прямого хлорирования этилена
8.2 Определение толщины тепловой изоляции
8.3 Расчет теплообменника
9 Аналитический контроль процесса
10 Автоматизация
10.1 Анализ объектов управления
10.2 Спецификация на приборы и средства автоматизации
11 Безопасность жизнедеятельности
11.1 Характеристика и анализ опасных производственных и вредных
факторов
11.2 Производственная санитария
11.3 Расчет освещения производственного помещения
11.4 Техника безопасности
12 Охрана природы
13 Экономика и организация производства
Вывод
Список литературы
Введение
Производство дихлорэтана тесно связано с винилхлоридом, поэтому современные варианты получения винилхлорида содержат технологические схемы получения дихлорэтана, как полупродукта для переработки в винилхлорид. Из винилхлорида получают поливинилхлорид, занимающего по объему выпуска второе место после полиэтилена среди полимерных материалов. [1]
Все процессы хлорирования можно подразделить на две основные группы: жидкофазные и газофазные. Преимущества первых состоят в применении умеренных температур (до 100–1200С) и легкости отвода тепла благодаря высоким коэффициентам теплоотдачи от жидкости к стенке.
Дихлорэтан – бесцветная летучая жидкость со сладковатым запахом. Дихлорэтан смешивается во всех отношениях со спиртами, бензолом, ацетоном и другими органическими соединениями.
Дихлорэтан находит широкое применение в различных областях промышленности и как растворитель: для очистки нефтепродуктов от парафинов, для экстрагирования жиров, для обезжиривания шерсти, мехов, а также для очистки металлических изделий перед хромированием или никелированием. Производство дихлорэтана является одним из важнейших факторов в производственной цепи получения полимеров, конечная цель которого получение полимерных и синтетических материалов (пластмасс), без которых нельзя представить жизнь современного общества. [1]
Сырьем для получения 1,2 – дихлорэтана являются этилен и хлор.
Выбор и обоснование метода производства 1,2 – дихлорэтана
В промышленном масштабе 1,2 – дихлорэтан получают двумя совмещенными методами, использующие хлор:
– прямое хлорирование этилена в жидкой фазе;
– окислительное хлорирование этилена в газовой фазе.
Реакция окислительного хлорирования идет с выделением тепла, катализатором служит хлорид меди. Процесс экзотермический, чем больше атомов хлора вводится, тем больше выделяется тепла. Реакция идет в газовой фазе, с теплоотводом справится трудно. Из – за наличия в реакционной массе паров воды при процессах окислительного хлорирования наблюдается сильная коррозия аппаратуры. Кроме обычной защиты корпуса реакторов керамическими материалами, для изготовления охлаждающих устройств, применяют специальные сплавы. [2]
Недостатками этого способа является образование побочных продуктов замещения, а также трудности очистки дихлорэтана. Процесс газофазного хлорирования требует особенного требования по технике безопасности.
Современная тенденция развития экономии энергетических ресурсов привела к созданию процесса прямого хлорирования этилена с использованием тепла реакции для ректификации образующегося дихлорэтана.
Получение дихлорэтана основано на химической реакции взаимодействия этилена с хлором. Процесс ведут в жидкой фазе, в присутствии катализатора хлорного железа при температуре 49–650С. Благодаря этому достигается безопасность процесса. [2]
При обосновании метода отметим, что данная технологическая схема по своему процессу проста и экономически выгодна. Выбор жидкофазного метода оправдан термической нестабильностью получаемых хлорпроизводных, обусловленной отщеплением хлористого водорода (дегидрохлорированием). После окончательной промывки получаем более чистый дихлорэтан. Степень конверсии хлора близка к 100%, а степень конверсии этилена зависит от взятого избытка его и составляет 90–97%. Выход 1,2 – дихлорэтана более 99%.
Выбор места производства обусловлен:
– близким расположением источников сырья и энергии;
– огромные запасы поваренной соли;
– соседство с Восточно – Сибирской железной дорогой;
– возможность поставки сырья из Ангарска;
– в перспективе при освоении Ковыктинского месторождения в качестве сырья будет использоваться этилен, получаемый пиролизом этановой фракции.
Химизм, механизм, кинетика процесса
Получение 1,2 – дихлорэтана методом прямого хлорирования этилена основано на реакции взаимодействия испаренного хлора и этилена в жидкой фазе. Эта реакция является каталитической и экзотермической. Поскольку экзотермическая реакция синтеза дихлорэтана в объеме газовой фазы протекает с взрывом, процесс ведут в жидкой фазе дихлорэтана. Скорость процесса жидкофазного хлорирования этилена увеличивается с ростом температуры. [3]
Получение 1,2 – дихлорэтана методом прямого хлорирования этилена основано на реакции [3]:
FeCl3
С2H4 + С12 С2H4С12 + 220 кДж/моль
Катализатором является хлорное железо (FeC13), растворенное в дихлорэтане. Механизм реакции образования 1,2 – ДХЭ при взаимодействии этилена и хлора в присутствии катализатора состоит в электрофильном присоединении с промежуточным образованием π-комплекса.
FeC13 δ+
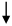



 СН2 = СН2 +С1 – С1 СН2 = СН2 CH2 – СН2+ + С1 – CH2 – СН2
СН2 = СН2 +С1 – С1 СН2 = СН2 CH2 – СН2+ + С1 – CH2 – СН2
С1 – С1δ – С1 С1 С1
π – комплекс карбоний катион
Роль хлорного железа состоит в том, что оно активирует молекулы хлора, ингибирует цепочки радикалов, ускоряет стадию перехода π – комплекса в σ – комплекс и образованию комплекса
 FеС13 + С12 FеС14- + Сl+
FеС13 + С12 FеС14- + Сl+
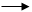 |
Хлорное железо играет роль не только катализатора присоединения, но и ингибитора радикальных процессов.
 FеС13 + Ŕ FеС12 + RС1
FеС13 + Ŕ FеС12 + RС1

 FеС12 + 1 2 С12 FеС13
FеС12 + 1 2 С12 FеС13
В качестве катализатора используют безводные хлориды железа при температуре от 0 °С до температуры кипения 1,2 – ДХЭ при давлении 0,05–0,2 МПа.
Наряду с основной реакцией получения 1,2 – ДХЭ протекают реакции заместительного хлорирования, которые ведут к образованию побочных продуктов, таких как 1,1,2 – трихлорэтан, винилхлорид и т.д. Образование других примесей, также связано со свободнорадикальными процессами.
Механизм побочных реакций следующий, сначала образуется радикал хлора.
 С12 2
С12 2 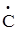 1
1
|
из
5.00
|
Обсуждение в статье: Химизм, механизм, кинетика процесса |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

