 |
Главная |
Современный состав атмосферы.
|
из
5.00
|
Химический состав тропосферы определяется присутствием четырех главных компонентов, составляющих более 99,99% её массы – азота, кислорода, аргона и углекислого газа. Кроме того, постоянными газовыми составляющими атмосферы является так же ряд микрокомпонентов, представленных главным образом редкими инертными газами и водородом. Кроме постоянных составных частей в атмосфере обычно присутствуют в переменных количествах ксенокомпоненты, являющиеся временными примесями, поступление которых обязано вулканической деятельности, жизнедеятельности биосферы, а так же производственной и бытовой деятельности человека. Большая часть ксенокомпонентов атмосферы в повышенных концентрациях оказывает отрицательное влияние на развитие растительности и живых организмов и, таким образом, должна рассматриваться как загрязнитель окружающей среды. К числу ксенокомпенентов атмосферы относятся также поступающие в нее в результате различных процессов пылевые частицы, которые часто мигрируют в воздушной среде на большие расстояние[2].
Таблица 1.
Состав атмосферы Земли (без Н2О )
| Элементы и соединения | Содержание | Общая масса, г | |||
| Об. % | Вес. % | ||||
| Главные компоненты | |||||
|
| 78,084 20,946
| 75,51 23,15 | 3,865* 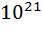 1,184*
1,184* 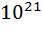
| ||
| Второстепенные компоненты | |||||
| Ar
| 0,934 0,033 99,997 | 1,28 0,046 99,986 | 65,5*  2,33*
2,33* 
| ||
| Микрокомпоненты | |||||
| Ne He Kr Xe H2 | 182* 53* 12* 0,9* 5* | 125*  7,2*
7,2*  29*
29*  3,6*
3,6*  0,3*
0,3* 
| 63,6* 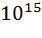 3,7*
3,7* 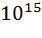 14,6*
14,6* 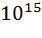 1,8*
1,8* 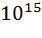 0,2*
0,2* 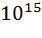
| ||
| Ксенокомпоненты | |||||


 Rn
Rn
| 15 5 4 4,5 | 9 7,6 6 6 | 4,3  4,0
4,0  3,1
3,1  2,32
2,32 
| ||
Главные компоненты атмосферы, их происхождение и источники поступления
Азот
Это главный химический элемент тропосферы, имеющий огромное значение для развития жизни на нашей планете. Из 16* 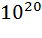 моль азота, присутствующих в земной коре, 2,7*
моль азота, присутствующих в земной коре, 2,7* 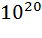 моль находится в виде
моль находится в виде  в атмосфере, 0,014*
в атмосфере, 0,014* 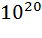 моль растворено в океанических водах и 10,3*
моль растворено в океанических водах и 10,3* 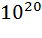 моль в той или иной форме заключены в горных породах литосферы[8].
моль в той или иной форме заключены в горных породах литосферы[8].
Азот постоянно поступает в атмосферу из глубин Земли с вулканическими эманациями, которые содержат от первых единиц до нескольких десятков процентов молекулярного азота (в газах лав гавайских вулканов, например, содержится 5,7 вес. %  ). Еще более высокое содержание азота отмечается в газах горячих источников, получивших в связи с этим наименование азотных терм. Лишь около 0,0014*
). Еще более высокое содержание азота отмечается в газах горячих источников, получивших в связи с этим наименование азотных терм. Лишь около 0,0014* 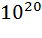 моль азота играют активную роль в круговороте этого элемента, однако роль эта весьма важна. В биосфере происходят широкая аккумуляция и фиксация азота из воздуха различными группами микроорганизмов, заключающаяся в превращении молекулярного азота
моль азота играют активную роль в круговороте этого элемента, однако роль эта весьма важна. В биосфере происходят широкая аккумуляция и фиксация азота из воздуха различными группами микроорганизмов, заключающаяся в превращении молекулярного азота  в
в  или
или  . Процесс этот идет с поглощением энергии. Другие группы бактерий участвуют в окислении
. Процесс этот идет с поглощением энергии. Другие группы бактерий участвуют в окислении  и
и  до нитрит-иона
до нитрит-иона  (Nitrosomonas) и далее до нитрат-иона
(Nitrosomonas) и далее до нитрат-иона 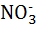 ( Nitrobacter ) по общей схеме:
( Nitrobacter ) по общей схеме:
Окисление  или
или  +
+  →
→  +
+ 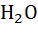 ;
;
Нитрификация  +
+  →
→ 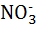 .
.
Оба процесса идут с выделением энергии[2].
Нитраты и нитриты, накапливающиеся таким образом в почве, в свою очередь, ассимилируются растениями. При этом вновь происходит восстановление их до  , который затем используется при построении аминогрупп. Важнейшим азотсодержащими соединениями животных и растений являются белки, которые содержат до 18% азота. Таким образом, органическое соединение азота, входящие в состав живого вещества, могут рассматриваться как аккумуляторы энергии[2].
, который затем используется при построении аминогрупп. Важнейшим азотсодержащими соединениями животных и растений являются белки, которые содержат до 18% азота. Таким образом, органическое соединение азота, входящие в состав живого вещества, могут рассматриваться как аккумуляторы энергии[2].
Помимо процессов накопления и связывания азота воздуха растениями в природе, правда, в более ограниченных масштабах, развивается и обратный процесс – денитрификация, осуществляемая в анаэробных условиях некоторыми видами бактерий. При этом процессе, также требующих затрат энергии, нитрат – или нитрит-ионы восстанавливаются до молекулярного азота или  . Подсчитано, что в результате денитрификации с 1 га почвы в атмосферу ежегодно поступает 50-60 кг азота. Процесс этот идет с выделением энергии по следующей общей схеме:
. Подсчитано, что в результате денитрификации с 1 га почвы в атмосферу ежегодно поступает 50-60 кг азота. Процесс этот идет с выделением энергии по следующей общей схеме:
COOH-  -
-  +
+  →
→  +
+ 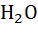 +
+  [2].
[2].
В отличие от биосферы, где миграция азота сопровождается образованием и распадом его соединений, для атмосферы образование окислов азота представляет собой хотя и закономерное, но редкое явление. Поэтому соединение азота с кислородом воздуха требует значительной энергии, в атмосфере такого рода реакции происходят только при вспышке молнии. Таким образом, содержание  в тропосфере прямо зависит от числа и интенсивности гроз. Об этом можно судить по вариациям содержания нитратов в дождевых водах районов с различным климатом. Максимальное содержание нитрат-иона отмечается в дождевых водах, богатых нрозами тропических регионов, минимальное – в осадках влажных рацонов умеренного климата[2].
в тропосфере прямо зависит от числа и интенсивности гроз. Об этом можно судить по вариациям содержания нитратов в дождевых водах районов с различным климатом. Максимальное содержание нитрат-иона отмечается в дождевых водах, богатых нрозами тропических регионов, минимальное – в осадках влажных рацонов умеренного климата[2].
С азотом связан ряд важных проблем, непосредственно касающихся состояния окружающей среды:
1. Проблема загрязнения атмосферы окислами азота;
2. Эксценссивное использование азота атмосферы в процессах техногенеза;
3. Загрязнение гидросферы и почв продуктами переработки атмосферного азота.
Техногенное поступление окислов азота в тропосферу происходит при всех процессах сжигания твердого и жидкого топлива и для индустриально развитых стран измеряется десятками миллионов тонн в год. Повышая окислительную способность атмосферы и увеличивая кислотность метеорных осадков, а так же содержание нитратов в водах районов загрязнения , аномальные концентрации окислов азота воздухе могут привлечь нежелательные изменения развития экосистем, являясь отрицательным фактором для окружающей среды. В списке наиболее важных загрязнителей, рекомендуемых для международного контроля, окислы азота помещены на пятом месте.
Не менее, а может быть более серьезную проблему для окружающей среды представляют извлечение и использование азота воздуха человеком для разнообразных промышленных и главным образом сельскохозяйственных нужд (азотные удобрения). В результате количество неактивного азота, извлекаемого из атмосферы и преобразуемого в активные соединения азота с кислородом и водородом, в конечном итоге превышает поступление его в атмосферу в результате денирификации[2].
Кислород
Запасы кислорода в атмосфере составляют порядка 1,5* 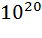 моль . Единственным источником поступления кислорода в окружающую среду являются процессы фотосинтеза. Зеленые растения биосферы ежегодно выделяют в атмосферу около 4,67*
моль . Единственным источником поступления кислорода в окружающую среду являются процессы фотосинтеза. Зеленые растения биосферы ежегодно выделяют в атмосферу около 4,67*  г кислорода. Из этого количества 11,3% производят наземные растения и 88,7% водные растения. Таким образом, растения и особенно растения океана играют исключительную роль в накоплении кислорода в атмосфере Земли. В процессах гипергенеза на поверхность земной коры происходит непрерывное связывание свободного кислорода атмосферы при окислении закисного железа ( с образованием окисного ), соединений двухвалентного марганца, сульфидов, органических остатков[3].
г кислорода. Из этого количества 11,3% производят наземные растения и 88,7% водные растения. Таким образом, растения и особенно растения океана играют исключительную роль в накоплении кислорода в атмосфере Земли. В процессах гипергенеза на поверхность земной коры происходит непрерывное связывание свободного кислорода атмосферы при окислении закисного железа ( с образованием окисного ), соединений двухвалентного марганца, сульфидов, органических остатков[3].
За всю историю существования нашей планеты в результате бактериального и растительного фотосинтеза выделилось 1,8-2,3*  г
г  . Эта величина получена на основе данных о количестве органического углерода, захороненного в осадках. Для окисления горных пород, находящихся на Земле, потребовалось бы почти на порядок большее количество кислорода. Следовательно, фотосинтезирующие организмы могли лишь частично сформировать кислородную атмосферу Земли[3].
. Эта величина получена на основе данных о количестве органического углерода, захороненного в осадках. Для окисления горных пород, находящихся на Земле, потребовалось бы почти на порядок большее количество кислорода. Следовательно, фотосинтезирующие организмы могли лишь частично сформировать кислородную атмосферу Земли[3].
На основе изучения изотопного состава  воздуха показано, что кислород атмосферы состоит на 2/3 из кислорода геологического происхождения и на 1/3 из кислорода, генерированного фотосинтезирующими организмами. Первичный кислород образовался в результате дегазации базальтовой магмы ( поступление
воздуха показано, что кислород атмосферы состоит на 2/3 из кислорода геологического происхождения и на 1/3 из кислорода, генерированного фотосинтезирующими организмами. Первичный кислород образовался в результате дегазации базальтовой магмы ( поступление  из земных недр продолжается и в настоящее время). Коллектором этого газа служат воды океана. Биогенный кислород появился позже. В итоге современная атмосфера формируется за счет как абиогенного, так и биогенного кислорода.
из земных недр продолжается и в настоящее время). Коллектором этого газа служат воды океана. Биогенный кислород появился позже. В итоге современная атмосфера формируется за счет как абиогенного, так и биогенного кислорода.
Деятельность человека в основном направлена на уменьшение количества кислорода в атмосфере. В связывании свободного кислорода воздуха заключается сущность сжигания любого органического топлива. Ежегодно человеком в процессе сжигания из атмосферы извлекается около 9* 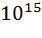 г кислорода, что составляет почти 2% его количества, вырабатываемого за этот период растениями биосферы. Отрицательное влияние деятельности человека на развитие лесов также вносит ощутимый «вклад» в уменьшение поступления кислорода в атмосферу вследствие фотосинтеза. Хотя эта отрицательная роль человека в некоторой степени компенсируется орошением и сельскохозяйственным озеленением засушливых земель, однако масштабы этих процессов до настоящего времени несоизмеримы[2].
г кислорода, что составляет почти 2% его количества, вырабатываемого за этот период растениями биосферы. Отрицательное влияние деятельности человека на развитие лесов также вносит ощутимый «вклад» в уменьшение поступления кислорода в атмосферу вследствие фотосинтеза. Хотя эта отрицательная роль человека в некоторой степени компенсируется орошением и сельскохозяйственным озеленением засушливых земель, однако масштабы этих процессов до настоящего времени несоизмеримы[2].
5. Второстепенные компоненты атмосферы
Аргон
Это наиболее распространенный инертный газ атмосферы, который почти полностью имеет радиогенное происхождение и образуется в результате распада радиоактивного изотопа калия-40 по схеме
 +е→
+е→ 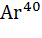 .
.
Период полураспада  , который составляет 0,0119% природного калия, равен 1,3 млрд. лет. Таким образом, поступление аргона в воздушную оболочку Земли из литосферы происходит постоянно. Изотопный состав следующий:
, который составляет 0,0119% природного калия, равен 1,3 млрд. лет. Таким образом, поступление аргона в воздушную оболочку Земли из литосферы происходит постоянно. Изотопный состав следующий: 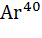 96,6%;
96,6%;  0,063%;
0,063%;  0,337%[2].
0,337%[2].
Углекислый газ
В атмосфере содержится 58* 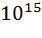 моль углерода в составе углекислого газа. В отличие от кислорода, основная масса которого заключена в атмосфере, лишь около 2% свободного
моль углерода в составе углекислого газа. В отличие от кислорода, основная масса которого заключена в атмосфере, лишь около 2% свободного  находится в газообразном состоянии в воздухе. Оставшиеся 98% углекислого газа ( 2943*
находится в газообразном состоянии в воздухе. Оставшиеся 98% углекислого газа ( 2943* 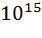 моль углерода) растворены в гидросфере и, таким образом, заключены в Мировом океане[3].
моль углерода) растворены в гидросфере и, таким образом, заключены в Мировом океане[3].
Зеленые растения в процессе фотосинтеза накапливают углерод из воздуха, превращая углекислый газ в сложные углеводороды, имеющие общую формулу –СООН-. Биологический цикл углерода в окружающей среде может быть изображен следующей схемой:
 →-СООН-→
→-СООН-→ 
газ тв. вещ-во газ
Органическое вещество, являющееся аккумулятором солнечной энергии, в определенных условиях после гибели растений и живых организмов может быть преобразовано в ископаемые, обогащенные углеродом, твердые и жидкие органические продукты, концентрирующие энергию, аккумулированную живым веществом. Эти продукты – каменный уголь и нефть – являются в настоящее время главной энергетической базой человеческого общества и уже в течение ряда столетий повсеместно используются в качестве горючих полезных ископаемых. Образование последних происходило в результате захоронения органических остатков в осадочных породах, что преграждало доступ к ним свободного кислорода. В противном случае в процессе разложения весь углерод органического веществ был окислен до  .Особенно благоприятные условия для захоронения отмерших растительных остатков в девонском и каменноугольном периодах палеозойской эры. Захоронение органических остатков в течение геологического времени сохранило в атмосфере значительное количество кислорода. На важную роль геохимическую роль захоронения углерода для формирования кислородной атмосферы земного шара указывал В. И. Вернадский. Однако в последнее столетие человек с поразительной быстротой использует горючие ископаемые, которые накапливались в земной коре в течение сотен миллионов лет. Ежегодно в атмосферу выводится порядка 0,42*
.Особенно благоприятные условия для захоронения отмерших растительных остатков в девонском и каменноугольном периодах палеозойской эры. Захоронение органических остатков в течение геологического времени сохранило в атмосфере значительное количество кислорода. На важную роль геохимическую роль захоронения углерода для формирования кислородной атмосферы земного шара указывал В. И. Вернадский. Однако в последнее столетие человек с поразительной быстротой использует горючие ископаемые, которые накапливались в земной коре в течение сотен миллионов лет. Ежегодно в атмосферу выводится порядка 0,42* 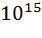 моль углерода. Столь значительные поступления техногенного углекислого газа в течение последнего столетия существенно увеличили его содержание в атмосфере. Эффект воздействия растущей концентрации
моль углерода. Столь значительные поступления техногенного углекислого газа в течение последнего столетия существенно увеличили его содержание в атмосфере. Эффект воздействия растущей концентрации  в атмосфере на окружающую среду в течение длительного времени обсуждается специалистами. Главную заботу при этом вызывает способность углекислого газа к абсорбции длинноволнового излучения, что может привести к так называемому парниковому эффекту, следствием которого должно быть постепенное потепление климата. При существующих масштабах накопления
в атмосфере на окружающую среду в течение длительного времени обсуждается специалистами. Главную заботу при этом вызывает способность углекислого газа к абсорбции длинноволнового излучения, что может привести к так называемому парниковому эффекту, следствием которого должно быть постепенное потепление климата. При существующих масштабах накопления  расчетный уровень потепления составляет 2ºС[3].
расчетный уровень потепления составляет 2ºС[3].
При переходе человечества на использование иных видов энергии ( ядерной, солнечной, геотермальной и т. д. приток 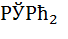 в атмосферу резко сократится. При сохранении существующих темпов роста потребления ископаемого топлива запасов каменного угля на Земле хватит на 150 лет, а нефти и газа соответственно на 50 и 49 лет. Таким образом, после 2020 г следует ожидать резкого уменьшения поступления техногенного
в атмосферу резко сократится. При сохранении существующих темпов роста потребления ископаемого топлива запасов каменного угля на Земле хватит на 150 лет, а нефти и газа соответственно на 50 и 49 лет. Таким образом, после 2020 г следует ожидать резкого уменьшения поступления техногенного  в атмосферу. В последующие несколько тысяч лет в результате регулирующего воздействия океана содержание углекислого газа в атмосфере будет понижено до уровня, соответствующего природному равновесию[1].
в атмосферу. В последующие несколько тысяч лет в результате регулирующего воздействия океана содержание углекислого газа в атмосфере будет понижено до уровня, соответствующего природному равновесию[1].
|
из
5.00
|
Обсуждение в статье: Современный состав атмосферы. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы





