 |
Главная |
Какими основными параметрами характеризуется состояние рабочего тела? Напишите уравнение состояния и укажите размерности входящих в него величин СИ.
|
из
5.00
|
Величины, которые характеризуют физическое состояние тела называются термодинамическими параметрами состояния. Такими параметрами являются удельный объем, абсолютное давление, абсолютная температура, внутренняя энергия, энтальпия, энтропия, концентрация, теплоемкость и т.д. При отсутствии внешних силовых полей (гравитационного, электромагнитного и др.) термодинамическое состояние однофазного тела можно однозначно определить 3-мя параметрами – удельным объемом (υ), температурой (Т), давлением (Р).
Если изменить термодинамическое состояние системы, т. е. подвести или отнять тепло, сжать газ или дать возможность ему расшириться, то все параметры рассматриваемой системы изменят свою величину.
Давление равно силе, действующей на единицу площади поверхности тела. Когда говорят о давлении газа или пара, под силой понимают суммарную силу ударов молекул этого газа или пара, направленную перпендикулярно к стенкам сосуда. Подавляющее большинство приборов для определения давления измеряет разницу между давлением среды (иногда называемым полным, или абсолютным давлением) р иатмосферным (барометрическим) В. Если измеряемое давление выше атмосферного, такой прибор называется манометром, а измеряемое давление — избыточным
Ризб. = Р - В.
В этом случае полное (абсолютное) давление, являющееся параметром состояния,
Р= Ризб. + В.
Если измеряемое давление ниже атмосферного, такой прибор называется вакуумметром, а измеряемое давление — вакуумметрическим (или вакуумом).
Рвак = В - Р.
В этом случае полное (абсолютное) давление
Р = В – Рвак.
Температура — это мера нагретости тела. Если теплота переходит от одного тела к другому, это значит, что температура первого тела Т1 больше температуры второго тела Т2. Если же теплообмен между телами отсутствует, температуры одинаковы T 2 = T 1 .
Удельный объем — это отношение полного объема вещества V к его массе m .
v = 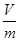 .
.
Плотность — это отношение массы вещества к его объему.
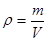 .
.
То есть плотность является величиной, обратной удельному объему.
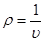 .
.
Зная удельный объем (или плотность), можно найти объем вещества по известной массе
V = m * v , V = 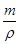 ,
,
или массу вещества по известному объему
m = V / v , m = V r .
Величины, характеризующие термодинамическое состояние газа, давление р, удельный объем v и температура Т зависят друг от друга. Если, например, газ определенной температуры занимает какой-то определенный объем, то он будет находиться под некоторым давлением. Изменение объема или температуры изменит давление газа.
Таким образом, из трех величин р, v и Т две могут быть заданы произвольно, а третья определится как функция первых двух.
Зависимость, связывающую между собой давление, объем и температуру газа, называют уравнением состояния данного газа. Это уравнение выражает основное соотношение, характеризующее термодинамические свойства газа.
Для идеального газа уравнение состояния имеет простой вид
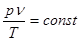 ,
,
т. е. отношение произведения абсолютного давления газа на его объем к абсолютной температуре остается постоянным. Для 1 кг газаэту постоянную величину называют газовой постоянной и обозначают буквой R :
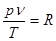 , (1-1)
, (1-1)
или
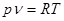 , (1-2)
, (1-2)
Уравнение состояния (1-2) часто называют уравнением Клапейрона, по имени ученого, предложившего это уравнение.
Зная два параметра газа, по уравнению (1-1) можно легко найти третий, так как R является величиной, постоянной для каждого газа. Для температурных пределов, которые обычно применяют в технике, газовые постоянные подсчитаны для большинства газов и сведены в таблицы.
Газовая постоянная R представляет работу 1 кг газа в процессе при постоянном давлении и при изменении температуры на 1 градус.
Для произвольного количества газа массой m уравнение состояния будет:
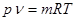 , (1-3)
, (1-3)
В 1874 г. Д.И.Менделеев основываясь на законе Дальтона ("В равных объемах разных идеальных газов, находящихся при одинаковых температурах и давлениях, содержится одинаковое количество молекул") предложил универсальное уравнение состояния для 1 кг газа, которую называют уравнением Клапейрона-Менделеева:
Р·υ = Rμ·Т/μ , (1-4)
где: μ - молярная (молекулярная) масса газа, (кг/кмоль);
Rμ = 8314,20 Дж/кмоль (8,3142 кДж/кмоль) - универсальная газовая постоянная и представляет работу 1 кмоль идеального газа в процессе при постоянном давлении и при изменении температуры на 1 градус.
Зная Rμ можно найти газовую постоянную R = Rμ/μ.
Для произвольной массы газа уравнение Клапейрона-Менделеева будет иметь вид:
Р·V = m·Rμ·Т/μ , (1-5)
Измерение или расчет каких-либо характеристик рабочего тела относятся к количественной оценке величины этих характеристик по сравнению с эталоном самой величины. Подобные эталоны приняты в международной практике при введении стандартов на сами характеристики и их эталоны. В настоящее время действует, как обязательный, международный стандарт (SI) или Российский (СИ), утвержденный в 1980 году как обязательный для всех отраслей науки и техники.
Из основных единиц системы СИ в теплотехнике применяют: единицу длины — метр (м), массы —килограмм (кг), времени — секунда (с) и температуры — Кельвин (К), из которых можно получить единицу площади (м2), объема (м3), удельного объема (м3/кг), плотности (кг/м3), скорости (м/с), ускорения (м/с2). Силу измеряют в ньютонах (1Н=1 кг*м/с2), давление в паскалях (1 Па = 1 Н/м2), энергию в джоулях (1 Дж = 1 Н*м), мощность в ваттах (1Вт=1 Дж/с).
Кроме того, используются приставки кило (к), мега (М), гига (Г), соответственно увеличивающие единицы в тысячу, миллион и миллиард раз (например, 1 кг=1000 г; 1 МПа=106 Па; 1 ГДж=109 Дж), или
милли (м) и микро (мк), соответственно уменьшающие единицы в тысячу и миллион раз (например, 1 мм = 10-3 м, 1 мкс = 10-6 с).
Единица давления паскаль очень мала и поэтому не всегда удобна, так как 1 Па меньше атмосферного давления примерно в 100 000 раз. Поэтому иногда используют такие более крупные единицы, как бар и техническая атмосфера: 1 бар = 105 Па; 1 т. атм = 1 кгс/см2 = 0,98 бар.
При измерении температуры кроме шкалы Кельвина, предусмотренной системой СИ, допускается шкала Цельсия. Температуру, измеренную в Кельвинах (К), обозначают Т, а в градусах Цельсия (° С) — t : T = t + 273,15. Как видно из этой формулы, цена деления шкал Кельвина и Цельсия одинаковая, лишь начало отсчета сдвинуто на 273,15 градуса. Поэтому при измерении разности температур значения, выраженные в Кельвинах и градусах Цельсия, одинаковы Т2-Т 1= t 2 - t 1 .
Энергию в системе СИ измеряют в джоулях. Кроме того, в теплотехнике иногда используются килокалория (обычно для измерения теплоты) и киловатт-час (для измерения электроэнергии): 1ккал = 4,19 кДж; 1 кВт*ч = 3600 кДж.
Необходимо помнить, что единицы, названные в честь ученых, пишутся с прописной буквы, а все остальные — со строчной.
|
из
5.00
|
Обсуждение в статье: Какими основными параметрами характеризуется состояние рабочего тела? Напишите уравнение состояния и укажите размерности входящих в него величин СИ. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

