 |
Главная |
Боевые ОВ - производные фосфоновой кислоты
|
из
5.00
|
В 1952 г. были синтезированы наиболее ядовитые из нервно-паралитических ОВ - фосфорилтиохолины, названные V-газами. Самый ядовитый из них - O-этиловый-S-(N,N-диизопропиламино)этиловый эфир метилфосфоновой кислоты или VX. В общей формуле для VX:

R1 = CH3-; R2 = C2H5O-; X = (i-C3H7)2NCH2CH2S-. Попадание на кожу даже одной мельчайшей капельки (около 3 мг) VX смертельно.
В быту используются аналоги зарина и VX - дезактиваторы холинэстеразы насекомых. Наиболее известны дихлофос (R1 = R2 = CH3O-; X = CCl2=CHO-), хлорофос (R1 = R2 = CH3O-; X = CCl3CH(OH)O-) и карбофос. ПДК паров дихлофоса 0,2 мг/м3, смертельная доза (для крыс) 50 мг/кг. Для хлорофоса и карбофоса ПДК 0,5 мг/м3 .
4.2. ФОСФОРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ (ФОС)
4.2.1. Значение
О роли фосфорорганических соединений в важнейших биохимических реакциях организма написаны многие тома. В любом учебнике биохимии эти вещества не только многократно упоминаются, но и подробно описываются. Без фосфорорганических соединений не мог бы идти процесс обмена углеводов в ткани мозга. Фосфорсодержащий фермент фосфорилаза способствует не только распаду, но и синтезу полисахаридов в мозгу.
В процессе окисления углеводов в ткани мозга важную роль играют дифосфо-пиридиннуклеотид и неорганический фосфат. Другой важнейший процесс – сокращение мышц поддерживается энергией, выделяющейся при реакциях с участием аденозинфосфатов. При сокращении мышцы молекула аденозинтрифосфата (АТФ) распадается на аденозиндифосфат и неорганическую фосфорную кислоту. При этом освобождается много энергии (8...11 ккал/моль). О важнейшей роли этих веществ свидетельствует и тот факт, что в мышечной ткани всегда поддерживается постоянный уровень АТФ.
Фосфорорганические соединения (ФОС) содержат в молекулах атом Р, связанный с органическими радикалами непосредственно или через гетероатом (O, S, N и др.). Первые ФОС (смесь метилфосфинов) выделены в 1846 Л.Тенаром и Берцелиусом при метилировани фосфида Са.
4.2.2. Классификация ФОС
ФОС можно классифицировать по количеству заместителей у атома Р (координационному числу), которое может быть от 1 до 6. Примеры соединений с различными координационные числом атома Р приведены в таблице 1:
Таблица 1. Примеры ФОС с различными координационными числами
| Координационное число | Соединение |
| 1 | (СH3)3C–CCP |
| 2 | [(CH3)2N]2C=PH |
| 3 | P(OCH3)3 |
| 4 | (C4H9)3PO |
| 5 | C6H5(CH3)2P(OC2H5)2 |
| 6 | CF3PHF4– |
По другой классификации, охватывающей наиболее распространенные ФОС, выделяют фосфорсодержащие кислоты и их производные (табл. 2), а также фосфины и родственные соединения.
Таблица 2. Название некоторых кислот фосфора, их эфиров и солей
| Формула | Кислоты | Эфиры и соли |
| Производные пятивалентного фосфора | ||
| (HO)3PO | Ортофосфорная (фосфорная) | Фосфаты |
| RP(O)(OH)2 | Фосфоновые кислоты | Фосфонаты |
| R2P(O)OH | Фосфиновые кислоты | Фосфинаты |
| Производные трехвалентного фосфора | ||
| HP(OH)2 | Гипофосфористая (фосфорноватистая) | Гипофосфиты |
| P(OH)3 | Фосфористая | Фосфиты |
| RP(OH)2 | Фосфонистые кислоты | Фосфониты |
| R2OPH | Фосфинистые кислоты | Фосфиниты |
К ФОС второго типа относятся первичные RPH2, вторичные R2PH, третичные фосфины R3P, а также окисленные формы последних: фосфиноксиды R3PO, фосфинсульфиды R3PS, фосфинселениды R3PSe, фосфазосоединения R3P=NR и фосфиналкилены R3P=CR2. Ко второму типу принадлежат также фосфониевые соединения R4P+X– и фосфораны R5P. Известны также полифосфины и их производные и металлокомплексы [например, (RО)3Р·СuВr, (R3P)3·RhСl, R3РО·SnR4]. Во всех приведенных формулах радикалы R могут быть одинаковыми или различными.
4.2.3. Распространение ФОС в природе
Разнообразные ФОС содержатся в живых организмах, где выполняют ответственные биологические функции. К ним, например, относятся нуклеиновые кислоты, нуклеотиды, фосфаты моносахаридов (например, глюкозо-1- и глюкозо-6-фосфаты), нуклеозидмоноциклофосфагы (например, аденозинмонофоат циклический), различные типы фосфолипидов и др. К природным ФОС также относят производные фосфоновых кислот – антибиотик фосфомицетин, фосфорные аналоги a- и b- аминокарбоновых кислот и пептиды их основе.
4.2.4. Физические свойства ФОС
ФОС могут быть газами, жидкостями или твердыми веществами. Для идентификации и изучения их используют все основные физико-химимические методы, но в первую очередь спектроскопию ЯМР 31Р. Величины химических сдвигов определяются главным образом электроотрицательностями атомов, связанные атомом Р, и степенью обратного p-дативного взаимодействия с ним. Сигналы ЯМР 31Р располагаются в очень широкой области значений (несколько сотен м.д.) и проявляют при этом выраженную специфичность.
4.2.5. Химические свойства ФОС
1. Таутомерия. Для гидрофосфорильных соединений и тиогидрофосфорильных соединений известен такой вид прототропии:

Как правило, равновесие сдвинуто в сторону формы А, однако, при наличии сильных электроноакцепторных заместителей Х и Y [например, (CF3)2POH] – в сторону Б.
Циклические средние фосфиты и амидофосфиты с протонодонорной группой в боковой цепи могут частично или полностью превращаться в гидроспирофосфорановые формы:

Тиокислоты фосфора характеризуются особым видом прототропии:

Увеличение электроноакцепторных свойств заместителей Х приводит к накоплению формы Б.
В химии ФОС известны и фосфотропные процессы:

Если радикалы R и R' одинаковые, то процесс является вырожденным. Особый вид таутомерии (псевдовращение) характерен для фосфоранов, которые способны обменивать у атома Р заместители, занимающие аксиальные и экваториальные положения:

Принцип псевдовращения широко используют для объяснения механизмов реакций ФОС.
2. Диспропорционирование. Производные пяти и особенно трехвалентного Р, в молекулах которых атомы Р связаны с различными электроноакцепторными группами, склонны к межмолекулярному обмену этими группами, например:
2(RO)2P(O)Cl <–> (RO)3P(O) + ROP(O)Cl2
Диспропорционирование обычно катализируется кислотами. Наличие циклических фрагментов в молекуле препятствует диспропорционированию.
3. Фосфорилирование. С помощью ФОС, в молекулах, которых атом Р связям с электроноакцепторной (уходящей) группой, фосфорный можно водить в состав нуклеофилов (осуществлять фосфорилирование). В качестве уходящих групп и обычно выступают галогенениды, алкиокси-, тиоалкоксигруппы и др.
P(O)Cl3 + 3ROH –> (RO)3PO + HCl
Кислоты также используются в качестве фосфорилирующих средств, однако, как правило, после предварительной, активации, т. е. после превращения кислотного гидроксила в легкоуходящую группу:
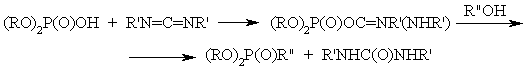
Производныс кислот с трехвалентным атомом Р проявляют более высокую фосфорилирующую активность, чем производные с пятивалентным атомом Р.
4. Важнейшие реакции производных трехвалентного Р. Эти соединения легко окисляются, присоединяют атомы S, Se, Te, Hal, иминируются, алкилируются:
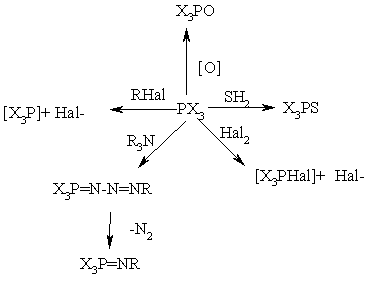
Eсли X=OAlk, SAlk, то первичный продукт взаимодействия PX3 c RHal далее распадается с образованием фосфорильного (тиофосфорильного) соединения (Арбузова реакция). При взаимодействии средних фосфитов с a-галогенкарбонильными соединения может происходить как реакция Арбузова, так и иной процесс, приводящий к фосфовиниловым эфирам (Перкова реакция):
(RO)3P + BrCH2C(O)CH3 –> (RO)2P(O)OC(CH3)=CH2
Многие производные трехвалентного Р присоединяются к сопряженным диенам и другим p,p-сопряженным системам, образующиеся продукты могут выделяться, как целевые вещества либо без выделения вступать в дальнейшие превращения.
Соединения с трехвалентным атомом Р легко обрадуют комплексы с производными переходных металлов.
5. Важнейшие реакции производных пятивалентного Р. Кислород фосфорильной группы в таких ФОС заменяется на серу под действием P2S5. В молекулах третичных фосфиноксидов он элиминируется при восстановлении трихлорсиланом.
Сложные эфиры тионовых кислот при действии алкилгалогенидов или при нагревании претерпевают тион-тиольную перегруппировку:

В большинстве фосфорильных соединений со связью С–Р a-метиленовые протоны фосфорильной группы подвижны, что приводит к их депротонированию под действием сильных основании. Образующиеся карбанионы при взаимодействии с альдегидами и кетонами образуют олефины (Хорнера реакция):

Подобная реакция происходит под действием фосфиналкиленов (Виттига реакция):
Ph3P=CH2 + RCHO –> CH2=CHR + Ph3PO
a-Гидроксифосфонаты при нагревании в присутствии оснований могут превращаться в фосфаты (фосфонат-фосфатная перегруппировка):
RCH(OH)P(O)(OR')2 –> RCH2OP(O)(OR')2
Фосфорильные соединения образуют комплексы с различными переходными и непереходными металлами с участием кислорода фосфорильной группы. Устойчивость комплексов обычно возрастает при хелатировании металла.
4.2.6. Получение ФОС
Общий путь синтеза ФОС включает три последовательные стадии:
· получение элементарного фосфора из минерального сырья.
· превращение фосфора в неорганические производные (Р4О10, РСl3, РСl5, РОСl3).
· получение ФОС взаимодействием. этих производных со спиртами, аминами, альдегидами, олефинами и др. Возможно также превращение фосфора в ФОС, минуя неорганические производные (например, взаимодействие элементного Р с алкилгалогенидами или спиртами).
Среди многочисленных способов синтеза конкретных ФОС выделяют методы позволяющие получать соединения со связью С–Р. Эти методы приведены ниже.
Фосфины и гидрофосфорильные (тиогидрофосфорильные) соединения в условиях гомолитических реакций; легко присоединяются к олефинам с образованием связи С–Р:

Эти же соединения в условиях гетеролитических реакций присоединяются по связям С=O, С=N, С=S, С=C c образованием разнообразных функционализированных ФОС:

При алкилировании и арилировании средних эфиров кислот трехвалентного фосфора образуется новая связь С–Р (реакция Арбузова).
Аналогично осуществляется реакция с использованием металлических солей гидрофосфорильных соединений (реакция Михаэлиса - Беккера):
(RO)2PONa + R'X –> R'P(O)(OR)2 + NaX
Этот синтез целесообразно проводить в условиях межфазного катализа.
Галогенангидриды органических кислот фосфора образуются присоединении РСl5 и родственных веществ к непредельным соединениям:
2PCl5 + RCH=CH2 –> RCHClCH2PCl4PCl6
При взаимодействии алканов или алкенов с РСl3 и кислородом образуются сложные смеси веществ, основными компонентами которых являются дихлорангидриды фосфоновых кислот (реакция окислительное хлорфосфонирование).
Ароматические соединения легко фосфорилируются РСl3, P2S5 и другими элекрофилами в условиях реакции Фриделя-Крафтса.
Алкилгалогениды в присутствии кислот Льюиса алкилируются PCl3 c образованием связи С–Р:

При нагревании белого и красного фосфора с арил- или алкилгалогенидами образуется смесь хлорфосфинов. Вариант этой реакции, представляющий практическое значение – алкилирование Р присутствии иода.
Связь С–Р образуется также при взаимодействии. галогенангидридов кислот фосфора с металлоорганическими соединениями, при этом один и несколько атомов галогена обмениваются на углеводородные радикалы:
PCl3 + RLi –> R3P + LiCl
4.3. АТФ
Важнейшая особенность фосфорных кислот - образование полифосфатов:

Подобные структуры являются фрагментами АТФ. Высвобождение и аккумуляция энергии в АТФ обеспечивается за счет обратимого гидролиза трифосфата до дифосфата и наоборот.

Молекула АТФ - это один своеобразный нуклеотид, который, как и другие нуклеотиды, состоит из трех компонентов: азотистого основания - аденина, углевода - рибозы, но вместо одного содержит три остатка молекул фосфорной кислоты. Связи, обозначенные значком ~, богаты энергией и называются макроэргическими. Каждая молекула АТФ содержит две макроэргические связи.

При разрыве макроэргической связи и отщеплении с помощью ферментов одной молекулы фосфорной кислоты освобождается 40 кДж/моль энергии, а АТФ при этом превращается в АДФ - аденозиндифосфорную кислоту. При отщеплении еще одной молекулы фосфорной кислоты освобождается еще 40 кДж/моль; образуется АМФ - аденозинмонофосфорная кислота. Эти реакции обратимы, то есть АМФ может превращаться в АДФ, АДФ - в АТФ.
Молекулы АТФ не только расщепляются, но и синтезируются, поэтому их содержание в клетке относительно постоянно. Значение АТФ в жизни клетки огромно. Эти молекулы играют ведущую роль в энергетическом обмене, необходимом для обеспечения жизнедеятельности клетки и организма в целом.

4.4. Фосфорные удобрения
«В 1839 г. англичанин Лауз впервые получил суперфосфат – фосфорное удобрение, легко усвояемое растениями».
| 4.4.1. Значение Одним из основных элементов питания растений является фосфор. Правильное его использование ускоряет рост и развитие растений, повышается урожай и качество сельскохозяйственной продукции. Согласно данным полевых опытов агрохимслужбы, внесение 90 кг фосфора на 1 га посевной площади в зависимости от почвы повышает урожайность озимой пшеницы на 400-500 кг/га, ячменя -- 300-600 кг/га, кукурузы -- 400-800 кг/га, подсолнечника -- 150-200 кг/га, сахарной свеклы -- 300-800 кг/га, картофеля -- 150-250 кг/га. Внесение фосфорных удобрений увеличивает содержание крахмала в клубнях картофеля, положительно влияет на накопление сахара в сахарной свекле. |
Прядильные культуры после внесения фосфорных удобрений имеют более длинное, прочное и тонкое волокно. Наряду с этим значительно увеличивается зимостойкость озимых зерновых культур, многолетних трав и плодово-ягодных культур, а также устойчивость растений при засухе. Особенностью фосфорных удобрений является также то, что они способствуют повышению эффективности действия других видов удобрений. На почвах с низким содержанием фосфора на 15-25% снижается эффективность азотных и калийных удобрений.
Большее количество фосфора содержится в товарной части урожая, поэтому значительная его часть отчуждается с продукцией. И если в природе существует кругооборот азота, в котором участвует атмосферный азот, то запасы фосфора в почве могут пополняться только благодаря внесению органических и минеральных удобрений.
Фосфорными удобрениями являются кальциевые и аммонийные соли фосфорной кислоты, а также некоторые другие соединения:
Популярное: Почему стероиды повышают давление?: Основных причин три... Как вы ведете себя при стрессе?: Вы можете самостоятельно управлять стрессом! Каждый из нас имеет право и возможность уменьшить его воздействие на нас... Личность ребенка как объект и субъект в образовательной технологии: В настоящее время в России идет становление новой системы образования, ориентированного на вхождение...  ©2015-2024 megaobuchalka.ru Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. (266)
|
Почему 1285321 студент выбрали МегаОбучалку... Система поиска информации Мобильная версия сайта Удобная навигация Нет шокирующей рекламы |
||||||||||
(0.011 сек.)

