 |
Главная |
Изучение механизма гидролиза алкоголята алюминия
|
из
5.00
|
гидролиз алкоголят алюминий оксид
Анализ отечественной и зарубежной литературы показал, что механизм гидролиза алкоголята алюминия еще совсем не изучен. В найденной литературе были предложены только схемы последовательного гидролиза всех алкокси групп, которые экспериментально не были подтверждены. В связи с этим нами была предпринята попытка изучения механизма гидролиза методом ЯМР спектроскопии. Спектры снимали на ядрах Al27, C13 и H1.
Гидролиз образцов проводился в различных условиях. В качестве осадителей использовали растворы 0.1М HCl, H2O, 1% масс раствор NH4Cl и 0.5% масс раствор NH3. Стехиометрическое отношение алкоголята алюминия и гидролизующего агента варьировалась от 0 до 1.
В ходе проведенных работ было установлено несколько интересных фактов. Но осталось еще вопросы по идентификации веществ и о механизме их образования.
1. Например, в спектре (рис. 2) исходного алкоголята алюминия четко прослеживаются четыре линии. И ни одна из них не относится к три-изопропилату алюминия. То есть, несмотря на то, что мы обычно на бумаге пишем три-изопропилат алюминия, такая форма реально не существует в растворе.
2. Из тех линий, которые мы видим, одну можно по литературным данным отнести к шести координированному алюминию с зарядом 3+ - [Al(C3H7OH)6]3+. Однако трудно представить причины образования заряженных комплексов в данной системе. Вероятнее всего, в предположении незаряженных форм, наиболее корректной интерпретацией этой формы будет: октаэдр - 6-координированный алюминий Al(OPri)3(PriOH)3 (2,5 м.д.). В исходном растворе содержание этой формы примерно 20%. Вторую линию можно отнести к димеру первой формы, вероятнее всего, H2Al(OPri)4-(OH)2 -Al(OPri)4H2 (5 м.д.).
. Исходя из химических сдвигов для третьей и четвертой линии и их относительного уширения, их можно предположительно отнести соответственно к пяти и четырех координированному алюминию. Но если представить себе четырехкоординированный алюминий еще можно в виде тетраэдра Al(OPri)3HOPri (64 м.д.), то пятикоординированный (37 м.д.) уже сложнее. Так же непонятна причина, по которой эта форма оказывается стабильной в растворе.
. Попытка изучения кинетики гидролиза алкоголята алюминия не удалась. Независимо от выбора условий, гидролиз шел быстро, практически с моментальным образованием достаточного крупных коагулятов алюминия, которые методом ЯМР обнаружить нельзя. И в дальнейшем в растворе уже никаких изменений не происходило. Все последующие процессы шли в образовавшемся геле. Поэтому в будущем нами планируется изучение уже именно геля другими методами.
. Варьируя степень гидролиза, мы не наблюдали новых форм алюминия (рис. 3). Менялось только абсолютная интенсивность описанных выше форм, относительная же оставалась прежней (рис. 4). Логично было бы предположить, что скорость гидролиза разных форм должна быть различной и относительная интенсивность их на разных стадиях гидролиза должна меняться, но, как видно из спектров, она сохраняется на каждом этапе гидролиза. Значит, между этими формами существует равновесие, которое устанавливается, быстрее, чем идет гидролиз, либо все три алкоксидных группы замещаются на гидроксильные группы практически одновременно.
Проведенные исследования показали несостоятельность приведенных в литературе схем гидролиза алкоголята алюминия, которые являются слишком упрощенными вариантов тех процессов, которые происходят при гидролизе. И они не отражают тех реальных химических превращений, которые протекают при гидролизе алкоголятов алюминия. Этот процесс нуждается в дальнейших исследованиях, и основной упор нужно сделать уже на изучение изменений, происходящих во влажном геле.
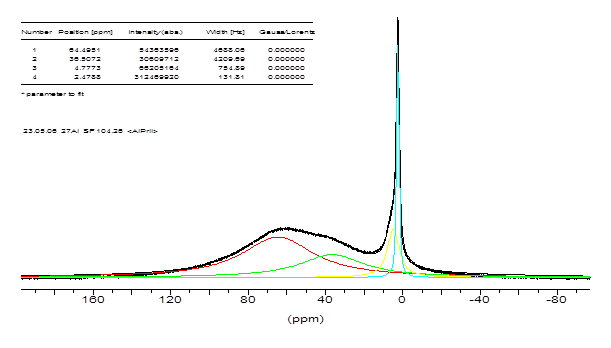
Рис.2. Спектр ЯМР 27Al р-ра изопропилата алюминия
Видны 4 формы. Ширина линии 64 м.д. много большая, чем у показанного тетраэдра и вызвана или сильным искажением тетраэдра, или сборкой полиядерного соединения, в которой часть радикалов OPr играют роль мостика.

Рис. 3. Спектр ЯМР 27Al р-ра изопропилата алюминия, к которому добавлено 0,5 экв. Н2О

Рис. 4. Доли форм алюминия в различных образцах:
Где A- пик с хим. сдвигом 63,5 м.д.,
B- пик с хим. сдвигом 36.9 м.д.,
C- пик с хим. сдвигом 6.1 м.д.,
D- пик с хим. сдвигом 2.6 м.д.
Из рисунка 4 видно, что, не смотря на колебания, которые находятся в пределах ошибки эксперимента, относительное соотношение различных форм алкоголята алюминия практически не зависит от количества и типа гидролизующего агента. Цифры по оси абсцисс относятся к условиям эксперимента, различающихся составом растворов для гидролиза и количеством добавленной воды.
|
из
5.00
|
Обсуждение в статье: Изучение механизма гидролиза алкоголята алюминия |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

