 |
Главная |
В) Гидролиз по катиону и аниону
|
из
5.00
|
Бинарные соли, образованные катионом слабого основания и анионом слабой кислоты, гидролизуются и по катиону и по аниону. Уравнение обратимой реакции гидролиза в ионном виде запишется:
Kt+ + An- + H2O Û KtOH + HАn
Константа гидролиза этого процесса равна:
 (IV.22)
(IV.22)
Вывод формул для вычисления Кгидр, hгидр, [Н+], рН осуществляется аналогично ранее рассмотренным случаям.
1. Константа гидролиза - Кгидр
Для вывода формулы Кгидр преобразуем выражение (IV.22), введя в него табличные величины констант ионизации электролитов, образующихся при гидролизе. Для процессов ионизации слабых электролитов KtOH и HАn:
KtOН Û Kt+ + OH- HАn Û Н+ + Аn-
Константы ионизации соответственно равны:
 (IV.23)
(IV.23)
 (IV.24)
(IV.24)
Проведя преобразования как и в предыдущих случаях, получим:
 (IV.25)
(IV.25)
Подставив в выражение (IV.25) уравнения (IV.23) и (IV.24), записываем формулу, позволяющую вычислить константы гидролиза, используя табличные значения констант ионизации слабых электролитов, образующихся при гидролизе.
 (IV.26)
(IV.26)
Т.е. константа гидролиза солей, образованных катионом слабого основания и анионом слабой кислоты, равна отношению ионного произведения воды к произведению констант ионизации образующихся при гидролизе слабых электролитов.
2. Степень гидролиза - hгидр
Как и в предыдущих случаях, подставим в уравнение для константы гидролиза (IV.22) концентрации прогидролизовавшейся части соли и той ее части, которая осталась непрогидролизованной, т.е.: [KtOH] = [HАn] = Сгидр = Ссоли × hгидр;
[Kt+] = [Аn-] = Ссоли - Сгидр. = Ссоли - Ссоли · hгидр = Ссоли (1 - hгидр),
 ,
,
или после сокращения получим:  , откуда
, откуда
 (IV.27)
(IV.27)
По катиону и аниону соли гидролизуются в значительной степени и значением hгидр в знаменателе пренебречь нельзя.
3. Концентрация ионов водорода [Н+] и рН растворов.
В результате реакции гидролиза рассматриваемого типа образуются слабое основание и слабая кислота:
Kt+ +An- + Н2O Û KtOH +HАn
Реакция среды в данном случае обусловлена сравнительной силой образующихся при гидролизе электролитов. Формулу для вычисления концентрации ионов водорода с точностью, достаточной для практических целей, можно вывести из уравнения для константы гидролиза (IV.22):

т.к. [KtOH] = [HАn], а [Kt+] = [An-] = Ссоли – [HАn] ≈ Ссоли, то после подстановки этих величин в формулу (IV.22) и некоторых преобразований получим:
 (IV.28)
(IV.28)
Из уравнения для константы ионизации слабой кислоты HАn выразим равновесную концентрацию кислоты:
 ;
;  ,
,
т.к. концентрация анионов в растворе приблизительно равна концентрации соли [An-] ≈ Ссоли, то  (IV.29)
(IV.29)
Подставив значение (IV.29) в выражение для константы гидролиза (IV.22), запишем уравнение:
 .
.
Сокращаем дробь и получаем величину концентрации ионов водорода:
 ;
;  ;
;
 (IV.30)
(IV.30)
Из полученной формулы видно, что концентрация ионов водорода в растворах солей, гидролизующихся по катиону и аниону, не зависит от концентрации соли, а зависит от соотношения констант ионизации кислоты и основания, образующихся при гидролизе, т.е. от их сравнительной силы.
Для того чтобы получить выражение для вычисления рН растворов, прологарифмируем уравнение (IV.30) и поменяем знаки на противоположные:
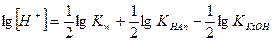 ;
;
 ;
;
 (IV.31)
(IV.31)
Выводы:
Формулы для расчета констант гидролиза бинарных солей:
 (по Kt+);
(по Kt+);  (по Аn-),
(по Аn-),
 (по Kt+ и Аn-)
(по Kt+ и Аn-)
Формулы для расчета степени гидролиза - hгидр:
 (по Kt+);
(по Kt+); 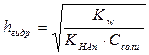 (по Аn-)
(по Аn-)
 (по Kt+ и Аn-) или
(по Kt+ и Аn-) или  (по Kt+ и Аn-)
(по Kt+ и Аn-)
Формулы для расчета концентрации ионов водорода [Н+] и рН:
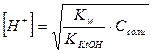 (по Kt+)
(по Kt+)  (по Kt+);
(по Kt+);
 (по Аn-)
(по Аn-)  (по Аn-);
(по Аn-);
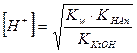 (по Kt+ и Аn-)
(по Kt+ и Аn-)  (по Kt+ и Аn-)
(по Kt+ и Аn-)
|
из
5.00
|
Обсуждение в статье: В) Гидролиз по катиону и аниону |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

