 |
Главная |
Тепловые эффекты химических реакций
|
из
5.00
|
Химическая термодинамика – это раздел химии, изучающий превращения энергии в химических процессах и энергетические характеристики различных веществ. Этот раздел химии позволяет определить направление и полноту протекания произвольной химической реакции или энергетические расходы, необходимые для осуществления реакции, которая самопроизвольно идти не может.Системой называют ограниченную часть физического мира, всякий материальный объект, обособленный физическими или вооброжаемыми границами раздела от окружающей среды.
Системы, в которых исключен какой бы то ни было обмен веществом или энергией с окружающей средой, называют изолированными. Системой называют закрытой, если она может обмениваться с окружающей средой энергией, и не может обмениваться веществом. Например, запаянная в ампуле вещество, которая попеременно помещается в холодную или горячую среду. Системы, которые могут обмениваться веществом и энергией с окружающей средой, называют открытыми. К ним относятся живые организмы. Они находятся в так называемом стационарном состоянии, когда концентрация частиц поддерживается постоянной за счет непрерывного притока и оттока веществ из системы.
При химической реакции выделяется или поглощается теплота (Qv) реакции происходит при постоянном объеме (V-cоnst), если величина Qv положительна, то реакция эндотермическая. Система поглощает тепловую 

 энергию в ходе реакции, внутренняя энергия реагентов меньше внутренней энергии продуктов.
энергию в ходе реакции, внутренняя энергия реагентов меньше внутренней энергии продуктов.

Н кон
∆Н> 0-эндотермическая реакция
Е Н исх


 Если величина Qv отрицательна, то реакция экзотермическая. Система выделяет тепловую энергию в ходе реакции внутренняя энергия реагентов выше внутренней энергии продуктов.
Если величина Qv отрицательна, то реакция экзотермическая. Система выделяет тепловую энергию в ходе реакции внутренняя энергия реагентов выше внутренней энергии продуктов.
Qv= ∆U.
Н исх
∆Н<0-экзотермическая
Н кон
Теплота Qv зависит от изменения внутренней энергии реагентов и продуктов реакции.
Теплотой реакции при постоянном давлении (Qp), при температуре (Т) называется тепловая энергия, которая поглощается в ходе реакции при постоянном давлении. Реагенты и продукты реакции приводятся в стехиометрических количествах при температуре Т начального состояния. Теплота реакции равна изменению энтальпии (∆Н) .
Qp=∆Н
Если величина Qp положительна, то реакция эндотермическая; энтальпия продуктов реакции выше энтальпии реагентов.
Если величина Qp отрицательна, то реакция экзотермическая; энтальпия продуктов реакции ниже энтальпии реагентов. Чтобы сравнить между собой теплоты разных реакций, необходимо точно указать условия, при которых эти реакции протекают. Прежде всего необходимо, чтобы реагенты и продукты реакции взяты в стехиометрических количествах, физическое состояние каждого компонента должно быть точно задано.
2 Состояние веществ и энтальпия
Запас энергии любого химического вещества в расчете на 1 моль вырастает с увеличением температуры и давления. Например; если внешнее давление равно 101,3КП, при t<0˚ С вода находится в твердом состоянии –лёд, при t>100˚С-в газообразном фазовом состоянии, а между 0˚ и 100˚ С-в виде жидкой воды. Поэтому температура – это главный переменный параметр, который используют для изменения состояния вещества, имея виду как его фазовое состояние, так и запас энергии.
Запас энергии данного вещества при заданных давлении (Р) и температуре (Т) называется энтальпией и обозначается Н(р, Т).
Энтальпия – функция состояния вещества, т.е. она определяется химической природой вещества, его фазовым состоянием и параметрами состояния, температурой и давлением.
Для любого вещества физическое состояние, в котором оно наиболее устойчиво при стандартных условиях Р=101,3Кпа Т=298К˚ , называют стандартным состоянием. Агрегатное состояние указывают справа от формул соответствующих веществ в скобках (г)-газ, (ж)-жидкость, (к)- кристалл.
Изменение энтальпии в процессе образования данного вещества в стандартных состояниях, называют стандартной энтальпией образования и обозначают ∆Нº 298
Стандартные энтальпии образования простых веществ в стандартных условиях равны нулю.
Для количественной оценки теплоты, которую получает тело, при нагревании используют понятие теплоемкости.
Теплоемкостью называют количество теплоты, соответствующее изменению температуры единицы количества вещества на 1К˚. Количество теплоты, необходимое для нагревания 1г вещества на 1К˚, называется удельной теплоемкостью.
Количество теплоты, необходимое для нагревания 1 моль вещества на 1К˚ называется молярной теплоемкостью.
С - обозначение теплоемкости.
С мол. = С уд*М. за единицу количества теплоты принято джоуль/К˚.
Пользуются теплоемкостью при Р- const- изобарическая теплоемкость Ср, при V- const- изохорическая теплоемкость Сv

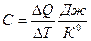 , ∆ Т= Т
, ∆ Т= Т  ,
, 
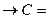
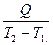
Средняя теплоёмкость при интервале температуры T 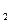 -T
-T 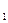
Теплоёмкость зависит от температуры, при котором её определяют.
Эта зависимость характерезуется сложной функцией: С=С  ,
,
где а, в, с –коэффициенты.
При V-const в интервале Т  теплоту вычисляют по формуле:
теплоту вычисляют по формуле:
Q  С
С 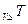 ; при Р-const Qр=
; при Р-const Qр= 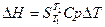
Рассмотрим взаимосвязь  и
и 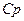

С 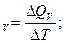 Q
Q 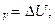 C
C 
C 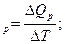 Q
Q 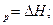 C
C 
Используя уравнения РV=RT; 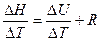 дифференцировав и прологарифмировав, получим уравнение С
дифференцировав и прологарифмировав, получим уравнение С 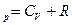
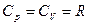 - уравнение Майера,
- уравнение Майера,
где R-универсальная газовая постоянная R=8,314Дж/кмоль*град.
Теплоемкость при постоянном давлении Cp всегда больше ,чем теплоемкость при постоянном объеме Cv, т.к. нагревание вещества при постоянном давлении сопровождается работой расширения. Тепловой эффект реакций и фазовых превращений зависит от температуры. Рассмотрим переход системы из одного состояния в другое различными путями. Например:
аА+вВ=сС+dD
Теплоемкости исходных веществ обозначим 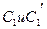 и суммарное
и суммарное  , а теплоемкости продуктов
, а теплоемкости продуктов 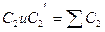 . Тепловой эффект протекающий при Т будет равен Q, а тепловой эффект протекающий при
. Тепловой эффект протекающий при Т будет равен Q, а тепловой эффект протекающий при  будет равен
будет равен 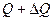 .
.
Данную реакцию можно провести двумя путями:
1) при Т выделяется Q.
2) осуществить нагревание продуктов на величину Т.
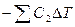


 B
B
Q T 
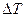
 A
A

Энергия затрачивается 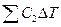
Суммарный эффект Q в - 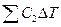
1) осуществить нагревание реагентов на 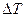 , затрачивается энергия
, затрачивается энергия 
2) осуществить процесс при  выделяется теплота
выделяется теплота 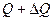
Суммарный эффект 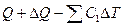 , т.к. оба пути приводят к одному и тому же состоянию, полученные эффекты равны.
, т.к. оба пути приводят к одному и тому же состоянию, полученные эффекты равны.

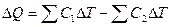
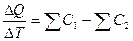 -
-
Закон Кирхгофа.
Температурный коэффициент теплового эффекта равен разности сумм теплоемкостей реагентов и сумм теплоемкостей продуктов.
Для определения тепловых эффектов, сопровождающих химические реакции, применяются приборы, называемые колориметрами.
3Закон Гесса
Тепловой эффект при постоянном давлении и произвольной температуре равен изменению энтальпии 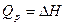 это уравнение означает, что если энтальпия продуктов меньше энтальпии реагентов, т.е. если
это уравнение означает, что если энтальпия продуктов меньше энтальпии реагентов, т.е. если  , то реакция является экзотермической. Если же энтальпия продуктов больше энтальпии реагентов, т.е.
, то реакция является экзотермической. Если же энтальпия продуктов больше энтальпии реагентов, т.е. 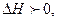 то реакция является эндотермической.
то реакция является эндотермической.
Так как энтальпии всех реагентов и всех продуктов является функциями состояния, тепловой эффект реакции не зависит от пути ее осуществления. Этот закон сформулирован русским ученым Г.И.Гессом в 1840г. Он означает, что из данных реагентов данные продукты реакции могут быть получены с помощью различных последовательностей реакций, но сумма тепловых эффектов для любой из этих последовательностей реакций будет одной и тот же. Например:
1) 

2) 
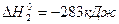
3) 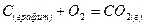
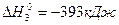
Установленный экспериментально и затем обоснованный термодинамический закон Гесса применяют для расчета эффектов любых реакций, если известны энтальпии образования 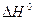 всех реагентов и продуктов реакции.
всех реагентов и продуктов реакции.
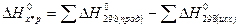
Из закона Гесса вытекают следствия:
1) Тепловой эффект разложения какого-либо соединения точно равен тепловому эффекту его образования с обратным знаком.
2) Если совершаются две реакции, приводящие из различных начальных состояний (С(графит) и С(алмаз)) к одинаковому конечному состоянию, то разница между тепловыми эффектами представляет тепловой эффект перехода из одного состояния в другое. Например:
 +393,5 кДж
+393,5 кДж
 +395,34 кДж
+395,34 кДж
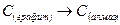 -1,83 кДж
-1,83 кДж
3) Стандартный тепловой эффект реакции  равен сумме теплот образования продуктов реакции за вычетом суммы теплот образования веществ.
равен сумме теплот образования продуктов реакции за вычетом суммы теплот образования веществ.
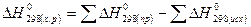
Теплота сгорания - называют тепловой эффект реакции полного сгорания 1 моль данного сведения соединения до образования высших оксидов.
Тепловой эффект реакции сгорания равен разности теплот сгорания исходных веществ и суммы теплот сгорания конечных продуктов с учетом коэффициентов в уравнении реакций.
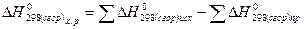
4) Если две реакции, приводящие из одинакового начального состояния к различным конечным состоянием, то разница между тепловыми эффектами представляет процесс перехода из одного конечного состояния в другое.
Н2+1/2О2=Н2О (ж)+285,84кДж
Н2+1/2О2=Н2О (г) +241,83кДж
Н2+1/2О= Н2О (к)+291,67кДж

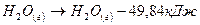
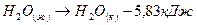
4 Второе начало термодинамики. Энтропия
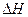 реакции является энергетической функцией состояния веществ. Первый закон термодинамики – Закон сохранения энергии: в замкнутой системе сумма всех энергии постоянна; при их взаимопревращениях энергия не теряется и не создается вновь. Этот закон применительно к химическим реакциям записывается так:
реакции является энергетической функцией состояния веществ. Первый закон термодинамики – Закон сохранения энергии: в замкнутой системе сумма всех энергии постоянна; при их взаимопревращениях энергия не теряется и не создается вновь. Этот закон применительно к химическим реакциям записывается так:
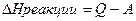 ,
,
где 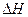 реакции –изменение энтальпии в ходе реакций;
реакции –изменение энтальпии в ходе реакций;
Q–количество теплоты, полученное реагирующей системой извне;
А – количество совершенной работы.
Если реакция не совершает работы, то А = 0 и изменение энтальпии точно равно тепловому эффекту при постоянном давлении:  .
.
Первый закон термодинамики не говорит о самопроизвольности процесса. Все процессы в природе можно разбить на две группы: самопроизвольные и не самопроизвольные.
Изменение внутренней энергии 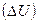 и энтальпии
и энтальпии 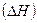 не может служить критерием, позволяющим предвидеть направления реакции. Для суждения о направлении процесса необходимо ввести новую функцию, которая отвечает ряду требований. Она должна быть функцией состояния, не зависеть от пути достижения данного состояния. Во-вторых, для всех процессов идущих самопроизвольно изменение этой функции должно иметь один и тот же знак.
не может служить критерием, позволяющим предвидеть направления реакции. Для суждения о направлении процесса необходимо ввести новую функцию, которая отвечает ряду требований. Она должна быть функцией состояния, не зависеть от пути достижения данного состояния. Во-вторых, для всех процессов идущих самопроизвольно изменение этой функции должно иметь один и тот же знак.
Существует функция состояния, которая называется энтропией (S). При самопроизвольном процессе наблюдается увеличение беспорядка. Мерой
неупорядочности служит функция - энтропия (S).
Энтропия связана с термодинамической вероятностью реализации данного состояния, число микросостояний 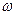 , отвечающее данному макросостоянию, называется термодинамической вероятностью этого макроскопического состояния. Энтропия S определяется через термодинамическую вероятность макросостояния уравнением Больцмана-Планка
, отвечающее данному макросостоянию, называется термодинамической вероятностью этого макроскопического состояния. Энтропия S определяется через термодинамическую вероятность макросостояния уравнением Больцмана-Планка

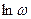
где, R  - const Больцмана
- const Больцмана
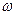 - число возможных микросостояний.
- число возможных микросостояний.
В изолированной системе самопроизвольные процессы протекают в сторону увеличения энтропии. Это второй закон термодинамики. Таким образом, если 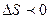 - процесс не возможен.
- процесс не возможен.
5 Свободная энергия Гиббса и Гельмгольца
Любая система определяется соотношением энтальпийного и энтропийного факторов. Первый – стремится к упорядочению, второй – к разупорядочению,
т. е. термодинамически более вероятно.
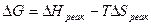
Функция, которая учитывает оба фактора - свободная энергия Гиббса (G) при постоянном давлении, при постоянном объеме – свободная энергия Гельмгольца 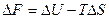
где, 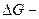 изобарно-изотермический потенциал.
изобарно-изотермический потенциал.
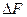 - изохорно- изотермический потенциал.
- изохорно- изотермический потенциал.
Судить о возможности самопроизвольного протекания процесса по знаку функции свободной энергии 
Если 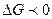 в процессе происходит уменьшение энергии, то процесс возможен; если
в процессе происходит уменьшение энергии, то процесс возможен; если 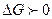 - процесс не возможен.
- процесс не возможен.
При постоянной температуре и давлении самопроизвольно протекают лишь процессы и реакции, сопровождающиеся уменьшением свободной энергии Гиббса 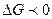 .
.
Химические реакции могут протекать самопроизвольно при следующих соотношениях между энтальпийным 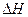 и энтропийным
и энтропийным  вкладами в
вкладами в  реакций:
реакций:
1) 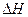 реак
реак  , если
, если  , то
, то 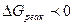 . При этом протекает экзотермическая реакция, сопровождающая уменьшением энтропии.
. При этом протекает экзотермическая реакция, сопровождающая уменьшением энтропии.
2) 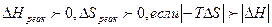 , т.е. абсолютное значение энтропийного вклада,
, т.е. абсолютное значение энтропийного вклада,  преобладает над энтропийным вкладом, то
преобладает над энтропийным вкладом, то 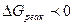 . При этом протекает эндотермическая реакция с возрастанием энтропии.
. При этом протекает эндотермическая реакция с возрастанием энтропии.
3) 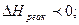
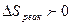 . В этом случае оба фактора действуют в одном направлении.
. В этом случае оба фактора действуют в одном направлении.
При высоких температурах (4000-6000К0) происходит диссоциация на атомы любых молекул, которая сопровождается значительно ростом энтропии. Энтропийный вклад  - становится доминирующим и поэтому, при высоких температурах химические соединения не существуют. Вблизи абсолютного нуля энтропийный вклад ничтожен, и поэтому могут самопроизвольно проходить только экзотермические процессы.
- становится доминирующим и поэтому, при высоких температурах химические соединения не существуют. Вблизи абсолютного нуля энтропийный вклад ничтожен, и поэтому могут самопроизвольно проходить только экзотермические процессы.
Энтропия чистых веществ существующих в виде идеальных кристаллов, при температуре абсолютного нуля равна нулю. 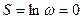 , при
, при  .
.
Биосинтез белков, жиров (липидов) и углеводов (сахаров) не может протекать самопроизвольно из-за того, что перечисленные соединения способны самопроизвольно окисляться. Реакция окисления этих веществ имеют 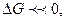 а реакции их биосинтеза из СО2 ,Н2О и N2, соответственно,
а реакции их биосинтеза из СО2 ,Н2О и N2, соответственно,  В этом главная причина сложнейшего устройства живых клеток.
В этом главная причина сложнейшего устройства живых клеток.
Контрольные вопросы
1 Какие реакции являются экзо-эндо-термическими?
2 Дайте формулировку и математическое выражение первого закона термодинамики.
3 В чем сущность закона Гесса и следствий из него?
4 Что такое теплоемкость? Какие виды теплоемкости известны? Как они связаны?
5 В чем заключается зависимость теплоемкости от температуры?
6 Что такое внутренняя энергия и как она связана с энтальпией?
7 Дайте формулировку и математическое выражение второго закона термодинамики.
8 Что такое энтропия системы? Величина энтропии обратимых и необратимых процессов.
9 Как изменяется свободная энергия в ходе самопроизвольной реакции? Можно ли принудительно осуществлять реакции, неспособные протекать самопроизвольно, если можно, то как?
10 Объясните, почему при 2900К энтропия 1 моль воды выше всего для газообразного состояния, меньше для жидкого и еще меньше для кристаллического?
Рекомендуемая литература
Основная:
1 Князев Д.А., Смарыгин С.Н. Неорганическая химия.- М.: Высшая шк., 1990, глава 5, стр. 32-50.
Дополнительная:
2 Угай Я.А. Общая химия.- М.: Высшая школа, 1977., глава 5, стр. 131-166.
3 Гольбрайх З. Е. Сборник задач и упражнений по химии. М.: Высш. шк.,1984.
|
из
5.00
|
Обсуждение в статье: Тепловые эффекты химических реакций |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

