 |
Главная |
Определение химического потребления кислорода (ХПК)
|
из
5.00
|
Введение
БПК  является обязательным анализом, но его частое определение в заводских условиях затруднительно по ряду причин.
является обязательным анализом, но его частое определение в заводских условиях затруднительно по ряду причин.
Под ХПК понимают количество растворенного в воде кислорода, выраженное в мг О 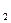 на 1 л воды, необходимое для реакций окисления находящихся в сточной воде органических соединений.
на 1 л воды, необходимое для реакций окисления находящихся в сточной воде органических соединений.
Считается, что БПК составляет около 70% от массы кислорода, требуемого для полного окисления органических веществ в пробе воды до СО2 и Н2О. При окислении сточных вод марганцевокислым калием (перманганатом) расход кислорода (БПК5) едва достигает 25% его потребности для полного окисления органических веществ по сравнению с бихроматным методом определения окисляемости (ХПК). Поэтому ХПК дает более точную оценку количества органических примесей в воде, а величина ХПК выше, чем БПК5. В численном выражении ХПК обычно на 20 – 30% больше БПК, а на картофелекрахмальных заводах в сточных водах ХПК более чем в два раза превышает БПК, что объясняется их химическим составом.
Наиболее полное определение окисляемых органических веществ достигается бихроматным методом (метод Ю. Лурье). Недостатком его является длительное окисление (двухчасовое кипячение) и большой расход концентрированной серной кислоты.
Исследовательский институт водного хозяйства г. Братиславы (Чехия) разработал ускоренный бихроматный метод определения ХПК, который в настоящее время используется и на отечественных сахарных заводах.
Цель анализа –провести оценку качества сточных вод по результатам их анализов на ХПК.
Принцип метода анализа основан на окислении органических веществ в сточных водах бихроматом калия.
Реактивы:
- 0,25 н. раствор K 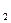 Cr
Cr 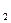 O
O 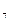 : 12,258 г K
: 12,258 г K 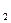 Cr
Cr 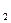 O
O 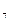 высушенного при температуре 105 ºС, растворить в 1 дм3 дистиллированной воды;
высушенного при температуре 105 ºС, растворить в 1 дм3 дистиллированной воды;
- 0,25 н. раствор соли Мора: 98 г соли Мора растворить в дистиллированной воде, добавить 20 см3 концентрированной H 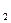 SO
SO  и после охлаждения довести дистиллированной водой до 1 дм3;
и после охлаждения довести дистиллированной водой до 1 дм3;
- сульфат серебра – кристаллический, ч.д.а;
- фенилантраниловая кислота: 0,25 г фенилантраниловой кислоты растворить в 12 см3 0,1 н. раствора NaOH и довести дистиллированной водой до 250 см3.
Приборы и материалы:
- колба Эрленмейера вместимостью 100 см3;
- пипетки;
- цилиндр на 50 см3;
- стеклянные шарики.
Ход определения
В колбу Эрленмейера вместимостью 100 см3 пипеткой вводят 10 см3 пробы или соответствующей ее части, доведенной дистиллированной водой до объема 10 см3.
Затем прибавляют приблизительно 0,1 г катализатора Ag 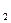 SO
SO  , пипеткой вводят точно 5 см3 0,25 н. раствора K
, пипеткой вводят точно 5 см3 0,25 н. раствора K 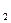 Cr
Cr 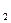 O
O 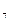 , а из цилиндра при непрерывном помешивании - 15 см3 концентрированной H
, а из цилиндра при непрерывном помешивании - 15 см3 концентрированной H 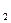 SO
SO  .
.
В раствор кладут капилляры или стеклянные шарики для спокойного кипения и выдерживают его одну минуту. Далее прибавляют 20 см3 дистиллированной воды и смесь охлаждают.
После охлаждения добавляют 3 – 4 капли N - фенилантраниловой кислоты и избыток не прореагировавшего бихромата калия оттитровывают 0,25 н. раствором соли Мора {FeSO  (NH
(NH  )
) 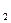 SO
SO  ·6H
·6H 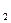 O} до светло- зеленого окрашивания.
O} до светло- зеленого окрашивания.
Затем делается глухой опыт: берут 10 см3 дистиллированной воды и делают анализ подобно рабочему опыту.
Расчеты:
Расчет ХПК проводится по формуле
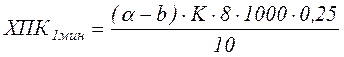 ,
,
где α - количество 0,25 н. раствора соли Мора, пошедшее на глухой опыт (10 см3 дистиллированной воды), см3;
b - количество 0,25 н. раствора соли Мора, пошедшее на рабочий опыт, см3;
К - поправочный коэффициент 0,25 н. раствора соли Мора;
10 – объем взятой пробы на анализ, см3;
0,25 – нормальность соли Мора;
Определение поправочного коэффициента К: отбирают 25 см3 0,25 н. раствора K 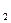 Cr
Cr 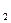 O
O 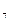 доводят дистиллированной водой до 250 см3, добавляют 20 см3 концентрированной H
доводят дистиллированной водой до 250 см3, добавляют 20 см3 концентрированной H 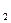 SO
SO  , охлаждают, затем добавляют 10 – 15 капель фенилантраниловой кислоты и титруют 0,25 н. раствором соли Мора
, охлаждают, затем добавляют 10 – 15 капель фенилантраниловой кислоты и титруют 0,25 н. раствором соли Мора
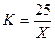 ,
,
где 25 – количество 0,25 н. раствора K 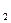 Cr
Cr 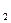 O
O 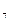 , взятого для титрования, см3;
, взятого для титрования, см3;
Х – количество 0,25 н. раствора соли Мора, пошедшее на титрование 25 см3 0,25 н. раствора, см3.
|
из
5.00
|
Обсуждение в статье: Определение химического потребления кислорода (ХПК) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

