 |
Главная |
ГИДРОЛИЗ СОЛЕЙ. КОНАСТАНТА ДИССОЦИАЦИИ
|
из
5.00
|
Наряду с понятием степени диссоциации существует понятие константы диссоциации Кд (константы равновесия для процесса диссоциации). Так, для процесса диссоциации уксусной кислоты
CH3COOH ⇄ CH3COO- + Н+
константа равновесия может быть записана так:
Кр = Кд = 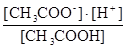 .
.
Здесь в числителе дроби произведение концентраций ионов – продуктов дис-социации, а в знаменателе – концентрация недиссоциированных молекул (кон-центрации принято обозначать символом иона или молекул в квадратных скобках).
Как и любая константа равновесия, константа диссоциации зависит от природы диссоциирующего вещества и растворителя, от температуры, но не зависит от концентрации раствора и представляет собой важную характеристику слабых электролитов, так как указывает на прочность их молекул в данном растворе. Чем меньше значение Кд в данном растворителе, тем слабее диссоциирует электролит и, следовательно, устойчивее его молекулы, и наоборот.
Константа диссоциации является характеристикой силы кислот и оснований.
Многоосновные кислоты и многокислотные основания диссоциируют ступенчато, т.е. вначале от молекулы отщепляется один из ионов, затем второй и т.д. При диссоциации многоосновных кислот сначала отщепляется один ион водорода, а в случае диссоциации многокислотных оснований – один гидроксид-ион. Каждая ступень характеризуется своим значением константы диссоциации, например:
I ступень H3PO4 ⇄ H+ + H2PO4-, K1 =  = 7,5×10-3;
= 7,5×10-3;
II ступень H2PO4- ⇄ H+ + HPO42-, K2 =  = 6,3×10-8;
= 6,3×10-8;
III ступень HPO42- ⇄ H+ + PO43-, K3 =  = 1,3×10-12.
= 1,3×10-12.
Поскольку K1>K2>K3, то вполне очевидно, что диссоциация преимущественно протекает по первой ступени и остальными стадиями можно пренебречь.
При ступенчатой диссоциации вещества распад по следующей ступени не может происходить в большей степени, чем по предыдущей.
Электролитическая диссоциация воды.
Водородный показатель
Вода – очень слабый электролит. Уравнение диссоциации воды
H2O ⇄ H+ + OH-
Константа диссоциации этого процесса определена экспериментально:
Kд =  = 1,8×10-16. (1)
= 1,8×10-16. (1)
Степень диссоциации воды очень мала, поэтому концентрация недис-социированных молекул воды практически равна общей концентрации воды. Концентрацию молекул воды можно рассчитать, разделив массу 1 л воды на массу ее моля:
[H2O] =  = 55,5 моль/л.
= 55,5 моль/л.
Подставляя в уравнение (1) величины Kд и [H2O], будем иметь для стандартных условий
[H+]×[OH-] = 10-14.
Произведение концентратов ионов водорода и гидроксид-ионов в воде (ионное произведение воды), обозначаемое Kw, при данных условиях является величиной постоянной:
Kw = [H+]×[OH-] = 10-14.
В чистой воде [H+] = [OH-] = 10-7 моль/л. Если, например, к чистой воде добавить столько кислоты, чтобы концентрация ионов H+ повысилась до 10-3 моль/л, то концентрация гидроксид-ионов понизится и произведение [H+]×[OH-] останется равным 10-14. Следовательно, в этом растворе концентрация гидроксид-ионов будет следующей:
[OH-] =  = 10-11 моль/л.
= 10-11 моль/л.
И, наоборот, если добавить к воде щелочь и повысить концентрацию гидроксид-ионов, например до 10-5 моль/л, то концентрация ионов водорода
[H+] = 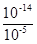 = 10-9 моль/л.
= 10-9 моль/л.
Таким образом, чтобы охарактеризовать реакцию среды любого водного раствора, достаточно указать лишь концентрацию ионов H+ (или OH-). На практике за такой показатель была принята концентрация ионов H+. В нейтральном растворе [H+] = 10-7 моль/л, в кислом [H+] > 10-7 (например 10-4, 10-6), в щелочном [H+] < 10-7 (например 10-8, 10-9).
Для удобства концентрацию H+ характеризуют водородным показателем рН:
рН = -lg[H+].
В нейтральном растворе рН = 7, в кислотном рН < 7, в щелочном рН > 7.
Задача 1. Концентрация гидроксид-ионов равна 0,00001 моль/л. Опреде-лить концентрацию ионов водорода и рН раствора.
Решение. [OH-] = 0,00001 = 1,0×1,0-5 моль/л. Используя выражение ионного произведения воды, рассчитаем концентрацию ионов водорода:
[H+] = 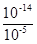 = 10-9 моль/л.
= 10-9 моль/л.
рН представляет собой десятичный логарифм концентрации водородных ионов в растворе, взятый с обратным знаком: рН = -lg[H+]. Подставим значение [H+] = 10-9 моль/л в формулу и определим водородный показатель раствора: рН = -lg10-9 = 9.
Задача 2. Приготовили 0,01М раствор NaOH. Чему равна [OH-]? Вычислите [H+].
Решение.
1. Если считать, что NaOH диссоциирует на 100 %, то [OH-] = 10-2 моль/л.
2. [H+]×[OH-] = 10-14, откуда [H+] = 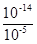 = 10-12 моль/л.
= 10-12 моль/л.
Задача 3. Определить [H+] для раствора с рН = 5. Какой это раствор - кис-лый или щелочной?
Решение. Поскольку рН = -lg[H+] и известно, что рН = 5, то [H+] = 10-5 моль/л, раствор кислый, т.е. рН < 7.
Гидролиз солей
Гидролиз - это химическая реакция взаимодействия ионов соли с ионами воды, связанная с образованием слабодиссоциирующих веществ. Наблюдающееся многообразие гидролиза практически можно свести к трем типам.
|
из
5.00
|
Обсуждение в статье: ГИДРОЛИЗ СОЛЕЙ. КОНАСТАНТА ДИССОЦИАЦИИ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

