 |
Главная |
Определение эквивалентной или нормальной концентрации
|
из
5.00
|
Эквивалентная концентрация или нормальность (Сн или Н) – число эквивалентов растворенного вещества, содержащихся в 1 л раствора (Сн = 0,75 моль/л или 0,75Н).
Пример 5. Какое количество сульфата натрия содержится в 400 мл 0,6 Н раствора?
Решение. В 1 л раствора содержится 0,6 молярных масс эквивалента сульфата натрия или См×Эм = 0,6×71 = 42.6 г.
Составим пропорцию:
в 1 л раствора содержится 42,6 г Na2SO4;
в 0.4 л раствора содержится х г Na2SO4.
Отсюда х = 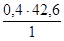 = 17,4 г Na2SO4 нужно взять, чтобы приготовить 400 мл 0,6Н раствора.
= 17,4 г Na2SO4 нужно взять, чтобы приготовить 400 мл 0,6Н раствора.
В общем виде
m = V×Сн Эм, (3)
где Сн– нормальная концентрация, моль/л;
Эм – молярная масса эквивалента растворенного вещества, г/моль.
Определение моляльной концентрации раствора
Моляльная концентрация или моляльность (Сm) - число молей растворен-ного вещества, приходящихся на 1 кг (1000 г) растворителя (Сm = 1,5 моль/кг или 1,5m).
Пример 6. В каком количестве эфира надо растворить 3,04 г анилина С6Н5NH2, чтобы получить раствор, моляльность которого равна 0,3 моль/кг.
Решение. На 1000 г растворителя (эфира) приходится 0,3 моля анилина или Сm×М = 0,3×93,3 = 27,9 г.
Составим пропорцию:
на 1000 г растворителя приходится 27,9 г анилина;
на х г растворителя приходится 3,04 г анилина.
Отсюда х  = 108,96 г эфира нужно, чтобы приготовить 0,3m раствор.
= 108,96 г эфира нужно, чтобы приготовить 0,3m раствор.
В общем виде
m1 =  , (4)
, (4)
где Сm – моляльная концентрация, моль/кг;
m – масса растворенного вещества, г;
m1 – масса растворителя, г;
М – молярная масса растворенного вещества, г/моль.
Определение титра раствора
Титр (Т) показывает, сколько г (мг) растворенного вещества содержится в 1 мл раствора (г/мл):
Т = 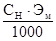 . (5)
. (5)
Пример 7. Определите титр 0,25Н раствора сульфата меди (II).
Решение. Определим титр раствора сульфата меди по формуле (4):
Т = 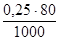 = 0,2 г/мл,
= 0,2 г/мл,
где Эм – молярная масса эквивалента сульфата меди.
Вычисления, связанные с взаимным переходом
одних форм выражения концентрации в другие
Пример 8. Определите массовую долю азотной кислоты (в процентах) в 4,3М растворе НNO3, плотность которого составляет r = 1,14 г/мл.
Решение. Определим массу кислоты, содержащейся в 1 л раствора по формуле (2):
mНNO3 = V×См×М = 1×4,3×63 = 271 г.
Определим массу 1 л (1000 мл) раствора азотной кислоты:
m = V×r = 1000×1,14 = 1140 г.
Следовательно, массовая доля кислоты составит
w НNO3 = 271/1140 = 0,238 или 23,8 %.
Пример 9. Найти моляльность, нормальность 15%-ного (по массе) раствора серной кислоты (r = 1,10 г/мл).
Решение. Для вычисления моляльности найдем сначала массу серной кислоты, приходящуюся на 1000 г воды:
1000:85 = х:15 (здесь 85 г – масса воды, содержащейся в 100 г 15%-ного раствора: 100-15 = 85 г.)
х = 15×1000/85 = 176,5 г
Молярная масса Н2SO4 равна 98 г/моль, следовательно, Сm = 176,5/98 = 1,8 моль/кг.
Для расчета нормальности раствора найдем массу серной кислоты, содержащейся в 1000 мл (т.е. 1000×1,1 = 1100 г) раствора:
1100:100 = у:15; у = 1100×15/100 = 165 г.
|
из
5.00
|
Обсуждение в статье: Определение эквивалентной или нормальной концентрации |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

