 |
Главная |
Электрохимические методы анализа. 1. ИОНОМЕТРИЯ ОСНОВАНА НА ИЗМЕРЕНИИ
|
из
5.00
|
1. ИОНОМЕТРИЯ ОСНОВАНА НА ИЗМЕРЕНИИ
1) сопротивления
2) проводимости
3) электродвижущих сил
4) количества электричества
2. ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К ЭЛЕКТРОДУ СРАВНЕНИЯ
1) постоянный потенциал
2) механическая прочность
3) высокий мембранный потенциал
4) высокая восприимчивость к изменению pH
3. ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА РАВЕН
1) EГЭ=Eк+Eа-IR
2) EГЭ=Eк-Eа-IR
3) EГЭ=Eк-Eа+IR
4) EГЭ=Eк+Eа+IR
4. В УРАВНЕНИИ ЭЛЕКТРОДНОГО ПОТЕНЦИАЛА, ПРЕДСТАВЛЕННОГО ВЫШЕ, IR-ЭТО
1) сопротивление ячейки
2) омическое падение напряжения
3) силовая постоянная
4) скачок потенциала
5. В РАСТВОРЕ, СОДЕРЖАЩЕМ ХЛОРИД-ИОНЫ, СЕРЕБРЯНЫЙ ЭЛЕКТРОД ЯВЛЯЕТСЯ ЭЛЕКТРОДОМ
1) первого рода
2) второго рода
3) третьего рода
4) четвёртого рода
6. МЕТОД, ОСНОВАННЫЙ НА ИЗМЕРЕНИИ ПОТЕНЦИАЛА ЭЛЕКТРОДА В АНАЛИЗИРУЕМОМ РАСТВОРЕ И ПОСЛЕ ВВЕДЕНИЯ ИЗВЕСТНОГО ОБЪЁМА СТАНДАРТНОГО РАСТВОРА, НАЗЫВАЕТСЯ
1) метод градуировочного графика
2) метод градуировки электрода
3) метод стандартов
4) метод добавок
7. ПРИ ПОТЕНЦИОМЕТРИЧЕСКОМ ТИТРОВАНИИ МОЖНО ОПРЕДЕЛИТЬ ОТДЕЛЬНО В РАСТВОРЕ ПРИ СОВМЕСТНОМ ПРИСУТСТВИИ СЛЕДУЮЩИЕ ГАЛОГЕНИД-ИОНЫ
1) Cl-, Br-, I-
2) Cl-, Br-
3) Br-, I-
4) Cl-, I-
8. СУММА ЭНЕРГИИ ТЕПЛОВОГО ДВИЖЕНИЯ, ВНУТРИ- И МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ, ЯДЕРНОЙ ЭНЕРГИИ ПРЕДСТАВЛЯЕТ СОБОЙ
1) внешнюю энергию
2) внутреннюю энергию
3) энтальпию
4) связанную энергию
9. ПРИ ПОВЕШЕНИИ ТЕМПЕРАТУРЫ НА 1º0ПО ПРАВ ИЛУ ВАНТ-ГОФФА СКОРОСТЬ РЕАКЦИИ УВЕЛИЧИВАЕТСЯ В
1) 1-2 раза
2) 2-4 раза
3) 4-6 раз
4) 10 раз
10. ЕСЛИ В КАЖДОЙ ИЗ ОКИСЛИТЕЛЬНО- ВОССТАНОВИТЕЛЬНЫХ ПАР ПЕРЕНОСИТСЯ ОДИНАКОВОЕ ЧИСЛО ЭЛЕКТРОНОВ, ТО РЕАКЦИЮ НАЗЫВАЮТ
1) сопоставимой
2) соразмерной
3) дивергентной
4) комплиментарной
11. В ОСНОВЕ КУЛОНОМЕТРИЧЕСКОГО МЕТОДА АНАЛИЗА ЛЕЖАТ ЗАКОНЫ
1) Кулона
2) Ампера
3) Фарадея
4) Нернста
12. МАССА ВЕЩЕСТВА, ВЫДЕЛИВШЕГОСЯ НА ЭЛЕКТРОДЕ В ПРОЦЕССЕ ЭЛЕКТРОЛИЗА ПРИ ПРОТЕКАНИИ ЕДИНИЦЫ КОЛИЧЕСТВА ЭЛЕКТРИЧЕСТВА
1) массовый эквивалент
2) электрохимическая единица
3) эквивалент массы
4) электрохимический эквивалент
13. КОЛИЧЕСТВО ЭЛЕКТРИЧЕСТВА, КОТОРОЕ НУЖНО ЗАТРАТИТЬ НА ВЫДЕЛЕНИЕ 1 МОЛЯ ВЕЩЕСТВА В ПРОЦЕССЕ ЭЛЕКТРОЛИЗА НАЗЫВАЕТСЯ
1) число Фарадея
2) электрохимическая единица
3) коэффициент Кулона
4) единица Кулона
14. КОЛИЧЕСТВО ЭЛЕКТРИЧЕСТВА, ПЕРЕНОСИМОЕ В 1 СЕКУНДУ ПРИ ПОСТОЯННОЙ СИЛЕ ТОКА В 1 АМПЕР, НАЗЫВАЕТСЯ
1) Фарадей
2) Кулон
3) Вебер
4) Тесла
15. ЭЛЕКТРОЛИТИЧЕСКАЯ ЯЧЕЙКА, В КОТОРОЙ ПРИ ЗАМЫКАНИИ ЦЕПИ СО 100%-НЫМ ВЫХОДОМ ПО ТОКУ ПРОТЕКАЕТ ЭЛЕКТРОХИМИЧЕСКАЯ РЕАКЦИЯ ИЗВЕСТНОЙ СТЕХИОМЕТРИИ, НАЗЫВАЕТСЯ
1) кондуктометр
2) кулонометр
3) гальванометр
4) потенциостат
16. ТИТРАНТ, ОБРАЗУЮЩИЙСЯ В РЕЗУЛЬТАТЕ ЭЛЕКТРОХИМИЧЕСКОЙ РЕАКЦИИ НА ЭЛЕКТРОДЕ, НАЗЫВАЕТСЯ
1) электролитический титрант
2) электрогенерированный кулонометрический титрант
3) кулоногенерированный титрант
4) титрант электродной генерации
17. ПРЯМАЯ КУЛОНОМЕТРИЯ ИСПОЛЬЗУЕТСЯ ДЛЯ ОПРЕДЕЛЕНИЯ
1) электрогенерируемых веществ
2) электронеактивных веществ
3) поляризуемых веществ
4) электроактивных веществ
18. ПРИЧИНОЙ ВОЗНИКНОВЕНИЯ КОНЦЕНТРАЦИОННОЙ ПОЛЯРИЗАЦИИ ЯВЛЯЕТСЯ
1) увеличение количества восстановленного вещества
2) обеднение поверхностного слоя электрода электроактивным веществом
3) уменьшение перенапряжения на электроде
4) высокая плотность тока
19. ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ, СОСТАВЛЕННЫЙ ИЗ КАДМИЕВОГО КАТОДА, ПОГРУЖЁННОГО В РАСТВОР СОЛИ КАДМИЯ, И МЕДНОГО КАТОДА, ПОГРУЖЁННОГО В РАСТВОР СОЛИ МЕДИ – ЭТО


 1) Cd Cu 2+(0.01M ) Cd 2+(0.01M ) Cu
1) Cd Cu 2+(0.01M ) Cd 2+(0.01M ) Cu

 2) Cd Cd 2+(0.01M ) Cu
2) Cd Cd 2+(0.01M ) Cu
Cu 2+(0.01M )



 3) Cd Cd 2+(0.01M ) Cu 2+(0.01M ) Cu
3) Cd Cd 2+(0.01M ) Cu 2+(0.01M ) Cu

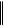
 4) Cu Cd 2+(0.01M ) Cu 2+(0.01M ) Cd
4) Cu Cd 2+(0.01M ) Cu 2+(0.01M ) Cd
20. УРАВНЕНИЕ ЭЛЕКТРОХИМИЧЕСКОЙ ЯЧЕЙКИ – ЭТО
1) EГЭ= Ea- Ek+ IR
2) EГЭ= Ek- Ea+ IR
3) EГЭ= Ea+ Ek- IR
4) EГЭ= Ek- Ea- IR
21. КАКАЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА ЯВЛЯЕТСЯ НЕОБРАТИМОЙ
1)
| |
+ 5e + 8H +
« Mn2+
+ 4H 2O
2) Ag + + e « Ag
| |
Fe(CN )4-
| |
+ 2e « 2Br -
22. ПРИ ПРОХОЖДЕНИИ ТОКА 0,8 А ЧЕРЕЗ РАСТВОР В ТЕЧЕНИИ 15,2 МИНУТ НА КАТОДЕ ВЫДЕЛИТСЯ
1) 0,065 г О2
2) 0,2402 г Сu
3) 0,0605 г Сu
4) 0,2402 г О2
23. КОНДУКТОМЕТРИЯ ОСНОВАНА НА ИЗМЕРЕНИИ
1) сопротивления
2) удельного сопротивления
3) подвижности ионов
4) удельной электропроводности
24. В ПРОВОДНИКАХ ВТОРОГО РОДА ПЕРЕНОС ЭЛЕКТРИЧЕСТВА ОСУЩЕСТВЛЯЕТСЯ
1) движением электронов
2) движением ионов
3) движением атомов к катоду или аноду
4) движением свободных электронов, не участвующих в образовании связей
25. УМЕНЬШЕНИЕ ЭЛЕКТРИЧЕСКОЙ ПРОВОДИМОСТИ В КОНЦЕНТРИРОВАННЫХ РАСТВОРАХ ПРОИСХОДИТ ЗА СЧЁТ
1) увеличения сил межионного взаимодействия
2) образования пересыщенного раствора
3) увеличения давления на стенки сосуда
4) уменьшения скорости движения электронов
26. ПРОВОДИМОСТЬ РАСТВОРА, СОДЕРЖАЩЕГО 1 МОЛЬ ЭКВИВАЛЕНТА ВЕЩЕСТВА И НАХОДЯЩИМИСЯ МЕЖДУ ДВУМЯ ПАРАЛЛЕЛЬНЫМИ ЭЛЕКТРОДАМИ, РАССТОЯНИЕ МЕЖДУ КОТОРЫМИ 1 СМ, НАЗЫВАЕТСЯ
1) молярной проводимостью
2) удельной проводимостью
3) эквивалентной проводимостью
4) предельная проводимость
27. ТОРМОЖЕНИЕ ДВИЖЕНИЯ ИОНА ПОД ДЕЙСТВИЕМ ЭЛЕКТРИЧЕСКОГО ПОЛЯ НАЗЫВАЕТСЯ
1) релаксационным торможением
2) электростатическим торможением
3) компенсационным торможением
4) электрофоретическим торможением
28. СУЩЕСТВЕННО БОЛЬШЕЙ ПОДВИЖНОСТЬЮ ПО СРАВНЕНИЮ С БОЛЬШИНСТВОМ ИОНОВ ОБЛАДАЕТ ИОН
1) аммония
2) водорода
3) калия
4) серебра
29. УДЕЛЬНАЯ ЭЛЕКТРОПРОВОДНОСТЬ СВЯЗАНА С ПОДВИЖНОСТЬЮ ПО СООТНОШЕНИЮ
 1) c = 10-3A ål C
1) c = 10-3A ål C
d i i
2) c = 10-3Cl
3) c = 103Cl
 4) c = C 1000
4) c = C 1000
l
30. ЕДИНИЦЕЙ ИЗМЕРЕНИЯ ЭЛЕКТРОПРОВОДНОСТИ ЯВЛЯЕТСЯ
1) Ом
2) Ом-1
3) Ом·см
4) См·см-1
31. ДЛЯ КОНДУКТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ ПРИГОДНЫ РЕАКЦИИ
1) окислительно-восстановительные и кислотно-основные
2) осадительные или косплексообразования
3) кислотно-основные или осадительные
4) комплексообразования или окислительно- восстановительные
32. В УРАВНЕНИИ
R = r d , r - ЭТО
 A
A
1) удельное сопротивление
2) удельная электропроводность
3) плотность тока
4) эквивалентная электропроводность
|
из
5.00
|
Обсуждение в статье: Электрохимические методы анализа. 1. ИОНОМЕТРИЯ ОСНОВАНА НА ИЗМЕРЕНИИ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

