 |
Главная |
ПОСЛЕДОВАТЕЛЬНОСТЬ ЭЛЕКТРОДНЫХ ПРОЦЕССОВ
|
из
5.00
|
При наличии нескольких видов ионов или недиссоциированных молекул электрохимически активных веществ возможно протекание нескольких электродных реакций. Рассмотрим их последовательность. Так как на катоде идет реакция восстановления, т.е. прием электронов окислителем, то в первую очередь должны реагировать наиболее сильные окислители. На катоде прежде всего протекает реакция с наиболее положительным потенциалом.
Для катодного восстановления при электролизе водного раствора электролита все окислители можно разделить на 3 группы:
а) ионы металлов, потенциал которых существенно более отрицательнее потенциала водородного электрода. К ним относятся ионы щелочных и щелочноземельных металлов, стоящих левее алюминия в ряду напряжений. В водных растворах этих металлов на катоде выделяется водород:
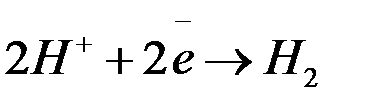 . Эти металлы могут быть получены электролизом расплавов солей этих металлов (
. Эти металлы могут быть получены электролизом расплавов солей этих металлов ( 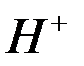 отсутствуют);
отсутствуют);
б) окислители, потенциал которых более положителен чем потенциал водородного электорда. Это ионы  платиновый
платиновый 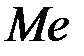 , кислород, галогены. В присутствии этих ионов
, кислород, галогены. В присутствии этих ионов 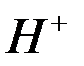 не восстанавливается.
не восстанавливается.
в) ионы, потенциал которых мало отличается от потенциала водородного электрода. Это ионы
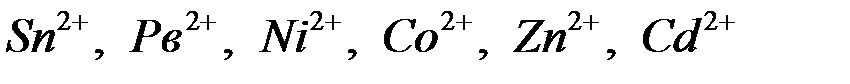 и др., стоящие в ряду напряжений между
и др., стоящие в ряду напряжений между 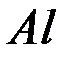 и водородом.
и водородом.
При сравнении этих потенциалов 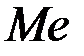 и водорода можно было бы сделать вывод о невозможности выделения металла на катоде. Однако, следует учесть, что стандартный водородный потенциал относится к активности ионов водорода
и водорода можно было бы сделать вывод о невозможности выделения металла на катоде. Однако, следует учесть, что стандартный водородный потенциал относится к активности ионов водорода 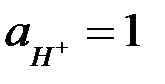 , т.е. рН=0. С увеличением рН потенциал водородного электрода становится отрицательнее. Например, при рН=5,0;
, т.е. рН=0. С увеличением рН потенциал водородного электрода становится отрицательнее. Например, при рН=5,0;  и
и 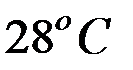
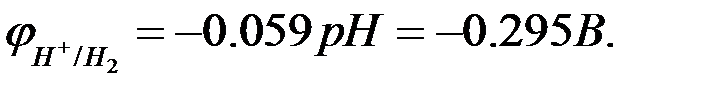 В то же время потенциалы металла в области, где не происходит выпадения их нерастворимых гидроксидов, от рН не зависит. Видно, что при рН=5 потенциал водородного электрода отрицательнее стандартных потенциалов
В то же время потенциалы металла в области, где не происходит выпадения их нерастворимых гидроксидов, от рН не зависит. Видно, что при рН=5 потенциал водородного электрода отрицательнее стандартных потенциалов 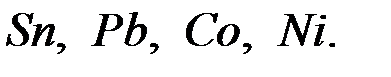 Наряду с этим следует учесть, что выделение водорода на многих катодах происходит с более высокой поляризацией, чем у многих металлов. Таким образом, при некоторой плотности тока потенциал выделения водорода становится отрицательнее, чем потенциал выделения металла, поэтому на катоде может выделиться металл.
Наряду с этим следует учесть, что выделение водорода на многих катодах происходит с более высокой поляризацией, чем у многих металлов. Таким образом, при некоторой плотности тока потенциал выделения водорода становится отрицательнее, чем потенциал выделения металла, поэтому на катоде может выделиться металл.
При электролизе часть количества электричества расходуется на выделение водорода, часть на выделение металла. Доля общего количества электричества (в%), которая расходуется на выделение одного из веществ, называется выходом по току этого вещества:
 ,
,
где 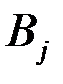 — выход по току
— выход по току  -го вещества;
-го вещества;  — количество электричества, израсходованное на превращение
— количество электричества, израсходованное на превращение  -го вещества;
-го вещества; 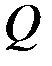 — общее количество электричества, прошедшее через электрод.
— общее количество электричества, прошедшее через электрод.
Итак, с увеличением катодной поляризации растет выход по току металла, поэтому в данном случае высокое водородное перенапряжение — явление положительное. Вследствии этого из водных растворов удается выделить на катоде 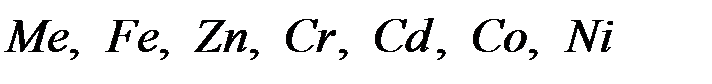 и др. металлы.
и др. металлы.
На катоде протекают реакции окисления восстановления, т.е. отдача электронов, поэтому в первую очередь на аноде должны реагировать наиболее сильные восстановители-вещества, имеющие наиболее отрицательный потенциал.
На аноде может протекать несколько процессов:
а) растворение металла:

б) окисление ионов 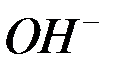 :
:
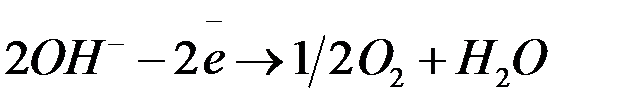
в) окисление других веществ, присутствующих в растворе или около электрода,
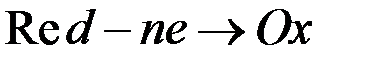
Если 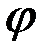 металлического анода <
металлического анода <  , то идет растворение анода (электролиз с растворимым анодом).
, то идет растворение анода (электролиз с растворимым анодом).
Если  >
>  , то протекает электролиз с нерастворимым анодом. В качестве нерастворимых анодов применяют
, то протекает электролиз с нерастворимым анодом. В качестве нерастворимых анодов применяют 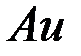 и платиновые металлы,
и платиновые металлы, 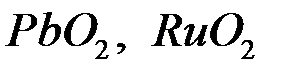 , графит. В этом случае идет окисления либо
, графит. В этом случае идет окисления либо 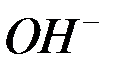 — ионов, или другие ионы или недиссоциированных молекул восстановителей. Если а растворе присутствует ионы
— ионов, или другие ионы или недиссоциированных молекул восстановителей. Если а растворе присутствует ионы  , то на аноде идет их окисление до
, то на аноде идет их окисление до 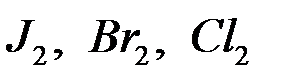 . Сначала выделяется
. Сначала выделяется  , затем все остальные
, затем все остальные 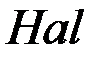 . Фтор из раствора получить нельзя, получают из расплавов фторидов. Ионы
. Фтор из раствора получить нельзя, получают из расплавов фторидов. Ионы 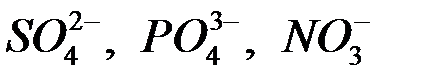 на аноде не окисляются, здесь идет выделение кислорода.
на аноде не окисляются, здесь идет выделение кислорода.
Рассмотрим электролиз водных растворов солей 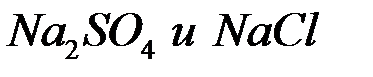 при
при 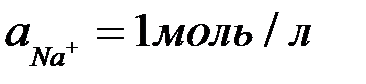 ; в растворе имеем ионы
; в растворе имеем ионы 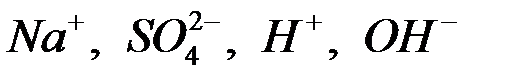 .
.
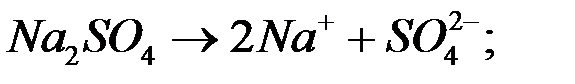
 При рН= 7,0 потенциал водородного электрода при
При рН= 7,0 потенциал водородного электрода при  и 250 С равен
и 250 С равен
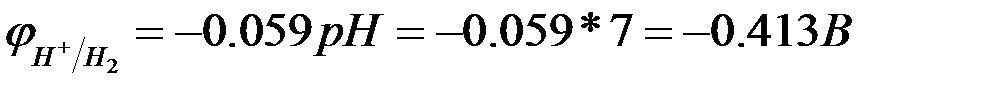
т.к. 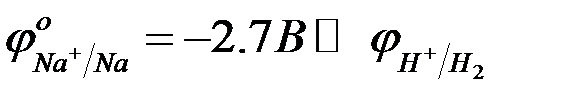 , то на катоде выделяется водород, на аноде -кислород. При электролизе
, то на катоде выделяется водород, на аноде -кислород. При электролизе  протекают реакции по уравнениям:
протекают реакции по уравнениям:
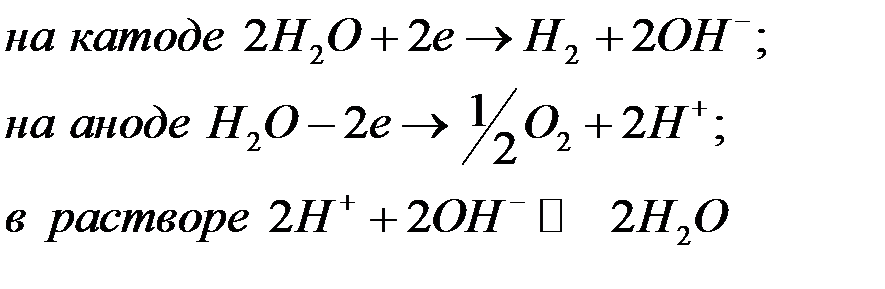
Суммарной является реакция разложения Н2О:
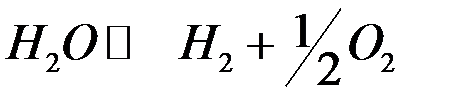 .
.
б) Раствор  при
при 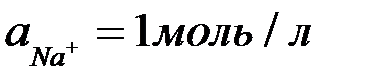 и
и 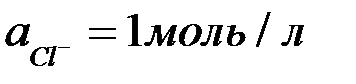 .
.
В растворе ионы 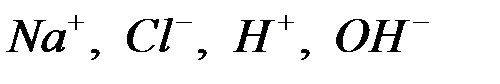 :
:
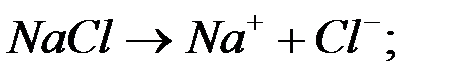

На катоде будет выделяться водород. На аноде возможно 2 реакции по уравненям:

При 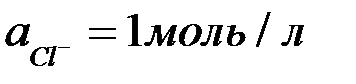
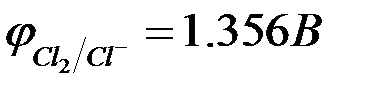
В нейтральном растворе равновесный потенциал кислородного электрода при  равен
равен
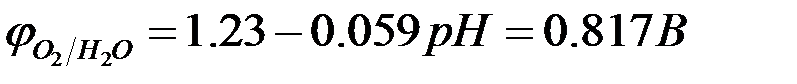
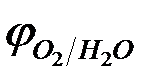 <
< 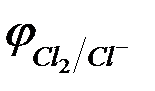 , однако
, однако 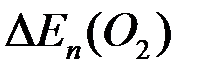 >
> 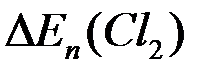 , поэтому при высоких плотностях тока в основном выделяется хлор. Т.е. на катоде выделяется водород, на аноде -хлор. В системе идет процесс:
, поэтому при высоких плотностях тока в основном выделяется хлор. Т.е. на катоде выделяется водород, на аноде -хлор. В системе идет процесс:
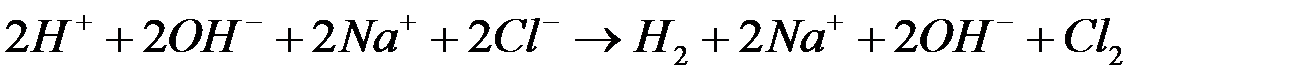 .
.
Пример 1. Определить массу цинка, который выделится на катоде при электролизе раствора 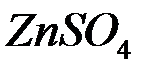 в течение 1ч. при токе 26,8 А, если выход цинка по току равен 50%.
в течение 1ч. при токе 26,8 А, если выход цинка по току равен 50%.
Решение: Согласно закону Фарадея,

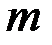 — масса вещества, окисленного или восстановленного на электроде;
— масса вещества, окисленного или восстановленного на электроде; 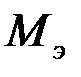 — масса моля эквивалентов вещества;
— масса моля эквивалентов вещества;  — ток;
— ток; 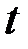 — продолжительность электролиза, с;
— продолжительность электролиза, с; 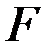 ≈ 96 500 Кл/моль.
≈ 96 500 Кл/моль.
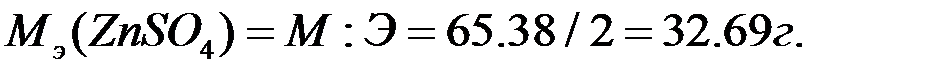

Т.к. выход по тока 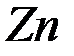 50%, то
50%, то  .
.
|
из
5.00
|
Обсуждение в статье: ПОСЛЕДОВАТЕЛЬНОСТЬ ЭЛЕКТРОДНЫХ ПРОЦЕССОВ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

