 |
Главная |
Частные реакции на анионы III аналитической группы
|
из
5.00
|
Сульфат железа(II) восстанавливает нитриты и нитраты до оксида азота(II). Нитраты в присутствии концентрированной серной кислоты, нитриты в присутствии разбовленного раствора серной кислоты. Оксида азота(II) образует с сульфатом железа(II) непрочное комплексное соединение бурого цвета:
2NaNO3+6FeSO4+4H2SO4 (конц.)→Fe2(SO4)3+2NO↑+4Na2SO4+4H2O
NO3-+4H++3e-→NO↑+2H2O|2
2Fe2+-2e-→2Fe3+ |3
2NO3-+8H++6Fe2+→2NO↑+4H2O+6Fe3+
2NaNO2+2FeSO4+2H2SO4 (разв.)→Fe2(SO4)3+2NO↑+Na2SO4+2H2O
NO2-+2H++1e-→NO↑+H2O|2
2Fe2+-2e-→2Fe3+ |1
2NO2-+4H++2Fe2+→2NO↑+2H2O+2Fe3+
FeSO4+NO↑→[Fe(NO)]SO4
С дифениламином:
Нитрат- и нитрит-ионы в концентрированной серной кислоте образуют соединение хиноидной структуры синего цвета.
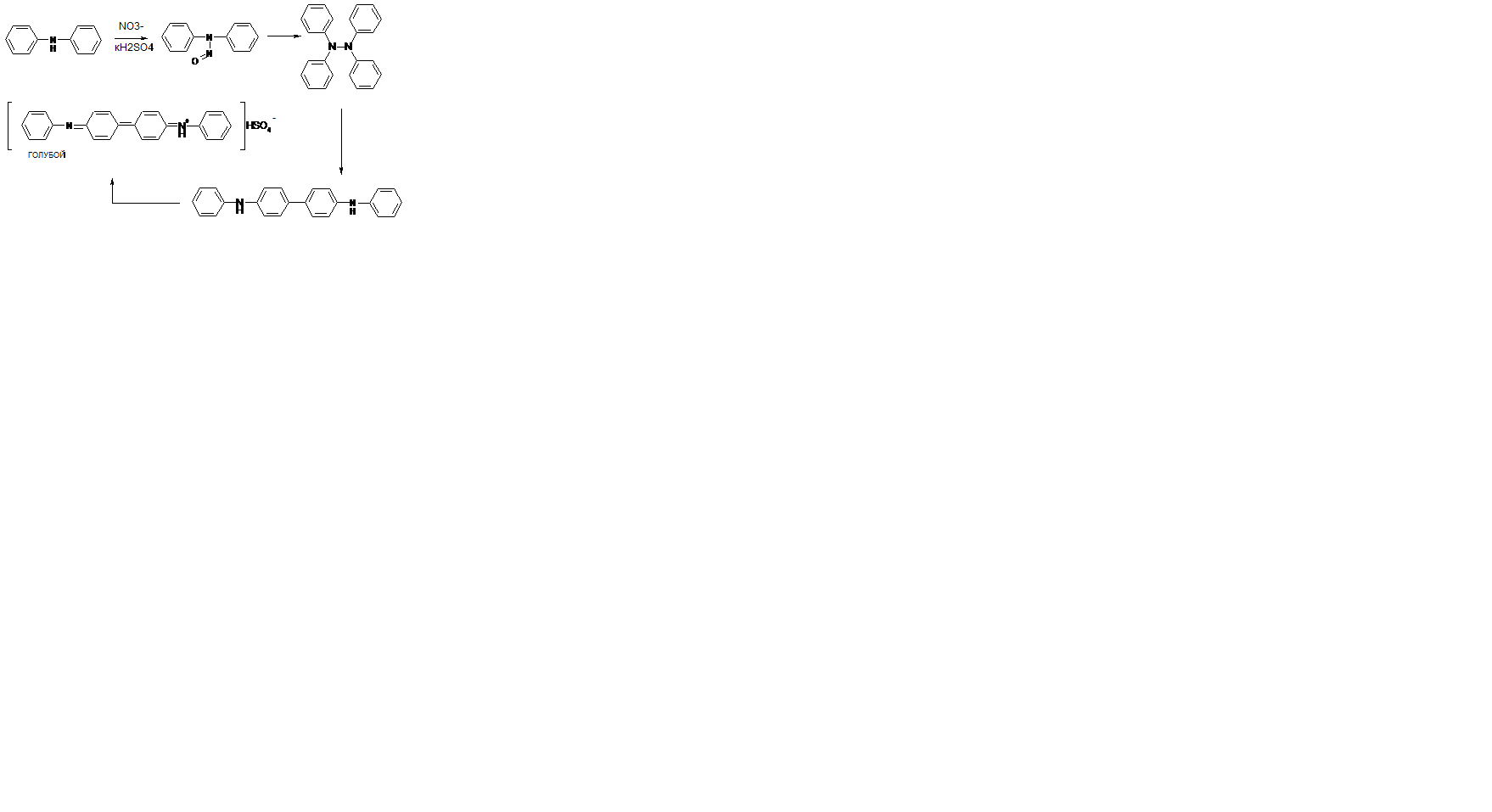
С антипирином в кислой среде:
Нитраты в присутствии концентрированной серной кислоты, нитриты в присутствии разбовленного раствора серной кислоты образуют окрашенные продукты:
Нитрит-ион:
NaNO2+HCl→HNO2+NaCl

Образуется нитрозоантипирин, наблюдают изумрудно-зеленое окрашивание. Реакция идет за счет замещения атома водорода в 4-ом положении на нитрозогруппу.
Нитрат-ион:
Образуется нитроантипирин, наблюдают красное окрашивание. Реакция идет за счет замещения атома водорода в 4-ом положении на нитрогруппу.
Частные реакции на нитрит-ион:
С разбавленной серной кислотой. ГФ.
2NaNO2+H2SO4→2HNO2+Na2SO4
HNO2→NO2↑+NO↑+H2O
2NO↑+O2→NO2↑
Нитрит-ион разлагается серной кислотой с выделением бурого газа оксида азота(IV). Реация идет на холоду.
Реакция образов азо-красителя. ГФ.
Нитрит-ион с первичными ароматическими аминами в среде хлороводородной кислоты образует соль диазония, которая с соединениями фенольной природы вступает в реакцию азосочетания с образованием азокрасителя.
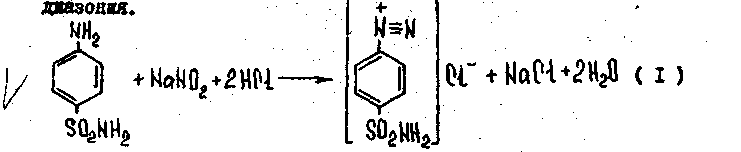
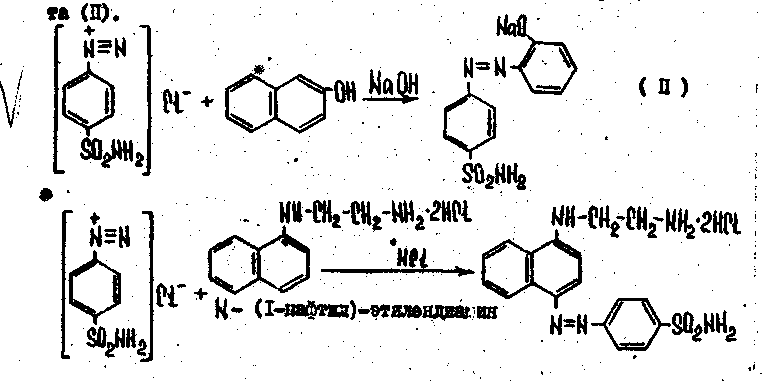
Образуется вишнево-красное окрашивание или красно-оранжевый осадок.
С реактивом Грисса (с сульфаниловой кислотой и-ɑ-нафтиламином)-позволяет определять «следы» нитритов.
Образуется красное окрашивание, при большой концентрации нитритов-красный осадок.
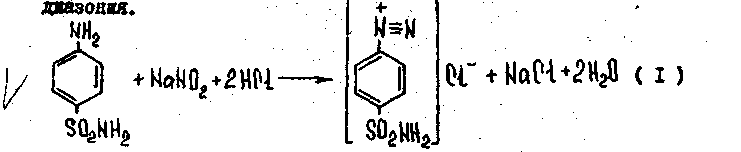
С калия йодидом:
2NaNO2+2KI+4HCl→I2+2NaCl+2KCl+2NO↑+2H2O
2I--2e-→I20 |1
NO2-+2H++1e-→NO0↑+H2O|2
2I-+NO2-+2H+→I20+NO0↑+H2O
Реакция проводятся в кислой среде, в присутствии хлороформа. Хлороформный слой окрашивается в фиолетовый цвет. Реакцию можно также проводить в присутствии крахмала появляется синее окрашивание. ГФ.
С перманганатом калия: реакция основана на окислении нитрит-иона до нитрат-иона.
5NaNO2+2KMnO4+3H2SO4→5NaNO3+2MnSO4+K2SO4+3H2O
NO2-+H2O-2e-→NO3-+2H+ |5MnO4-+8H++5e-→Mn2++4H2O|2 5NO2-+5H2O+2MnO4-+16H+→5NO3-+10H++2Mn2++8H2O5NO2-+2MnO4-+6H+→5NO3-+2Mn2++3H2O
Обесцвечивание раствора перманганата калия. Реакцию проводят при нагревании.
Ацетат-ион:
Сконцентрированной серной кислотой. ГФ.
2CH3COONa+H2SO4→Na2SO4+2CH3COOH
Концентрированная серная кислота вытесняет уксусную кислоту из ее солей. Ощущается запах уксусной кислоты, усиливающийся при нагревании.
С хлоридом железа(III). ГФ.
2CH3COONa+FeCl3→3NaCl+Fe(CH3COO)3
В нейтральной среде образуется красно-бурое окрашивание(цвет крепкого чая).При разбавлении водой и нагревании происходит гидролиз ацетата железа (III) и выпадает красно-бурый осадок основной соли железа (III).
Fe(CH3COO)3+2HOH→Fe(OH)2(CH3COO)↓+2CH3COOH или
3Fe(CH3COO)3+2HOH→[Fe3(CH3COOH)6(OH)2]CH3COO+2CH3COOH
С этиловым спиртом:
CH3COOH+C2H5OH→H2SO4CH3COOC2H5
Образуется уксусно-этиловый эфир с характерным запахом.
|
из
5.00
|
Обсуждение в статье: Частные реакции на анионы III аналитической группы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

