 |
Главная |
Комплексные соединения
|
из
5.00
|
Примеры решений задач
Пример 1. Вычислите заряды комплексных ионов , образованных платиной (IV): 1) [0,63]; 2) [  ]; 3) [
]; 3) [  ]. Назовите эти соединения.
]. Назовите эти соединения.
Решение.Степень окисления атома платины (комплексообразователя) равна +4, заряд молекулы аммиака (лиганда) равен нулю, а заряд хлорид-аниона (другого лиганда) равен -1; в итоге в соединении 1) - пентахлорамминплатине (IV) ([  ]
]  ) - суммарный заряд составляет +4 + (-5) = -1.
) - суммарный заряд составляет +4 + (-5) = -1.
Аналогичным образом находим заряды других комплексов:
2) в тетрахлордиамминплатине (IV) ([  ]) +4 + (-4) = 0,
]) +4 + (-4) = 0,
3) в дихлортетраамминплатине (IV) ([  ]
]  ) +4 + (-2) = +2.
) +4 + (-2) = +2.
В первом случае внешняя сфера содержит катионы, во втором – соединение является неэлектролитом, а в третьем – внешнюю сферу содержит анионы.
Пример 2. В результате приливания раствора  к раствору тиосульфата калия
к раствору тиосульфата калия 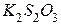 образуется комплексная соль
образуется комплексная соль  . Составьте уравнение реакции и укажите причину её протекания.
. Составьте уравнение реакции и укажите причину её протекания.
Решение:Учтём, что прочность аммиачных комплексов значительно ниже, чем тиосульфатных: это видно из сравнения соответствующих констант нестойкости (см. табл. 3 Приложения). Реакция всегда протекает в направлении образования более прочного комплексного иона. В рассматриваемом случае уравнение реакции в молекулярной форме имеет следующий вид:
 ,
,
В полной ионно-молекулярной форме это уравнение записывается так:
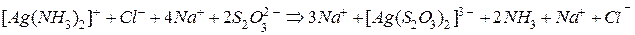 .
.
Принимая во внимание, что ионы  и
и  практически не изменяют своей концентрации в растворе, окончательно имеем:
практически не изменяют своей концентрации в растворе, окончательно имеем:
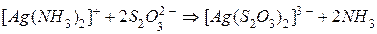 .
.
Пример 3. Константа нестойкости иона  составляет
составляет  . Вычислить концентрацию ионов серебра в 0,05 M растворе
. Вычислить концентрацию ионов серебра в 0,05 M растворе  , содержащем, кроме того, 0,01 моль/л
, содержащем, кроме того, 0,01 моль/л 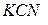 .
.
Решение.Вторичная диссоциациякомплексного иона протекает по уравнению:
 .
.
В присутствии избытка ионов  , создаваемого в результате диссоциации
, создаваемого в результате диссоциации 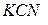 (которую можно считать полной), это равновесие смещено влево настолько, что количеством ионов
(которую можно считать полной), это равновесие смещено влево настолько, что количеством ионов  , образующихся при вторичной диссоциации, можно пренебречь. Тогда
, образующихся при вторичной диссоциации, можно пренебречь. Тогда  моль/л. По той же причине равновесная концентрация ионов
моль/л. По той же причине равновесная концентрация ионов  может быть приравнена к общей концентрации комплексной соли (0,05 моль/л).
может быть приравнена к общей концентрации комплексной соли (0,05 моль/л).
По условию задачи:
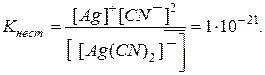
В итоге определим концентрацию ионов 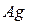 :
:

Пример 4. Растворы простых солей кадмия образуют с щелочами осадок гидроксида кадмия  , а с сероводородом – осадок сульфида кадмия CdS. Чем объяснить, что при добавлении щёлочи к 0,05 M раствору
, а с сероводородом – осадок сульфида кадмия CdS. Чем объяснить, что при добавлении щёлочи к 0,05 M раствору  , содержащему 0,1 моль/л KCN, осадок не образуется, тогда как при пропускании через этот раствор сероводорода выпадает осадок CdS ? Константу нестойкости иона
, содержащему 0,1 моль/л KCN, осадок не образуется, тогда как при пропускании через этот раствор сероводорода выпадает осадок CdS ? Константу нестойкости иона  принять равной
принять равной 
Решение.Из условий образования осадков  и CdS следует:
и CdS следует:
 ,
,
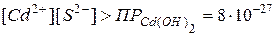 .
.
Учтём, что в растворе комплексной соли концентрацию ионов  можно аппроксимировать уравнением (см. пример 3):
можно аппроксимировать уравнением (см. пример 3):

Концентрация ионов  , достаточная для осаждения гидроксида кадмия, может быть определена из неравенства:
, достаточная для осаждения гидроксида кадмия, может быть определена из неравенства:
 .
.
Следовательно, в рассматриваемой системе при концентрациях ионов  меньших, чем 1
меньших, чем 1  , равновесие
, равновесие  смещено в сторону образования комплексного иона.
смещено в сторону образования комплексного иона.
Условие образования осадка сульфида кадмия из заданного раствора тетрацианокадмата калия отражает неравенство:

Таким образом, даже при малых концентрациях сульфид-иона равновесие 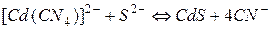 практически полностью смещено в сторону образования сульфида кадмия.
практически полностью смещено в сторону образования сульфида кадмия.
Контрольные задания
302. В чем заключается различие между комплексными и двойными солями с точки зрения ионной теории? Составьте уравнения диссоциации на ионы перечисленных ниже комплексных и двойных солей: Na3[Co(NO2)6]; [Cr(H2O)4Cl2]Cl; KCr(SO4)2; KMgCl3. Назовите комплексные соли, укажите валентность и координационное число их комплексообразователей. При добавлении к каким из указанных солей раствора щелочи выпадет осадок гидроксида металла?
303. Составьте уравнение реакции в молекулярной и ионной формах, которые соответствуют следующим схемам:
а) K2[HgCl4]  K2[HgI4];
K2[HgI4];
б) K[Ag(NO2)2]  [Ag(NH3)2]NO2.
[Ag(NH3)2]NO2.
Укажите, какие комплексные ионы в указанных схемах, исходные или конечные, характеризуются меньшими по величине константами нестойкости. Почему?
304. На комплексные соединения CoCl2·6NH3 и CoCl2·5NH3 подействовали раствором AgNO3. На полмоля одного соединения для осаждения хлора пошло полтора моля , а на полмоля второго – 1 моль AgNO3. Укажите координационные формулы этих соединений и определите заряды комплексных ионов.
305. Составьте молекулярное уравнение реакции, протекающей по схеме:
[Fe(CN)6]4- + MnO4- + 8 H+  [Fe(CN)6]3- + Mn2+ + 4H2O.
[Fe(CN)6]3- + Mn2+ + 4H2O.
Определите степени окисления комплексообразователей и напишите выражения констант нестойкости комплексных анионов.
306. Вычислите концентрацию катионов серебра в 0,1 Мрастворе соли [Ag(NH3)2]Cl. Назовите это соединение.
Ответ: 2,1·  моль/л.
моль/л.
307. Из сочетаний частиц Zn2+, NH3, CN- и Na+ можно составить 5 координационных формул комплексных соединений цинка. Укажите формулы данных соединений, если координационное число цинка равно четырем. Назовите эти соединения и запишите уравнения их диссоциации на ионы.
308. Рассмотрите следующую реакцию:
2[Co(H2O)6)]Cl2 + 2NH4Cl + 10 NH3 + H2O2 ® 2[Co(NH3)6]Cl3 + 14 H2O,
катализатором которой является древесный уголь. Какую степень окисления имеет атом кобальта в комплексных соединениях [Co(H2O)6)]Cl2 и [Co(NH3)6]Cl3 ? Какую роль играет пероксид водорода? В отсутствии катализатора продукты включают Co(NH3)5Cl3 и Co(NH3)5(H2O)Cl3; определите, какие комплексные ионы содержатся в этих соединениях.
309. Составьте уравнения диссоциации на ионы комплексных солей:
Cr(NH3)5Сl3; Cr(NH3)4(H2O)Cl3; Co(NH3)5(NO2)3; KСo(NH3)2(NO2)4,
заключив формулы комплексных ионов в квадратные скобки и имея в виду, что координационное число как хрома, так и кобальта равно шести.
310. Вычислите концентрацию ионов Cu2+ в растворе, полученном в результате реакции [Cu(NH3)2]2+ + 2 NH3  [Cu(NH3)4]2+ при добавлении 0,1 моля [Cu(NH3)2]2+ к 1,0 молю NH3 с последующим разбавлением этой смеси водой до объема в 1 л.
[Cu(NH3)4]2+ при добавлении 0,1 моля [Cu(NH3)2]2+ к 1,0 молю NH3 с последующим разбавлением этой смеси водой до объема в 1 л.
Ответ: 5,13·  моль/л.
моль/л.
311. Укажите возможные продукты следующих реакций, уравненных в левой части приведенных схем:
а) [Cr(H2O)6]Cl3 + 6KNСS 
б) [Ni(H2O)6]2+ + 2C2O42- 
в) Zn(CN)2 + 2KCN 
г) [Fe(H2O)6] 2+ + 2NH3 
д) [Fe(H2O)5(OH)] 2+ + НNO3 
312. Выпадет ли осадок Co(OH)3 , если к 0,1 н. раствору [Co(NH3)6]Cl3 прилить равный объем 2,0 М раствора NaOH? Кнест =6,2×10-36, произведение растворимости [Co(OH)3 ] = 4×10-32.
313. Укажите координационное число и степень окисления центрального атома металла в каждом из следующих координационных соединений : а) K2[FeCl4]; б) K3[FeCl6]; в) Na3[Cr(C2O4)3]; г) [Pt(NH3)4Cl2]Cl2; д) [Cr(H2O)5Cl]Cl2. Напишите соответствующие им выражения констант нестойкости комплексных ионов.
314. Укажите названия соединений, определите степень окисления комплексообразователя: а) [Cr(NH3)6]Cl3; б) [Cu(NH3)4]SO4; в) K4[Fe(CN)6]; г) Na2[Be(OH)4];
д) [Co(NH3)3Cl3]; е) K[Pt(NH3)Cl3]. Составьте уравнения электролитической диссоциации перечисленных веществ и запишите соответствующие им выражения констант нестойкости комплексных ионов.
315. Напишите формулы комплексных соединений по указанным названиям: а) гидроксид тетрааммин меди (II), б) хлорид хлородиаммин цинка (II), в) бромид бис (этилендиамин) никеля (II), г) трис (этилендиамин) кобальта (III). Составьте уравнение реакции между растворами KNO2 и Pt(NO2)2 в молекулярной и ионно-молекулярной формах. Назовите образуемое комплексное соединение.
316. Пользуясь таблицей констант нестойкости (см. табл.3 Приложений), определите, в каких случаях произойдет взаимодействие между растворами электролитов. Укажите для этих случаев молекулярные и ионные формы уравнений:
а) K2[HgBr4] +KCN;
б) Na3[Ag(S2O3)2] + KCN;
в) [Cu(NH3)4](NO3)2 +KCN;
г) K[Ag(NO2)2] + NH4OH;
д) [Ni(NH3)4]Cl2 + NaCN.
317. Приведите схемы диссоциации и выражения констант нестойкости следующих комплексных ионов: а) [Fe(CN)6]3-; б) [Fe(CN)6]4-; в) [Ag(NH3)2]+; г) [Ag(NH3)(H2O)]+;
д) [Cr(H2O)6]3+. Определите степени окисления указанных комплексообразователей.
318.Эмпирическая формула соли CrCl3×5 H2O. Исходя из того, что координационное число хрома равно шести, определите, какой объем 1 н. раствора AgNO3 понадобится для осаждения внешнесферно связанного хлора, содержащегося в 300мл 0,1 М раствора комплексной соли. При вычислениях считать, что вся вода, входящая в состав соли, связана внутрисферно.
Ответ: 60 мл.
319. При взаимодействии раствора [Cu(NH3)4]Cl2 c раствором KCN образуется соль K2[Cu(CN)4]. Составьте уравнение реакции и объясните причину её протекания.
320. Определите величину и знак заряда перечисленных ниже комплексных ионов:
[Cr(H2O)4Cl2]; [Pt(NH3)3Cl3]; [Ag(CN)2]; [Co(NO2)6]; [Cr(NH3)5Cl]; [PtCl6],
имея в виду, что комплексообразователями являются катионы Cr,3+Pt,4+ Ag+, Co3+. Приведите названия комплексных соединений.
321. Бромид кобальта образует с аммиаком следующие соединения:
CoBr3×6NH3; CoBr3×5NH3×H2O; CoBr3×5NH3; CoBr3×4NH3.
Действие раствора AgNO3 приводит к практически полному осаждению всего брома из первых двух соединений, около 2/3 брома из третьего соединения и около 1/3 брома из четвертого. Определите координационное число атома кобальта. Изобразите строение указанных комплексных соединений и составьте уравнения реакций их с нитратом серебра в молекулярной и ионной формах.
|
из
5.00
|
Обсуждение в статье: Комплексные соединения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

