 |
Главная |
Лекция 11. Тождественные частицы в классической и квантовой физике. Классическая и квантовая статистики
|
из
5.00
|
1. Соотношения неопределенности Гайзенберга
DхDр³h, где Dх - точность определения координаты микрочастицы, Dр- точность определения импульса микрочастицы.
2. Классические и квантовые тождественные частицы
| Классическое описание | Квантовое описание |
| Законы динамики mdv/dt=F dL/dt= rxF Еи р принимают лю- бые значения.Если задать исходные данные координат и скоростей частиц или тел, то можно рассчитать их траекторию с наперед заданной точностью. В классической физике одинаковые частицы различаются, хотя бы своими координатами. | Уравнение Шредингера y=ynlms . E,p,L,L2 - квантуются, т.е принимают строго определенные значения. Отсутствует понятие траектории отдельной частицы. y2 характеризует вероятность обнаружения частицы в той или иной области пространства. Реальные физические величины - статистические средние по большому ансамблю частиц. Квантовые частицы тождественны - принципиально неразличимы. Поскольку волновые пакеты, описывающие частицы могут перекрываться, то в одной и той же точке пространства возможно с какой-то вероятностью пребывание одновременно нескольких частиц. |
Физические величины, характеризующие элементарные частицы, атомы и молекулы (размеры, масса, импульс, энергия и т.д.) настолько малы, что в любом макроэксперименте мы сталкиваемся с системами, состоящими из огромного числа отдельных частиц. Результаты измерений в таком эксперименте оказываются статистически средними по большому числу частиц. Понятие статистического распределения вводят для описания событий, носящих чисто случайный характер. Вероятность появления значения величины х, лежащего в интервале от х до х+dx для системы N частиц можно представить dW= dN/N=f(x)dx. Здесь dN – число частиц, имеющих значение х в интервале от х до х+dx, f(x) – функция распределения. Вероятность того, что значение величины х заключено в интервале от 0 до ∞ равно 1, то есть W =  Тогда среднее значение величины g(x) определится следующим образом <g(x)>=
Тогда среднее значение величины g(x) определится следующим образом <g(x)>=  , например, <x>=
, например, <x>=  , <x2>=
, <x2>= 
3.Квантовые статистики
- Если при перестановке пары квантовых частиц в системе большого числа частиц описывающая их волновая функция не меняется, т.е. симметрична по отношению к операции перестановки двух частиц, то такие частицы называются бозонами, а система бозе-частиц описывается статистикой Бозе. Пример - газ фотонов - квантов электромагнитной энергии.
Функция распределения по энергиям Е для бозонов имеет вид:
 , где m - химический потенциал.
, где m - химический потенциал.
- Если при перестановке пары частиц местами волновая функция меняет знак, т.е. оказывается несимметричной, то система таких тождественных частиц называется фермионами. Фермионы описываются статистикой Ферми-Дирака. Пример - газ электронов проводимости в металлах.
Функция распределения для фермионов по энергиям Е имеет вид:
 |

 f(E) kT
f(E) kT


 1
1


 T=0 T¹0 f(E)=
T=0 T¹0 f(E)= 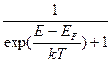 ,
,
 0 E
0 E
EF
где ЕF – энергия Ферми – максимальная энергия электронов проводимости при абсолютном нуле температур. Физический смысл 1 на графике функции распределения в том, что в каждом квантовом состоянии с энергией Е может находится только один электрон с данным набором квантовых чисел.
4.Распределения Максвелла – Больцмана
В системе классических частиц – молекул идеального газа функция распределения f(v)=  =Dn/(nDv) молекул этого газа по скоростям называется распределением Максвелла.
=Dn/(nDv) молекул этого газа по скоростям называется распределением Максвелла.
D  n/(nDv)
n/(nDv)
 |

 v
v
vвер
Здесь vвер – наиболее вероятное значение скорости молекул идеального газа.
Средняя скорость молекул идеального газа <v>= 
Средний квадрат скорости <v2>=  . Поэтому среднее значение кинетической энергии молекулы идеального газа равно
. Поэтому среднее значение кинетической энергии молекулы идеального газа равно
<W>=< 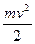 >=
>=  .
.
Классическое распределение Больцмана числа частиц в единице объема по высоте z находится из распределения Больцмана
f(z) =  . Здесь no – концентрация молекул газа вблизи поверхности Земли ( z = 0).
. Здесь no – концентрация молекул газа вблизи поверхности Земли ( z = 0).
Воспользуемся уравнением состояния идеального газа, из которого получим давление
 , тогда получим барометрическую формулу ( распределение давления газа в атмосфере с высотой:
, тогда получим барометрическую формулу ( распределение давления газа в атмосфере с высотой:
 . Здесь Ро – давление в атмосфере вблизи поверхности Земли.
. Здесь Ро – давление в атмосфере вблизи поверхности Земли.
Контрольные вопросы
1. Различие понятия тождественных частиц в классической
и квантовой физике.
2. Принцип неопределенности и его физический смысл.
3.Что такое корпускулярно-волновой дуализм?
4. Физический смысл распределений Максвелла и Больцмана.
Литература
1. И.В.Савельев Курс общей физики т.3,гл.2-9,2-10,4,7-52,
Наука,М.,1977г.
2. Б.М.Яворский, А.А.Пинский Основы физики т.2,гл.68-70, Наука, М.,1974г.
3. Дж.Орир Физика т.2 гл.24,25 Мир,м.,1981г.
Лекция 12. Три начала термодинамики. Фазовые состояния вещества. Фазовые переходы. Жидкие кристаллы
Понятие о статистическом и термодинамическом методах
В основе статистического метода лежит метод Гиббса. Он возник как последовательное обобщение работ Клаузиуса, Максвелла и Больцмана по атомно-молекулярной теории тепла. Работы Гиббса печатались в малоизвестных американских журналах. Лишь позднее теории Гиббса воздали должное.
Истоки атомно-молекулярной теории восходят к первым попыткам Бойля (1627-1691гг.) и Ньютона (1648-1727гг.) представить теплоту как молекулярное движение. Тогда еще не существовало количественной кинетической теории. В 1738 году Бернулли предложил первые наброски кинетической теории газов. М.В.Ломоносов в 1745-1747гг. более или менее последовательно развивал молекулярно-кинетическую теорию тепла. В частности, он предположил существование абсолютного нуля температур, обосновал превращение механического движения в тепловое. Однако, в то время атомистическая теория Ломоносова была отвергнута большинством приверженцев другого термодинамического подхода. Термодинамический метод - описательный метод. Он базируется на результатах эксперимента. Основные достижения термодинамики связаны с работами Карно (работа термодинамической системы за цикл), с построением классической термодинамики в 1850г. Клаузиусом и Томпсоном (лорд Кельвин). Развитие физики в значительной мере в 18 - 19 веках было сопряжено борьбой сторонников термодинамического и молекулярно-кинетического представлений. Особенно обострилась эта борьба на рубеже XIX и XX столетий между сторонниками термодинамического подхода (Оствальд, Мах) и молекулярно-кинетического направления (Клаузиус, Максвелл, Больцман). Для Больцмана эта борьба закончилась трагически. Его особенно донимали вопросы типа «А видел ли кто эти молекулы?» Он покончил жизнь самоубийством в 1906г. Больцман не знал, что еще в 1828 году английский ботаник Роберт Броун наблюдал, как под действием молекул движутся микроскопические частички. Сейчас броуновское движение пылинок в луче света наблюдает каждый из нас, и это служит лучшим подтверждением их существования. Истинность учения Больцмана была доказана поляком Смолуховским в работе по броуновскому движению. Современная физика включает в себя как составные части термодинамику и статистическую физику.
Законы термодинамики
Первый закон термодинамики отражает закон сохранения энергии
dQ=dU + dA. Количество тепла dQ, переданное телу, идет на увеличение его внутренней энергии dU и совершение работы dA.
Второй закон термодинамики
- Самопроизвольно идет процесс перехода системы из состояния с меньшей термодинамической вероятностью в состояние с большей термодинамической вероятностью.
- DS³0 Энтропия замкнутой системы не убывает. Поскольку энтропия характеризует степень хаотизации системы, то второе начало термодинамики говорит о том, что хаос в замкнутых системах должен только возрастать. Такой вывод привел Больцмана к представлению о тепловой смерти Вселенной.
- Невозможно прямое преобразование тепловой энергии в механическую без потерь.
Третий закон термодинамики свидетельствует о невозможности достижения абсолютного нуля температур.
|
из
5.00
|
Обсуждение в статье: Лекция 11. Тождественные частицы в классической и квантовой физике. Классическая и квантовая статистики |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

