 |
Главная |
Пример 3. Какое количество вещества оксида меди (II) содержится в 120 г его массы?
|
из
5.00
|
Решение. Используем формулу  ,
,
где n- количество вещества;
m- масса вещества;
М – молярная масса вещества, численно равна
относительной молекулярной массе
1. Относительная молекулярная масса Мr(СuО)=64+16=80, следовательно, молярная масса М (СuО)=80г/моль.
2. Пользуясь соотношением 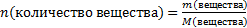
находим количество вещества: n(СuО)= 
Пример 4. Определите массу гидроксида натрия количеством вещества 2 моль.
Решение. Используем формулу  ,
,
1. Молярная масса М(NаOH)= 23+16+1=40г/моль.
2. m=nM
3. m(NаOH)= 2  40г/моль=80г.
40г/моль=80г.
Пример 5. Какой объем занимает 4 моль углекислого газа СО2.
Решение. Используем формулу  ,
,
где Vm=22,4 л/моль
1. V(СО2)=n(CO2)  Vm= 4
Vm= 4  22,4л/моль= 89,6л.
22,4л/моль= 89,6л.
Пример 6. Вычислите массу осадка, полученного действием раствора, содержащего 8г гидроксида натрия с раствором сульфата меди(II).
| Последовательность действий | Пример выполнения действий |
| 1.Запишите условие и требование задачи с помощью общепринятых обозначений | Дано: m(NаOH)=8г Найти: m(Cu(OH)2)-? |
| 2.Составьте уравнение химической реакции | Решение: CuSO4+2 NаOH→ Cu(OH)2+Na2SO4 |
| 3.В уравнении подчеркните формулы веществ, которые записаны в «Дано» и «Найти» | CuSO4+2 NаOH→ Cu(OH)2+Na2SO4 |
| 4. Под подчеркнутыми формулами подписать по коэффициентам «моли» | CuSO4+2 NаOH→ Cu(OH)2+Na2SO4 2 моль 1 моль |
| 5. Вычислите количество вещества n, которое записано в «Дано» |  n(NаOH) =
n(NаOH) = 
|
| 6. Подпишите найденное n под формулой этого вещества | CuSO4+2 NаOH→ Cu(OH)2+Na2SO4 2 моль 1 моль 0,2 моль |
| 7. Под формулой вещества, массу которого надо найти, поставим х моль | CuSO4+2 NаOH→ Cu(OH)2+Na2SO4 2 моль 1 моль 0,2 моль х моль |
| 8. Из полученной пропорции выразить х | 2 моль 1 моль
0,2 моль х моль
х =  –
это количество вещества n( Cu(OH)2) –
это количество вещества n( Cu(OH)2)
|
| 9. Зная n( Cu(OH)2) найдите массу Cu(OH)2 | m=nM
m(Cu(OH)2)= n Cu(OH)2  M Cu(OH)2
M Cu(OH)2 =64+(16+1) M Cu(OH)2
M Cu(OH)2 =64+(16+1)  2=98г/моль
m(Cu(OH)2)=0,1 2=98г/моль
m(Cu(OH)2)=0,1  98г/моль=9,8г 98г/моль=9,8г
|
| 10. Запишите ответ | Ответ: m(Cu(OH)2)=9,8г |
Контрольные задания
Подготовьте сообщения
1. Аллотропные модификации углерода (алмаз, графит), кислорода (кислород, озон), олова (серое и белое олово). (Указание: в сообщении написать о физических свойствах указанных модификаций и применении, можно оформить в виде таблицы).
2. Понятие о химической технологии, биотехнологии и нанотехнологии. (Указание: в сообщении отразить их определение и привести конкретные примеры применения.)
Решите задачи
ВНИМАНИЕ! Условие задач необходимо списывать.
Задача 1. Вычислите относительную молекулярную массу.
| 1. Азотной кислоты 2. Оксида алюминия 3. Гидроксида железа (III) 4. Сульфата бария 5. Гидроксида алюминия 6. Угольной кислоты 7. Соляной кислоты 8. Карбоната натрия 9. Оксида калия 10. Хлорида железа (II) 11. Фосфорной кислоты 12. Сульфата натрия 13. Оксида серы (IV) 14. Нитрата бария 15. Сульфата меди (II) 16. Аммиака 17. Карбоната кальция | 18. Оксида фосфора (V) 19. Гидроксида кальция 20. Оксида серебра 21. Нитрата магния 22. Гидроксида магния 23. Карбоната бария 24. Сульфата калия 25. Оксида меди (II) 26. Нитрата натрия 27. Хлорида цинка 28. Нитрата серебра 29. Оксида магния 30. Фосфата алюминия 31. Сульфида натрия 32. Гидроксида цинка 33. Хлорида железа (III) 34. Хлорида бария |
Чему равна молярная масса вещества из вашего варианта?
Задача 2.Расчитайте массовую долю (%) для первого элемента в веществе ….
| 1. СО2 2. Н2S 3. NH3 4. Н3РО4 5. СН4 6. Н2О 7. Na2SO4 8. Na2S 9. HNO3 10. HBr 11. С2Н4 12. СаF2 13. К2СО3 14. SO2 15. Ag2O 16. NO2 17. C2H6 | 18. HF 19. Nа3РО4 20. Н2СО3 21. CuO 22. Ag2O 23. Ва(ОН)2 24. СаО 25. N2O5 26. ZnO 27. K2SO3 28. CO 29. Fe2O3 30. HCl 31. Al2O3 32. H2SiO3 33. K2О 34. KOH |
Задача 3.
1. Рассчитайте, какое количество(n) углекислого газа получится при сгорании 6г угля С.
2. Юный радиотехник при травлении омедненной платы опустил ее в раствор хлорида железа (III).Какая масса меди перейдет в раствор, если в результате реакции, идущей согласно уравнению 2FeCl3 + Сu = 2FeCl2 + СuСl2, выделилось 1,35г хлорида меди(II).
3. Какова масса нитрата меди, образующегося при взаимодействии оксида меди(II) массой 4г с азотной кислотой?
4. Какое количество вещества (n) воды можно получить, если сжечь 3 моль газа водорода.
5. Какой объем кислорода (н.у.) потребуется для сжигания 2,4г магния?
6. Сколько литров водорода (н.у.)можно получить при действии избытка разбавленной серной кислоты на цинк массой 24г?
7. Сколько граммов гидроксида калия потребуется для взаимодействия с 70г серной кислоты?
8. Сколько граммов водорода можно получить при взаимодействии алюминия массой 54г с соляной кислотой?
9. 4,6г натрия растворили в воде с образованием щелочи и газа. Вычислите объем газа (н.у).
10. Какова масса соли, получившейся при взаимодействии оксида кальция массой 28 г с соляной кислотой?
11. Сколько литров оксида углерода (IV) (н.у.) можно получить при прокаливании известняка СаСО3, массой 200г?
12. Какая масса алюминия подверглась окислению кислородом, если образовалось 10,2г оксида алюминия.
13. При растворении цинка в соляной кислоте выделился газ объемом 6,72л. Вычислите массу растворившегося цинка.
14. Сколько литров водорода (н.у.) выделится при разложении электрическим током воды массой 72 г?
15. Сколько граммов серной кислоты прореагирует с цинком, если получается 4 моль сульфата цинка?
16. Сколько литров водорода (н.у.) сгорело, если образовалось 72 г воды?
17. Какое количество вещества водорода выделится при взаимодействии магния с соляной кислотой массой 146 г?
18. Сколько граммов сульфата цинка можно получить, имея 0,5 моль серной кислоты взаимодействующей с цинком?
19. Какой объем водорода в литрах выделится (н.у.) если с соляной кислотой прореагировало 3 моль магния?
20. Получают 3г ртути путем разложения оксида ртути НgО. Сколько граммов исходного вещества потребуется для этого?
21. Сколько потребуется карбоната кальция (мрамора) при взаимодействии с соляной кислотой для получения 5,6 л углекислого газа (н.у.)
22. Сколько молей кислорода необходимо для полного окисления 0,4 моль магния?
23. Сколько грамм гидроксида натрия потребуется для взаимодействия с 9,8г серной кислоты.
24. Хлорид магния реагирует с 10,6г карбоната натрия. Найти массу образовавшегося осадка.
25. Какой объем кислорода (н.у.) нужен для сжигания серы массой 6,4 г до SО2.
26. Какая масса гидроксида натрия потребуется для превращения сульфата меди (II) массой 16 г в гидроксид меди (II)?
27. Гидроксид алюминия массой 7,8 г растворили в соляной кислоте. Какая масса соли при этом образовалась?
28. Сколько грамм воды образуется при нейтрализации 8 г гидроксида натрия азотной кислотой?
29. Вычислите массу осадка, полученного действием раствора, содержащего 9,8г серной кислоты с раствором хлорида бария.
30. Определите объем водорода, вступающего в реакцию с 44,8 л кислорода для образования воды. Объемы газов измерены при н.у.
31. Хлорид натрия реагирует с 17 г нитрата серебра. Найти массу образовавшегося осадка.
32. Для получения меди из оксида меди (II) израсходован водород объемом 1,12 л (н.у.).Сколько меди в граммах при этом выделилось?
33. Какой объем кислорода (н.у.) израсходуется на сжигание 12 г магния?
34. Для нейтрализации серной кислоты потребовалось 5,6 г гидроксида калия. Вычислите массу образовавшейся при этом соли.
|
из
5.00
|
Обсуждение в статье: Пример 3. Какое количество вещества оксида меди (II) содержится в 120 г его массы? |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

