 |
Главная |
Ме – простые вещества являются восстановителями
|
из
5.00
|
54.Чем меньше величина  о, тем сильнее выражены свойства окислителя
о, тем сильнее выражены свойства окислителя
55. ЭДС рассчитывают по формуле ЭДС=φ катода — φ анода( ЭДС=φ окислителя — φ восстановителя); ЭДС > 0, то реакция возможна
Установите соответствие:
Окислительно-восстановительная реакция Тип
 1) 2KNO3 2KNO2 + O2 a) сопропорционирования
1) 2KNO3 2KNO2 + O2 a) сопропорционирования
 2) 2NO2 + H2O HNO3 + HNO2 б) внутримолекулярная
2) 2NO2 + H2O HNO3 + HNO2 б) внутримолекулярная
 3) 4NH3 + 5O2 4NO + 6H2O в) диспропорционирования
3) 4NH3 + 5O2 4NO + 6H2O в) диспропорционирования
 4) 2Na2S + Na2SO3 + 3H2SO4 3S + 3Na2SO4 + 3H2O г) межмолекулярная
4) 2Na2S + Na2SO3 + 3H2SO4 3S + 3Na2SO4 + 3H2O г) межмолекулярная
Б 2-в 3- г 4- а
Выберите правильный вариант:
57.В кислой среде (С.О.) марганца в KMnO4 изменяется до:
1) Mn0 3) Mn+4
2) Mn+2 4) Mn+6
58.Вещество проявляет только окислительные свойства:
1) Сr2(SO4)3 3) СrSO4
2) Сr0 4) K2Сr2O7
59.Окислительно-восстановительную двойственность проявляет:
1) H2SO4 3) Na2SO4
2) Na2SO3 4) H2S
Дополните:
60.Анод – электрод, на котором протекает процесс окисления
61.На границе Металл – раствор возникает электростатическое притяжение прилегающий слой жидкости заряжается положительно
62.Полуэлементом называют электрод, погруженный в подходящий электролит, разработанный для измерения электродного потенциала.
63.Стандартный (нормальный) электродный потенциал металла – это это потенциал металла, определенный относительно стандартного (нормального) водородного электрода, при условии, что концентрация ионов водорода Н+ и ионов испытуемого металла Men+ равны 1 моль-ион/л при стандартных условиях (298К, 101кП)
64.В цинковом полуэлементе – условно-графическая схема, которого
Zn2+ | Zn0 (2+ и 0 это заряды, наверху пишите)
процесс возникновения электродного потенциала отражает x уравнение Zn-2e = Zn 2+ (2+ это заряд напишите сверху)
65.Если возрастает концентрация ионов металла в растворе, то электродный потенциал уменьшается
66.Уравнение Нернста при Т = 298 К имеет вид ….
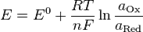
67.j катода больше j анода.
Установите соответствие:
68.В Г.Э.: Sn | SnSO4 | | NiSO4 | Ni
| Электроды 1. Катод в) – а) Sn 2. Анод г) + б) Ni | Металлы и заряды д) 0 лишнее |
68. В Г. Э.: Сu | CuCl2 | | ZnCl2| Zn
| ЭДС (н.у.) равно: 1. 0,42 В 2. 1,1 В | 3.– 1,1 В 4.– 0,42 В |
Выберите правильный вариант:
69. Если в гальвоническом элементе Анод – железный электрод, тогда Катод в Г.Э.:
| 1.Zn 2.Mg | 3.Sn 4.Cr |
Составьте условно- графическую схему.
Sn | SnCl2 | | FeCl2| Fe
70.pH =5, j p H2/н+ равно:
| 1. 0,155 В 2. 0,295 В | 3. -0,295 В 4. 0,130 В |
Ответ 3
Дополните:
71.Электрохимическая коррозия – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
72.На анодных участках протекает процесс называемый окислением а с электронной точки зрения – это процесс отдачи электронов
73.Деполяризаторы – вещества, которые служат для поглощения водорода, выделяющегося на положительном электроде гальванического элемента к ним относятся: 1) Деполяризаторы первого типа
2) Деполяризаторы второго типа
74. В кислой среде на катоде протекают два процесса – химизм:
1) а) в нейтральных или щелочных средах -
2Н2О + О2+ 4е- = 4ОН-
2) в кислых средах -
О20+ 4Н+ = 2Н2О
75.Электрохимическая коррозия возможна, если электродный потенциал анодного процесса меньше электродного потенциала катода
Установите соответствие:
76. Виды коррозии: Примеры:
| 1) по природе окружающей среды: 2) по механизму процесса; 3) по характеру разрушения металла | а) физическая; б) атмосферная; в) химическая; г) местная; д) равномерная; е) электрохимическая; ж) межкристаллитная; з) почвенная и) биологическая; к) жидкостная. 1-а, б, з, и, к 2-в, е 3-д, г ж |
|
из
5.00
|
Обсуждение в статье: Ме – простые вещества являются восстановителями |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

