 |
Главная |
Потенциал межмолекулярного взаимодействия
|
из
5.00
|
Взаимодействие молекул удобно характеризовать зависимостями силы f(r) и потенциальной энергией взаимодействия U(r), как функциями расстояния r между центрами сблизившихся молекул, приведенными на рис. (2-2.1 и 2-2.2).
При построении этих кривых сила взаимодействия и потенциальная энергия молекул, находящихся на бесконечно большом расстоянии друг от друга, положены равными нулю. На расстояниях r>r0(рис. 2-2.1) между молекулами действуют силы взаимного притяжения (отрицательный знак силы), а при r<r0 силы отталкивания (положительный знак силы).
Из рис. 2-2.1 видно, что по абсолютному значению сила притяжения растет с увеличением r вплоть до некоторого значения r1. Затем сила уменьшается и при расстоянии r0 между атомами становится равной нулю. При дальнейшем уменьшении r сила вновь появляется, но уже сила отталкивания, быстро растущая с уменьшением расстояния между молекулами, стремясь к бесконечности при  .
.
Кривой f(r) соответствует похожая на нее кривая U(r) (рис. 2-2.2). Сходство кривых не должно удивлять, так как f и Uсвязаны, как известно, соотношением  .
.
При расстоянии между атомами r0, когда сила взаимодействия равна нулю, потенциальная энергия проходит через минимум. О молекуле в таком положении принято говорить, что он находится на дне “потенциальной ямы”. Это положение равновесия, т. е. силы притяжения уравновешиваются силами отталкивания.
Какой-либо универсальной формулы U(r), пригодной для всех молекул, не существует. Более точно характеристика U(r) может быть дана лишь конкретно для данных молекул. Во многих вопросах теории к хорошим результатам приводит следующая аппроксимация функции U(r):
 , (2-2.1)
, (2-2.1)
в которой постоянные  подбираются из требований наилучшей аппроксимации реального потенциала. Как показало исследование потенциалов, в большинстве случаев хорошим приближением являются n=12, m=6 при
подбираются из требований наилучшей аппроксимации реального потенциала. Как показало исследование потенциалов, в большинстве случаев хорошим приближением являются n=12, m=6 при 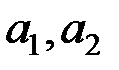 , уточняемых для конкретных атомов. Функция U(r), описываемая уравнением (2-2.1), называется потенциалом Леннарда–Джонса, широко используется в теории жидкостей и газов. Первый член (2-2.1) соответствует силам отталкивания, второй – силам притяжения, которые называются силами Ван-дер-Ваальса.
, уточняемых для конкретных атомов. Функция U(r), описываемая уравнением (2-2.1), называется потенциалом Леннарда–Джонса, широко используется в теории жидкостей и газов. Первый член (2-2.1) соответствует силам отталкивания, второй – силам притяжения, которые называются силами Ван-дер-Ваальса.
В теории уравнения состояния Ван-дер-Ваальса применяется более грубая аппроксимация. Крутой участок кривой U(r) заменяется вертикальной прямой, как это изображено на рис. 2-2.2 пунктиром. Если d – расстояние этой прямой от начала координат, то центры взаимодействующих частиц не могут сблизиться на расстояние, меньше d. Расстояние d играет роль диаметра молекулы, который относится к числу не вполне четко определяемых величин.
Рассматриваемая аппроксимация соответствует модели твердых упругих шаров, между которыми действуют силы притяжения; силы отталкивания учитываются тем, что размеры шаров считаются конечными.
|
из
5.00
|
Обсуждение в статье: Потенциал межмолекулярного взаимодействия |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

