 |
Главная |
Уравнение Клапейрона-Менделеева
|
из
5.00
|
Из перечисленных опытных законов следует, что состояние идеального газа описывается уравнением
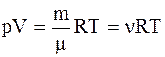 ,
,
где p, V, T - давление, объем и температура газа соответственно, m - масса газа, µ - молярная масса газа,  - универсальная газовая постоянная,
- универсальная газовая постоянная,  - количество вещества.
- количество вещества.
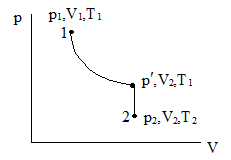 Чтобы получить уравнение Клапейрона-Менделеева, рассмотрим процесс перехода газа из состояния 1 в состояние 2. В первом состоянии газ имеет параметры p1,V1,T1, во втором - p2,V2,T2. Предположим, что переход из состояния 1 в состояние 2 происходит путем совершения изотермического и изохорного процессов так, как показано на рис.. Тогда промежуточное состояние будет характеризоваться параметрами p¢,V2,T1. Применив законы Бойля-Мариотта и Шарля, получим
Чтобы получить уравнение Клапейрона-Менделеева, рассмотрим процесс перехода газа из состояния 1 в состояние 2. В первом состоянии газ имеет параметры p1,V1,T1, во втором - p2,V2,T2. Предположим, что переход из состояния 1 в состояние 2 происходит путем совершения изотермического и изохорного процессов так, как показано на рис.. Тогда промежуточное состояние будет характеризоваться параметрами p¢,V2,T1. Применив законы Бойля-Мариотта и Шарля, получим
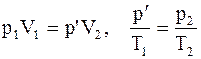 ,
,
откуда следует, что 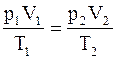 .
.
 Так как состояния 1 и 2 взяты произвольно, то для любого состояния будет
Так как состояния 1 и 2 взяты произвольно, то для любого состояния будет
 .
.
Значение константы для каждого газа будет своим. Но если рассматривать 1 моль газа, то из закона Авогадро следует, что для любого газа
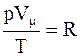
где Vm - объем одного моля. Так как V = nVm, то получаем уравнение Клапейрона-Менделеева.
Существует другая форма этого уравнения
 ,
,
где n - концентрация молекул, 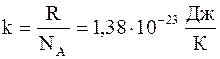 - постоянная Больцмана.
- постоянная Больцмана.
Основное уравнение молекулярно-кинетической теории  идеальных газов.
идеальных газов.
Газ, заключенный в сосуд, оказывает давление на его стенки. Это давление - результат столкновений молекул со стенками. При каждом столкновении изменяется импульс молекулы, следовательно, на нее со стороны стенки действует сила. По третьему закону Ньютона на стенку со стороны молекулы действует такая же, но противоположно направленная сила. Статистически усредняя эту силу по времени и по всем молекулам , можно получить уравнение, связывающее давление газа со средней кинетической энергией поступательного движения его молекул. Вывод этого уравнения проводится в предположении, что газ не находится во внешнем силовом поле. Следовательно, давление на все стенки сосуда одинаково. Кроме того, учитываются столкновения только со стенками сосуда. Влиянием столкновений молекул между собой, как показал Д. К. Максвелл, можно пренебречь.
Основное уравнение молекулярно-кинетической теории газов имеет вид
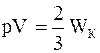 ,
,
где 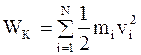 - суммарная кинетическая энергия поступательного движения всех N молекул газа,
- суммарная кинетическая энергия поступательного движения всех N молекул газа, 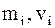 - масса и скорость i-ой молекулы.
- масса и скорость i-ой молекулы.
Средняя кинетическая энергия поступательного движения молекул найдется как
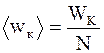 .
.
Из основного уравнения и уравнения Клапейрона-Менделеева следует, что
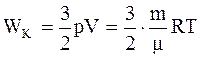 .
.
Тогда
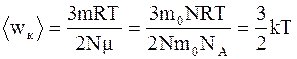 ,
,
где m0- масса одной молекулы. Таким образом, средняя кинетическая энергия поступательного движения молекул газа прямо пропорциональна его термодинамической температуре. Из этого выражения следует, что при 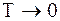
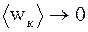 . Однако, в области сверхнизких температур неприменимы выводы классической физики. Там действуют законы квантовой статистики. Поэтому данное соотношение верно только при температурах далеких от 0 К.
. Однако, в области сверхнизких температур неприменимы выводы классической физики. Там действуют законы квантовой статистики. Поэтому данное соотношение верно только при температурах далеких от 0 К.
Скорости различных молекул газа различны. Для характеристики средней быстроты движения молекул вводится понятие средней квадратичной скорости, определяемой как
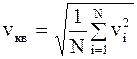 .
.
Для среднеквадратичной скорости можно получить выражения
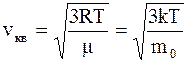 .
.
Например, молекулы водорода H2 при Т = 300 К в соответствии с этими выражениями имеют среднюю квадратичную скорость порядка 2•103 м/с.
|
из
5.00
|
Обсуждение в статье: Уравнение Клапейрона-Менделеева |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

