 |
Главная |
Тема 11. Ультрамикрогетерогенные системы. Мицеллы
|
из
5.00
|
Введение. Тут главное – научится строить мицеллы, потому что 1 из 50 вопросов точно будет про них. Кароч. Мицелла образуется в результате обменной реакции, в которой выпадает осадок, таблица растворимости в помощь. Например, AgNO3+NaCl=NaNO3+AgCl. При этом один из двух исходных электролитов должен быть взят в избытке, а то мицелла не получится. У нас будет NaCl. Дальше все просто, берем заготовку мицеллы, вот такую:
{ [ ( m… ) n… (n-x) … ] … }
И заполняем ее содержимым. После m пишется всегда осадок, он по мицелльному называется агрегат, в нашем примере AgCl. Дальше внимание, самый сложный момент! – идет ион, одинаковый в осадке и в избытке. У нас это будет Cl, по мицелльски это называется потенциалопределяющий ион. Дальше – ион, который тоже в избытке, но не потенциалопределяющий, и дальше еще раз он же, в моем примере это Na, называется противоион. Итого:
{ [ ( mAgCl ) nCl- (n-x) Na+ ] Na+ }
Потенциалопределяющий ион определяет заряд мицеллы, если он +, то и мицелла считается +, а хули вы хотели, потенциалопределяющий же. Если мицелла «+» то идет к катоду, «-» к аноду. Агрегат + потенциалопределяющий ион = ядро, все, что в квадратных скобках = гранула. Все полностью = мицелла. Потенциалопределяющий+первый противоион = плотный адсорбционный слой, второй противоион=диффузный слой. Так решаются задачи, когда известно, что в избытке, а определить надо потенциалопределяющий и противо-ион. Иногда бывают обратные задачи, когда известен противоион, или потенциалопределяющий, а построить надо мицеллу. Рассуждение обратное, что в противоионах, то и в избытке было.
Типичные вопросы:
1. Мицелла, строение.
Пример:

Красота.
Как с этим бороться:
Прочитать и понять введение к этому разделу, запомнить и научиться строить мицеллы быстро и находить в них составные части: агрегат-ядро-гранулу и т.д.
2. Правило Шульце-Гарди.
Пример:

Как то так.
Как с этим бороться:
Само правило утверждает, что:
1) Коагуляцию вызывают ионы, противоположные по знаку заряду гранулы
2) Коагулирующая способность возрастает с ростом заряда, пропорциональность 6 степени.
По первой части все ясно, на тему второй части попадаются порой знатные финты ушами. Например, В похоже на нее, но только наоборот. Или было про соотнесение коагулирующих способностей ионов с зарядами 1 и 3, соотношение получается 16:36=1:729. Всего не угадаешь, включайте голову.
3. Стабилизация систем.
Пример:

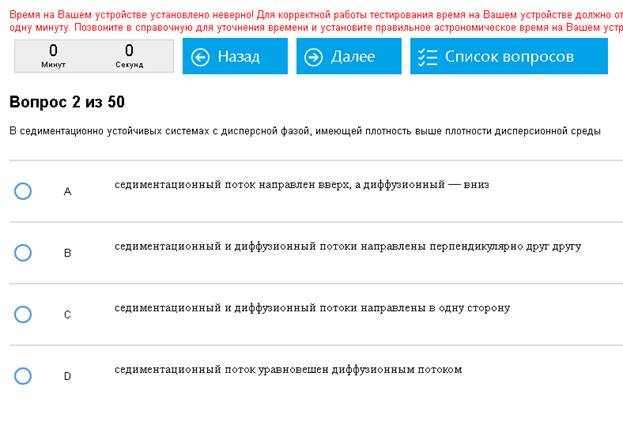
Жесть.
Как с этим бороться:
Общих методов тут нет, к сожалению, надо читать умную книжку и по данным там определениям ориентироваться. По примерам: агрегативная устойчивость повышается при добавлении ПАВ, этот вид устойчивости – устойчивость против объединения частиц. Седиментационная устойчивость – устойчивость к оседанию частиц, при этом седиментационный и диффузионный потоки уравновешены.
4. Образование ДЭС и поверхностная энергия.
Пример:
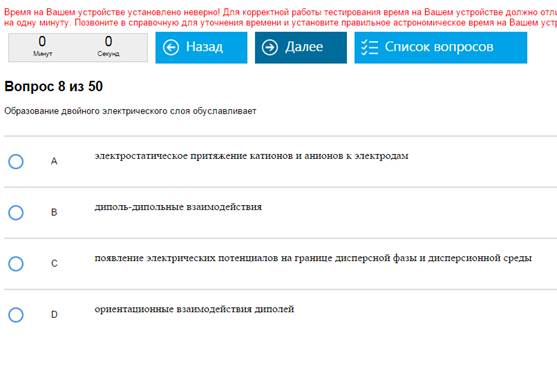


Болтовня.
Как с этим бороться:
Никак, только прочитав кучу умного текста и осмыслив его. В вопросах нет последовательности, их нельзя решать как одинаковые типовые задачи. Беда-беда. Первый пример – С, ну просто вот так есть и все, второй – тоже С, третий - А. Такова природа, вопросы почему в рамках этого пособия неуместны, хотя я мог бы и ответить.
Модуль, Органика
Тема 1. Номенклатура.
Введение. Обязательно нужно иметь в голове/под рукой обе таблицы по органике из голубой методички, а так же дополнить их недостающими веществами: сложными эфирами, сложными тиоэфирами, амидами, иминами, полуацеталями, ацеталями, альдолями.
Типичные вопросы:
1. Поставить в соответствие класс и формулу.
Пример:

Блин… что же такое альдимин и кетоимин?!? Спойлер - это А и D соответственно.

Довольно сложная разновидность вопросов такого типа.
Как с этим бороться:
элементарно, берем методичку и определяем по таблице, к какому классу какое вещество относится, есть гидроксильная группа – спирт, карбоксильная- кислота и т. д. Если в названии суффикс «ен» – то это алкен, «ол» – спирт и т. д. Суффикс «ат» характерен для сложных эфиров, оцените формиат, ацетат, пропионат. Важно извлечь связку: название класса-общая формула-приставка/суффикс в названии. Сложные случаи: двухатомный спирт НО-СН2-СН2-ОН, дикарбоновая кислота НООС-СООН, ангидрид  , ну, может, еще какая хрень попадется, типа ацетилфосфата или ацетилкофермента А, ацеталей-полуацеталей (кстати, вот и на примере они), гуглите и обрящете.
, ну, может, еще какая хрень попадется, типа ацетилфосфата или ацетилкофермента А, ацеталей-полуацеталей (кстати, вот и на примере они), гуглите и обрящете.
2. Назвать по радикально-функциональной номенклатуре.
Пример:

Fail… вариант А – ответ вопросом на вопрос? А вы не верили в еврейский заговор
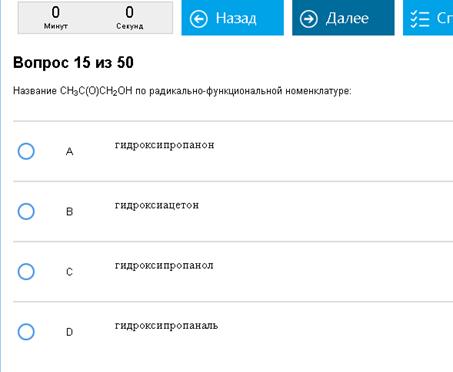
Ай. Ответ – гидроксиацетон, это патология не соответствующая алгоритму. Надеюсь, подобного больше нет

fail. Что же в итоге надо назвать? А еще эти люди запрещают нам ошибаться. Ответ – D. Вещество, которое дано в варианте А, называется дивинилкетон.
Как с этим бороться:
Для начала неплохо бы иметь под рукой/в голове таблицу радикалов и научиться отличать классы веществ друг от друга: спирты, амины, карбоновые кислоты, кетоны и проч. Освоив сию грамоту (вы же не халтурили в п. 1?), название по радикальной номенклатуре дается легко: называем радикалы, из которых состоит формула и добавляем название класса. С2Н5-ОН = этиловый спирт, СН3-О-СН3 = диметиловый эфир, N(СН3)3 = триметиламин, СН3-СН(-ОН)-СН2-СН3 = вторбутиловый спирт (извините, формула трудно читается, нету у меня сейчас хорошего редактора, чтобы красивую формулу нарисовать. Кафедра ОБОХимии, впрочем, тоже не особо заморачивается редактором химических формул, так что привыкайте). Еще нам попадался прикол про орто-, мета- и пара-изомеры бензола. Орто = заместители расположены на соседних углах, мета=через один угол, пара=через два угла, напротив друг друга. И еще прикол – карбоновые кислоты и альдегиды по непонятной причине в радикально-функциональной номенклатуре надо называть традиционными названиями: муравьиный альдегид, ацетальдегид, пропионовый альдеид – ряд альдегидов, муравьиная, уксусная, пропионовая, масляная – ряд кислот. Дополнительный бонус – нам может быть дана не формула, а название по заместительной номенклатуре, по которому нужно сначала понять, что это за неведомая хуйня вещество, а потом уже называть его по радикальной номенклатуре. О том, как бороться с заместительной номенклатурой, см. ниже.
3. Назвать по заместительной номенклатуре.
Пример:

Пропаналь такой пропаналь.
Как с этим бороться:
Заместительная номенклатура отлично описана в голубых методичках, но еще раз, для тех кто не осилил. Находим самую длинную из возможных углеродных цепей, находим функциональные (характеристические) группы, из них выбираем старшую (она обычно и единственная, если нет – смотрим правило старшинства групп), нумеруем цепь от старшей группы, строим название по схеме: приставки = радикалы и младшие группы с номерами, где они находятся, корень = длина главной цепи (метан, этан, пропан и т. д., вы ведь сдавали ЕГЭ и знакомы с этой херней, мои дорогие любители химии?), суффиксы «ан», «ен» и «ин» соответственно означают одинарные, двойные или тройные связи в главной цепи, суффикс = название старшей группы. Все эту фигню ценную информацию конкретно можно при желании извлечь из таблиц в голубой методичке. Классический пример – наш старый знакомый вторбутиловый спирт СН3-СН(-ОН)-СН2-СН3. По заместительной номенклатуре он будет называться бутанол-2. (Приставок нет, т.к. нет радикалов и младших групп, ОН-единственная и старшая поэтому, дает суффикс «ол». Нумерация углеродной цепи слева направо, чтобы ОН стояло у второго, а не третьего атома, бутанол-3 и бутанол просто без номера было бы ошибкой). Не путайте заместительную и радикальную номенклатуру. Не иначе, как из вредности, вам дано две номенклатуры. В разных номенклатурах одно и то же вещество будет называться по разному, что будет приводить к ошибкам.
4. Указать, какая группа есть у данного класса.
Пример:

Какую же группу содержит альдегид?
Как с этим бороться:
Блин, да это даже несерьезно обсуждать, я вас умоляю. Берете голубую методичку, вторая таблица, и вам откроется дивный мир органической химии, вы узнаете, что альдегиды содержат карбонильную группу, карбоновые кислоты – карбоксильную, простые эфиры – алкоксильную и т.д., и т.п. Главное, не забудьте – вы еще до сих пор умеете отличать классы органических веществ, на этой необоснованной мысли построена вся методичка.
5. Вопрос о родоначальных структурах.
Пример:

Вот и пропионовая кислота нарисовалась…
Как с этим бороться:
Довольно занудный вопрос. Насколько я могу судить, на кафедре ОБОХимии до сих пор нет внятного представления о том, что такое родоначальная структура, поэтому стоит иметь в виду следующее: родоначальная структура – это гомологический ряд карбоновых кислот, муравьиная, уксусная, пропионовая и прочее, что может быть найдено в табл. №1 голубой методички. То есть если вы видите что то типа H2N-CH2-COOH, и осознаете, что 1) это аминокарбоновая кислота 2) количество атомов «С» в ней совпадает с уксусной кислотой; то вы можете констатировать, что родоначальная структура для этой поебени биологически значимой молекулы (аминокислота глицин) – это уксусная кислота. Еще родоначальными структурами могут быть производные бензола: анилин, фенол, бензальдегид и бензойная кислота. Увы, не привожу их тут, ибо не могу рисовать здесь «гайки». Так вот, если к, например, бензольному кольцу подцеплен ОН – то это фенол, а если еще какая-нибудь группа NO2 – то это нитрофенол, а фенол для него родоначальная структура. Получилось довольно путано. Пока более простого объяснения мы не придумали, но мы работаем над этим.
6. Укажите характеристические группы в соединении
Пример:

Нитро- и гидроксильная группы затаились в молекуле
Как с этим бороться:
Элементарно. Вы же не забыли, какие бывают группы, ну же? Смотрим на формулу и мысленно вычленяем из нее, как правило, две функциональные группы.
7. Амид (фенол, ненасыщенное соединение и т.п.) – это …
Пример: забыл заскринить, извините.
Как с этим бороться:
Довольно стремный вопрос. Мне попались фенол и амид, вероятно, есть еще варианты. Надо обладать какой никакой, а все таки логикой, чтобы догадаться, что N,N-диметилацетАМИД относится к классу амидов, и какими никакими, а знаниями+логикой, чтобы указать, что фенол содержит гидроксильную группу, связанную с ароматическим кольцом
|
из
5.00
|
Обсуждение в статье: Тема 11. Ультрамикрогетерогенные системы. Мицеллы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

