 |
Главная |
PH крови и буф системы
|
из
5.00
|
механизм действия гемоглобинового буфера
гемоглобиновый буфер состоит из гемоглобина, окигемоглобина и калиевой соли гемоглобина
- гемоглобин НHb содержится в эритроцитах гемоглобин состоит из 4 полипептидных цепей и 4 гемов
гемоглобин НHb – очень слабая кислота (как белок)
НHb ® Hb- + Н+
- внутри клеток высокое содержание К+
в эритроцитах содержится калиевая соль гемоглобина КHb
калиевая соль гемоглобина КHb – сильный электролит
КHb ® Hb- + К+
- гемоглобин состоит из 4 полипептидных цепей и 4 гемов
каждый гем может присоединить 1 молекулу О2 с образованием связи кислорода и Fe2+ гема
O2 + НHb Û НHbO2
оксигемоглобин НHbO2 – кислота, более сильная, чем гемоглобин
HНbO2 Û H+ + HbO2-
- при добавлении кислоты идет реакция кислоты и калиевой соли гемоглобина КHb
Hb- + К+ + H+ + Cl-® НHb + К+ + Cl-
катионы водорода H+ связываются с образованием гемоглобина Hb- + H+® НHb
при добавлении кислоты идет реакция распада оксигемоглобина
H+ + HbO2-® HНbO2 ® O2 + НHb
при увеличении концентрации катионов водорода H+ рановесие реакции смещается вправо
- при добавлении основания идет реакция основания и гемоглобина
НHb + К+ + ОН-® Hb-+ К+ + Н2О
гидроксид-ионы ОH- связываются катионами водорода гемоглобина ОН- + H+ ® Н2О
при добавлении основания идет реакция образования оксигемоглобина
O2 + НHb ® HНbO2 ® H+ + HbO2-
+ К+ + ОН-® HbO2-+ К+ + Н2О
гидроксид-ионы ОH- связываются катионами водорода оксигемоглобина ОН- + H+ ® Н2О
- распад и образование оксигемоглобина согласуется с процессом транспорта кислорода:
более кислая среда в тканевых капиллярах, где накапливаются кислые продукты обмена веществ,
более щелочная среда в легочных капиллярах, где распадается угольная кислота и выводится СO2
64)65)Уравнению Гендерсона-Гассельбаха для расчет рН буферных систем.
буферные растворы сохраняют рН при разбавлении или добавлении небольших количеств к-ты или основания
рН буфера рассчитывают по уравнению Гендерсона-Гассельбаха
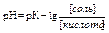 | 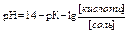 | ||||||
 | |||||||
 | |||||||
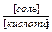 |
или
где рК – показатель кислотности или показатель основности
факторы, влияющие на рН буфера:
- природа компонетов буфера - показатель кислотности или показатель основности
- соотношение концетраций компонентов буферных растворов
оптимальное соотношение концетраций компонентов буферных растворов не более 10 (lg10=1)
69)Рабочий участок буф системы.зона буферного действия или рабочий участок рН = рК ± 1
- диапазон рН, соответствующий оптимальному соотношению концетраций компонентов буферных растворов
ПР: ацетатный буфер рН = 4,8 ± 1
гидрокарбонатный буфер рН = 6,36 ± 1
66)Буферная емкость.67)Формулы для её расчета по к-ти и щёлочи.
буферные – растворы, сохраняющие рН при разбавлении или добавлении небольших количеств к-ты или основания
способность буферных р-ров сохранять рН ограничена буферной емкостью
буферная емкость – пределы проявления буферного действия
буферная емкость равна числу молей эквивалента сильной к-ты или основания,
которые при добавлении к 1 л буфера меняют его рН на единицу
буферную емкость измеряют в моль/л
различают буферную емкость по кислоте и буферную емкость по щелочи
буферная емкость по кислоте равна числу молей эквивалента сильной кислоты,
которая при добавлении к буферу меняют его рН на единицу
буферная емкость по щелочи равна числу молей эквивалента щелочи,
которая при добавлении к буферу меняют его рН на единицу
где В - буферная емкость
|
из
5.00
|
Обсуждение в статье: PH крови и буф системы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

