 |
Главная |
Примеры решения заданий
|
из
5.00
|
Пример 1. Какова молярная концентрация раствора сульфата алюминия с массовой долей 10 % и плотностью 1,105 г/см3?

 • Масса 1 л раствора равна
• Масса 1 л раствора равна
 ρ p=1,105 г/мл
ρ p=1,105 г/мл 
CM –? • Рассчитаем массу Al2(SO4)3 в 1105 г раствора, исходя из формулы (1):

• Молярная масса  , следовательно, молярная концентрация сульфата алюминия исходя из формулы (4):
, следовательно, молярная концентрация сульфата алюминия исходя из формулы (4):

Пример 2. Чему равна массовая доля 0,2 М раствора (NH4)2SO4 с плотностью 1,015 г/мл?

 • Масса 1 л раствора равна
• Масса 1 л раствора равна
 ρ p=1,015 г/мл
ρ p=1,015 г/мл 
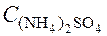 – ? • Рассчитаем массу (NH4)2SO4 в 1 л раствора,
– ? • Рассчитаем массу (NH4)2SO4 в 1 л раствора,
используя формулу (4) (молярная масса  ):
):

• Массовая доля сульфата алюминия в растворе по формуле (1) :
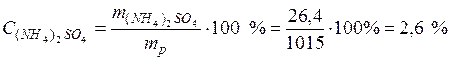
Пример 3. Смешали 50 мл 10 %-го раствора серной кислоты плотностью 1,069 г/мл и 150 мл 30 %-го раствора той же кислоты, плотностью 1,224 г/мл. Чему равна массовая доля кислоты в конечном растворе?
Условная схема приготовления конечного раствора:
раствор 1 (10 %) + раствор 2 (30 %) = раствор 3 (? %)

 • Массовая доля серной кислоты, исходя из (1):
• Массовая доля серной кислоты, исходя из (1):
ρ p 1=1,069 г/мл 
Vp 1= 50 мл • Исходя из того, что масса конечного раствора складывается
 из масс исходных растворов, а масса растворенной в нем
из масс исходных растворов, а масса растворенной в нем
ρ p 2=1,224 г/мл кислоты – из масс кислоты в исходных растворах, получаем:
 Vp 2= 150 мл
Vp 2= 150 мл 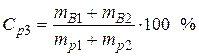
 • Используя значения плотностей растворов и выражение (1), найдем массы исходных растворов и растворенной в них серной кислоты:
• Используя значения плотностей растворов и выражение (1), найдем массы исходных растворов и растворенной в них серной кислоты:
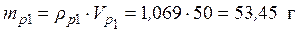

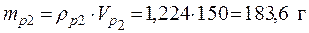

• Найдем массовую долю серной кислоты в конечном растворе:
 .
.
Пример 4. Какой объем 40 %-го раствора азотной кислоты плотностью 1,251 г/мл и воды потребуется для приготовления 500 мл 20 %-ой кислоты плотностью 1,119 г/мл?
Условная схема приготовления раствора:
раствор 1 (40 %) + вода = раствор 2 (20 %)

 • Необходимый объем исходного раствора кислоты выразим из (2):
• Необходимый объем исходного раствора кислоты выразим из (2):
ρ p 1=1,251 г/мл 
 • В полученном выражении неизвестна масса кислоты, но при
• В полученном выражении неизвестна масса кислоты, но при
ρ p 2=1,119 г/мл разбавлении исходного раствора водой масса растворенной
 Vp 2= 500 мл кислоты не изменяется, поэтому ее можно вывести из
Vp 2= 500 мл кислоты не изменяется, поэтому ее можно вывести из
Vp1– ? мл выражения массовой доли раствора 2:
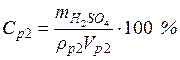

• Рассчитаем объем исходного раствора:

• Исходя из схемы получения конечного раствора:

Пример 5. Какой объем 10 %-го раствора КОН плотностью 1,082 г/мл потребуется для приготовления 2 л 1 М раствора?
Условная схема приготовления раствора:
раствор 1 (10 %) + вода = раствор 2 (1 М)

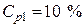 • Необходимый объем исходного раствора кислоты выразим из (2):
• Необходимый объем исходного раствора кислоты выразим из (2):
ρ p 1=1,082 г/мл 
 • В полученном выражении неизвестна масса щелочи, но при
• В полученном выражении неизвестна масса щелочи, но при
 Vp 2= 2 л разбавлении исходного раствора водой масса растворенной
Vp 2= 2 л разбавлении исходного раствора водой масса растворенной
Vp 1– ? мл щелочи не изменяется, поэтому ее можно вывести из
выражения молярной концентрации раствора 2:
 ;
; 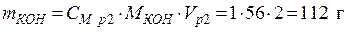
• Рассчитаем объем исходного раствора:

5.2. ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ ПОДГОТОВКИ
1. Какой объем 20 %-го раствора соляной кислоты (ρ = 1,1 г/мл) требуется для приготовления 2 л 5 %-го раствора той же кислоты (ρ = 1,02 г/мл)?
2. Определить молярную концентрацию концентрированной соляной кислоты
(ρ = 1,183 г/мл), содержащей 36 % хлороводорода.
3. Какой объем 50 %-го раствора KOH (ρ = 1,538 г/мл) требуется для приготовления 3 л 10 %-го раствора (ρ = 1,082 г/мл)?
4. Плотность 32 %-го раствора KOH равна 1,31 г/мл. Сколько моль KOH находится в 3 л раствора?
5. Какой объем 28 %-го раствора серной кислоты (ρ = 1,21 г/мл) можно приготовить из 100 г 92 %-го раствора?
6. К 1 л 6 %-го раствора серной кислоты (ρ = 1,04 г/мл) добавили 1 л воды. Вычислить молярную концентрацию полученного раствора.
7. Какой объем 50 %-го раствора H2SO4 (ρ = 1,4 г/мл) требуется для приготовления 2 л 1 М раствора?
8. Смешали 50 мл 20 %-го раствора соляной кислоты (ρ = 1,1 г/мл) и 150 мл 30 %-го раствора той же кислоты (ρ = 1,152 г/мл). Какова массовая доля HCl в полученном растворе?
9. Сколько граммов K2SO4 необходимо для приготовления 500 мл 0,1 М раствора?
10. Какой объем 20 %-го раствора NaОН плотностью 1,225 г/мл потребуется для приготовления 1 л 2 М раствора?
11. Смешали 500 г 10 %-го раствора и 300 г 30 %-го раствора H2SO4. Какова процентная концентрация полученного раствора?
12. Смешали 50 мл 30 %-го раствора азотной кислоты плотностью 1,286 г/мл и 50 мл 50 %-го раствора той же кислоты плотностью 1,316 г/мл. Чему равна массовая доля кислоты в конечном растворе?
13. Какой объем 1 М раствора хлорида натрия можно приготовить из 20 г безводного NaCl?
14. Какой объем 50 %-го раствора азотной кислоты (ρ = 1,316 г/мл) необходим для приготовления 3 л 1,5 М раствора?
15. К 1 л 10 %-го раствора NaOH (ρ = 1,115 г/мл) прибавили 3 л воды. Какова процентная концентрация полученного раствора?
16. Какая масса сульфата натрия требуется для приготовления 500 мл 0,2 М
раствора?
17. 100 мл 2 М раствора разбавили водой до 400 мл. Какова молярная концентрация раствора?
18. Из 600 г 5 %-го раствора соды (Na2CO3) выпариванием удалили 100 г воды. Какова массовая доля Na2CO3 в полученном растворе?
19. Вычислить объем 10 %-го раствора NaOH (ρ = 1,115 г/мл), который требуется для приготовления 1 л 1 М раствора.
20. В каком объеме 0,2 М раствора содержится 10 г NiSO4?
21. Смешали 20 мл 20 %-го раствора азотной кислоты (ρ = 1,119 г/мл) и 100 мл 30 %-го раствора той же кислоты (ρ = 1,184 г/мл). Вычислить процентную концентрацию полученного раствора.
22. Какая масса хлорида натрия содержится в 100 мл 1 М раствора?
23. Какой объем 10 %-го раствора карбоната натрия (ρ = 1,105 г/мл) требуется для приготовления 3 л 5 %-го раствора (ρ = 1,05 г/мл)?
24. Вычислить молярную концентрацию 25 %-го раствора сульфата цинка
(ρ = 1,3 г/мл).
25. Какой объем 30 %-й соляной кислоты (ρ = 1,152 г/мл) нужно взять для приготовления 1 л 2 М раствора?
26. Какой объем воды надо прибавить к 100 мл 50 %-го раствора азотной кислоты (ρ = 1,316 г/мл) для получения 20 %-го раствора?
27. Какая масса KNO3 должна быть растворена в 500 мл воды для получения 5 %-го раствора?
28. К 2 л 10 %-го раствора азотной кислоты (ρ = 1,054 г/мл) добавили 3 л
4 %-го раствора той же кислоты (ρ = 1,022 г/мл). Вычислить процентную концентрацию полученного раствора.
29. Вычислить молярную концентрацию 20 %-го раствора сульфата железа (II) (ρ = 1,21 г/мл).
30. К 50 мл 96 %-го раствора азотной кислоты (ρ = 1,5 г/мл) прилили 30 мл 9,9 М раствора той же кислоты (ρ = 1, 3 г/мл). Какова процентная концентрация полученного раствора?
Электролиты
Электролиты – это вещества, растворы и расплавы которых проводят электрический ток.
Способность электролитов проводить электрический ток называется электролитической проводимостью. Она связана с тем, что направленное перемещение ионов создает поток электрических зарядов.
|
из
5.00
|
Обсуждение в статье: Примеры решения заданий |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

