 |
Главная |
Расчеты в титриметрическом анализе
|
из
5.00
|
Титриметрический анализ – это метод количественного анализа, основанный на определении объема раствора реагента с точно известной концентрацией, затраченного на реакцию с определяемым компонентом.
В основе титриметрического анализа лежит химическая реакция:
bB + a A = продукты
B – определяемое или титруемое вещество (компонент), концентрация его не известна;
A - рабочий раствор или титрант, его концентрация известна;
a и b – стехиометрические коэффициенты реакции.
Любой раствор с точно известной концентрацией называется стандартным раствором. По способу приготовления стандартные растворы делятся на
первичные и вторичные.
Первичный стандартный раствор можно приготовить двумя способами:
1) Растворением точной навески вещества в определенном объеме растворителя. Вещества, по навеске которых можно приготовить стандартный раствор, называются первичными стандартами (установочные вещества, исходные вещества). Их состав должен строго соответствовать химической формуле, они должны быть химически чистыми и устойчивыми при хранении в твердом виде и в растворе. Каждый метод титриметрического анализа имеет свой первичный стандарт.
2) По фиксаналам или стандарт-титрам. Это промышленным способом приготовленные и запаянные в стеклянные ампулы точные навески веществ или объемы жидкостей, растворением которых в определенном объеме воды можно приготовить раствор с точно известной концентрацией.
Вторичный стандартный раствор готовят по приблизительной навеске с приблизительной концентрацией, затем определяют его концентрацию, т.е. стандартизируют по подходящему первичному стандартному раствору.
Основной операцией в титриметрическом анализе является титрование - это процесс постепенного прибавления титранта к раствору определяемого вещества до тех пор, пока их количества не станут эквивалентными. Этот момент называется точкой эквивалентности (ТЭ), которая фиксируется обычно по изменению окраски индикатора или другим способом.
В зависимости от типа реакции в титриметрическом анализе различают:
1) метод кислотно-основного титрования (метод нейтрализации, протолитометрия);
2) метод окислительно-восстановительного титрования (редоксметрия);
3) метод комплексонометрического титрования (комплексонометрия);
4) метод осадительного титрования.
В любом из этих методов можно использовать разные приемы (способы) титрования:
1) Прямое титрование – самое распространенное и удобное. Используется один рабочий раствор (титрант). Окончание титрования устанавливают по изменению окраски индикатора. По шкале бюретки определяют объем титранта, пошедший на реакцию (это аналитический сигнал), и по нему находят содержание определяемого вещества. Все расчеты ведут на основе закона эквивалентов: вещества взаимодействуют между собой и образуются в равных количествах эквивалентов. Для реакции
b B + a A = d D + c C
запись этого закона имеет вид:
𝛎(1/zB) = 𝛎(1/zA)= 𝛎(1/zD)= 𝛎(1/zC) (3.1);
где 𝛎(1/zX)- число молей эквивалентов любого из участвующих в реакции веществ (Х); B – определяемое вещество; A - рабочий раствор.
Из этого уравнения вытекают следующие расчетные формулы:
 =
= 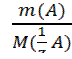 (3.2);
(3.2);
c (  ) ∙ V(B) = c (
) ∙ V(B) = c (  ∙ V(A) (3.3);
∙ V(A) (3.3);
Уравнение (3.3) называют основным уравнением титриметрического анализа.
Комбинированием уравнений 3.2 и 3.3 получают формулы:
 c (
c (  ∙ V(A) (3.4);
∙ V(A) (3.4);
 c (
c (  ∙ V(B) (3.5);
∙ V(B) (3.5);
m(B) = c (  ∙ V(A) ∙ M(1/z B) (3.6).
∙ V(A) ∙ M(1/z B) (3.6).
При титровании методом пипетирования массу определяемого компонента рассчитывают по формуле:
m(B) =  ∙
∙ 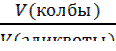 (3.7).
(3.7).
В приведенных выше уравнениях (3.2 - 3.7) использованы следующие обозначения: c (1/z X) – молярная концентрация эквивалента вещества (X) или нормальная концентрация, моль/л; m(X) – масса вещества, г; M(1/z X) – молярная масса эквивалента вещества, г/моль; 1/z – фактор эквивалентности; V(X) – объем раствора, в уравнениях (3.4-3.6) выражается в литрах; в уравнениях (3.3 и 3.7) объемы V(Х), V(колбы), V(аликвоты) выражаются в мл или см3.
При проведении расчетов в аналитической химии удобно пользоваться понятиями титра и титра рабочего раствора по определяемому веществу.
Титр раствора вещества – Т(X), г/см3 или г/мл - показывает, сколько граммов растворенного вещества содержится в 1 см3 (мл) раствора.
Т(X) =  (3.8).
(3.8).
Между нормальной концентрацией и титром существует взаимосвязь:
c(  x) =
x) =  (3.9) ; Т(X) =
(3.9) ; Т(X) =  (3.10).
(3.10).
Титр рабочего раствора по определяемому веществу - Т раб/опр или Т А/В - показывает, сколько г определяемого вещества взаимодействует с 1 мл (см3) рабочего раствора.
Траб/опр =  (3.11).
(3.11).
Эту величину можно рассчитать по формулам:
Траб/опр =  (3.12) ; Траб/опр =
(3.12) ; Траб/опр =  (3.13);
(3.13);
Траб/опр  (3.14).
(3.14).
Расчеты титра, нормальной концентрации и массы определяемого вещества при обработке экспериментальных данных проводят двумя способами:
I способ (по основному уравнению титриметрического анализа):
1) c (  ) ∙ V(B) = c (
) ∙ V(B) = c (  ∙ V(A);
∙ V(A);
2) Т(В) =  ;
;
3) m(В) = Т(В) ∙ V(колбы)
II способ (через титр рабочего раствора по определяемому веществу):
1) Траб/опр =  ;
;
2) Т (В) =  ;
;
3) c (  B) =
B) =  ;
;
4) m(В) = Т(В) ∙ V(колбы).
Здесь: В - определяемое вещество, А-рабочий раствор, V(колбы) - объем мерной колбы.
Наряду с прямым титрованием (1), описанном выше, в титриметрическом анализе используются и другие способы (приёмы) титрования.
2) Обратное титрование - используют, когда прямое титрование невозможно или когда определяемое вещество неустойчиво. В данном способе титрования к определяемому веществу добавляют в избытке определенный объем (V1) рабочего раствора №1. Затем его избыток оттитровывают рабочим раствором №2 (V2). Расчет содержания определяемого вещества ведут с учетом двух химических реакций, используя V1 и V2.
3) Заместительное титрование – применяют, когда нет подходящей реакции или индикатора для прямого титрования. В данном способе титрования к определяемому веществу добавляют вспомогательный реагент. Получившийся в эквивалентном количестве продукт, оттитровывают подходящим титрантом. По объему титранта сразу рассчитывают содержание определяемого вещества, минуя все расчеты вспомогательных реагентов.
4) Реверсивное титрование – применяют, когда определяемое вещество неустойчиво в условиях эксперимента. В этом случае рабочий раствор титруют раствором определяемого вещества. Способ используют, например, для определения содержания нитритов методом перманганатометрии.
Метод нейтрализации
Применяется для определения содержания кислот, оснований, солей, подвергающихся гидролизу и других веществ, реагирующих с кислотами или основаниями.
В основе этого метода лежит реакция:
H+ + OH- = H2O или
H3O+ + OH- = 2 H2O
Кривые титрования в методе нейтрализации - это графическая зависимость pH раствора от объема добавленного титранта. Рассмотрим три случая кривых титрования.
1) Титрование сильной кислоты сильным основанием (рис.1.):
HCl + NaOH = NaCl + H2O
Расчет кривой проведен для титрования 100.0 мл 0.1000 н раствора HCl 0.1000 н раствором NaOH.
На кривой титрования наблюдается скачок титрования - это резкое изменение pH раствора вблизи точки эквивалентности.
В данном случае скачок титрования лежит в интервале от рН=4 до рН=10. Величина скачка составляет 6 единиц рН.
Точка эквивалентности (ТЭ) совпадает с точкой нейтральности (ТН) – это точка, в которой рН раствора равен 7.
Кривая титрования симметрична относительно точки эквивалентности и точки нейтральности.
2) Титрование слабой кислоты сильным основанием (рис.2.):
CH3COOH + NaOH = CH3COONa + H2O
Расчет кривой проведен для случая взаимодействия 100.0 мл 0.1000 н раствора CH3COOH с 0.1000 н раствором NaOH. В данном случае скачок титрования лежит в интервале от рН=7.76 до рН=10. Величина скачка составляет 2.24 единиц pH, что значительно меньше, чем в первом случае. Точка эквивалентности лежит в щелочной области (pH = 8.87) и не совпадает с точкой нейтральности в результате гидролиза соли CH3COONa по аниону. Кривая титрования несимметрична относительно ТЭ и ТН.

Рис. 1. Титрование сильной кислоты сильным основанием.
| |
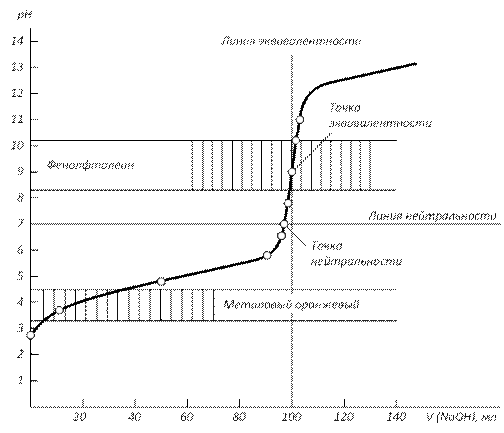
Рис.
| |
3) Титрование слабого основания сильной кислотой (рис.3.):
NH4OH + HCl = NH4Cl + H2O
Расчет кривой проведен для взаимодействия 100.0 мл 0.1000 н раствора NH4OH с 0.1000 н раствором HCl . В данном случае скачок титрования находится в интервале от рН=4 до рН=6,24. Величина скачка составляет 2.24 единиц pH. Точка эквивалентности лежит в кислотной области (pH=5.11) и не совпадает с точкой нейтральности в результате гидролиза соли NH4Cl по катиону. Кривая титрования несимметрична относительно ТЭ и ТН.

| |
Во всех трех случаях величина скачка увеличивается с увеличением концентрации реагирующих веществ и с уменьшением температуры. Чем больше величина скачка рН, тем точнее можно оттитровать определяемое вещество.
|
из
5.00
|
Обсуждение в статье: Расчеты в титриметрическом анализе |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

