 |
Главная |
Определение влияния температуры на константу скорости реакции.
|
из
5.00
|
Для выяснения влияния температуры на константу скорости реакции, описанным ранее способом находим значение констант скорости при температурах опытов 7, 8, 9:
а) При температуре t=80ºС, СA,O=1,0 моль/л, СY-,O=0,5 моль/л, τ1 = 8900, τ2 = 17800, …, τ8=71200 были получены такие данные:
Таблица 3.6. Результаты опыта 7, приведённые для линейной функции (3.11).
| i | τi | 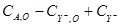
| 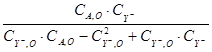
| αi |
| 1 | 8900 | 0,911 | 0,902305 | 0,205605 |
| 2 | 17800 | 0,842 | 0,812352 | 0,415644 |
| 3 | 26700 | 0,781 | 0,71959 | 0,658147 |
| 4 | 35600 | 0,736 | 0,641304 | 0,888502 |
| 5 | 44500 | 0,708 | 0,587571 | 1,063518 |
| 6 | 53400 | 0,675 | 0,518519 | 1,313559 |
| 7 | 62300 | 0,651 | 0,463902 | 1,536165 |
| 8 | 71200 | 0,634 | 0,422713 | 1,722124 |
Таблица 3.7. Расчётная таблица для опыта 7.
| i | τi | αi | (τi)2 | τiαi |
| 1 | 8900 | 0,205605 | 79210000 | 1829,885 |
| 2 | 17800 | 0,415644 | 316840000 | 7398,467 |
| 3 | 26700 | 0,658147 | 712890000 | 17572,51 |
| 4 | 35600 | 0,888502 | 1267360000 | 31630,68 |
| 5 | 44500 | 1,063518 | 1980250000 | 47326,54 |
| 6 | 53400 | 1,313559 | 2851560000 | 70144,05 |
| 7 | 62300 | 1,536165 | 3881290000 | 95703,1 |
| 8 | 71200 | 1,722124 | 5069440000 | 122615,2 |
| Сумма: | - | - | 16158840000 | 394220,5 |
Отсюда по формуле (3.14):
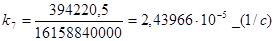
Таблица 3.8. Расчётная таблица для дисперсии адекватности опыта 7.
| i | 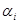
| 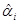
| 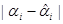
| 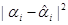
|
| 1 | 0,205605 | 0,21713 | 0,011525 | 0,000133 |
| 2 | 0,415644 | 0,434259 | 0,018615 | 0,000347 |
| 3 | 0,658147 | 0,651389 | 0,006758 | 4,57∙10-5 |
| 4 | 0,888502 | 0,868518 | 0,019984 | 0,000399 |
| 5 | 1,063518 | 1,085648 | 0,02213 | 0,00049 |
| 6 | 1,313559 | 1,302777 | 0,010782 | 0,000116 |
| 7 | 1,536165 | 1,519907 | 0,016258 | 0,000264 |
| 8 | 1,722124 | 1,737037 | 0,014913 | 0,000222 |
| Сумма: | - | - | - | 0,002017 |
Тогда по уравнению (3.16):
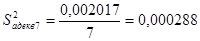
Проверку адекватности уравнения регрессии эксперименту проводиться по критерию Фишера по формуле (3.17):
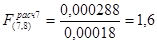
Для p = 0,05 по табличным данным [1] , 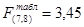 . Таким образом, т.к.
. Таким образом, т.к. 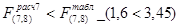 , то гипотеза об адекватности принимается.
, то гипотеза об адекватности принимается.
б) При температуре t=90ºС, СA,O=1,0 моль/л, СY-,O=0,5 моль/л, τ1 = 3900, τ2 = 7800, …, τ8=31200 были получены такие данные:
Таблица 3.9. Результаты опыта 8, приведённые для линейной функции (3.11).
| i | τi | 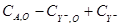
| 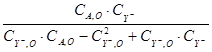
| αi |
| 1 | 3900 | 0,898 | 0,886414 | 0,241142 |
| 2 | 7800 | 0,841 | 0,810939 | 0,419124 |
| 3 | 11700 | 0,781 | 0,71959 | 0,658147 |
| 4 | 15600 | 0,74 | 0,648649 | 0,865728 |
| 5 | 19500 | 0,702 | 0,575499 | 1,105037 |
| 6 | 23400 | 0,677 | 0,522895 | 1,296749 |
| 7 | 27300 | 0,654 | 0,470948 | 1,506015 |
| 8 | 31200 | 0,633 | 0,420221 | 1,733948 |
Таблица 3.10. Расчётная таблица для опыта 8.
| i | τi | αi | (τi)2 | τiαi |
| 1 | 3900 | 0,241142 | 15210000 | 940,4528832 |
| 2 | 7800 | 0,419124 | 60840000 | 3269,167233 |
| 3 | 11700 | 0,658147 | 137000000 | 7700,315219 |
| 4 | 15600 | 0,865728 | 243000000 | 13505,35937 |
| 5 | 19500 | 1,105037 | 380000000 | 21548,22252 |
| 6 | 23400 | 1,296749 | 548000000 | 30343,92004 |
| 7 | 27300 | 1,506015 | 745000000 | 41114,21324 |
| 8 | 31200 | 1,733948 | 973000000 | 54099,18467 |
| Сумма: | - | - | 3100000000 | 172520,8352 |
Отсюда по формуле (3.14):
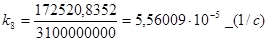
Таблица 3.11. Расчётная таблица для дисперсии адекватности опыта 8.
| i | 
| 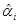
| 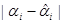
| 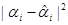
|
| 1 | 0,241142 | 0,216844 | 0,024298 | 0,00059 |
| 2 | 0,419124 | 0,433687 | 0,014563 | 0,000212 |
| 3 | 0,658147 | 0,650531 | 0,007616 | 5,8∙10-5 |
| 4 | 0,865728 | 0,867375 | 0,001647 | 2,71∙10-6 |
| 5 | 1,105037 | 1,084218 | 0,020819 | 0,000433 |
| 6 | 1,296749 | 1,301062 | 0,004313 | 1,86∙10-5 |
| 7 | 1,506015 | 1,517906 | 0,011891 | 0,000141 |
| 8 | 1,733948 | 1,734749 | 0,000801 | 6,42∙10-7 |
| Сумма: | - | - | - | 0,001457 |
Тогда по уравнению (3.16):
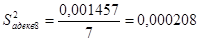
Проверку адекватности уравнения регрессии эксперименту проводиться по критерию Фишера по формуле (3.17):
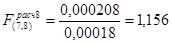
Для p = 0,05 по табличным данным [1] , 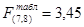 . Таким образом, т.к.
. Таким образом, т.к. 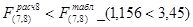 , то гипотеза об адекватности принимается.
, то гипотеза об адекватности принимается.
в) При температуре t=100ºС, СA,O=1,0 моль/л, СY-,O=0,5 моль/л, τ1 = 1800, τ2 = 3600,…, τ8=14400 были получены такие данные:
Таблица 3.12. Результаты опыта 9, приведённые для линейной функции (3.11).
| i | τi | 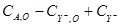
| 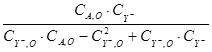
| αi |
| 1 | 1800 | 0,907 | 0,897464 | 0,216364 |
| 2 | 3600 | 0,833 | 0,79952 | 0,447488 |
| 3 | 5400 | 0,776 | 0,71134 | 0,681209 |
| 4 | 7200 | 0,739 | 0,64682 | 0,871374 |
| 5 | 9000 | 0,703 | 0,577525 | 1,098007 |
| 6 | 10800 | 0,672 | 0,511905 | 1,339233 |
| 7 | 12600 | 0,648 | 0,45679 | 1,567062 |
| 8 | 14400 | 0,63 | 0,412698 | 1,770076 |
Таблица 3.13. Расчётная таблица для опыта 9.
| i | τi | αi | (τi)2 | τiαi |
| 1 | 1800 | 0,216364 | 3240000 | 389,4555 |
| 2 | 3600 | 0,447488 | 12960000 | 1610,957 |
| 3 | 5400 | 0,681209 | 29160000 | 3678,528 |
| 4 | 7200 | 0,871374 | 51840000 | 6273,896 |
| 5 | 9000 | 1,098007 | 81000000 | 9882,067 |
| 6 | 10800 | 1,339233 | 117000000 | 14463,72 |
| 7 | 12600 | 1,567062 | 159000000 | 19744,99 |
| 8 | 14400 | 1,770076 | 207000000 | 25489,1 |
| Сумма: | - | - | 661000000 | 81532,71 |
Отсюда по формуле (3.14):
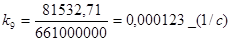
Таблица 3.14. Расчётная таблица для дисперсии адекватности опыта 9.
| i | 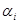
| 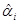
| 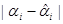
| 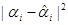
|
| 1 | 0,216364 | 0,222039 | 0,005675 | 3,22∙10-5 |
| 2 | 0,447488 | 0,444078 | 0,00341 | 1,16∙10-5 |
| 3 | 0,681209 | 0,666117 | 0,015092 | 0,000228 |
| 4 | 0,871374 | 0,888156 | 0,016782 | 0,000282 |
| 5 | 1,098007 | 1,110195 | 0,012187 | 0,000149 |
| 6 | 1,339233 | 1,332234 | 0,007 | 4,9∙10-5 |
| 7 | 1,567062 | 1,554273 | 0,01279 | 0,000164 |
| 8 | 1,770076 | 1,776312 | 0,006235 | 3,89∙10-5 |
| Сумма: | - | - | - | 0,000953 |
Тогда по уравнению (3.16):
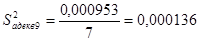
Проверку адекватности уравнения регрессии эксперименту проводиться по критерию Фишера по формуле (3.17):
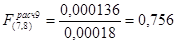
Для p = 0,05 по табличным данным [1] , 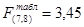 . Таким образом, т.к.
. Таким образом, т.к. 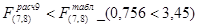 , то гипотеза об адекватности принимается.
, то гипотеза об адекватности принимается.
Далее из уравнения Аррениуса (3.21):
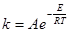 (3.21)
(3.21)
Получим линеаризованную форму:
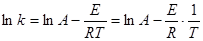 (3.22)
(3.22)
Для найденных значений k7, k8, k9, равных, соответственно:
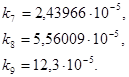
Строим график в координатах уравнения (3.22), т.е. (ln ki) от (1/T). По графику рис. 3.4 можно определить значение A и значение E, т.к. 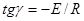 , а отрезок отсекаемый графиком на оси ln ki равен ln A. Отсюда, т.к.
, а отрезок отсекаемый графиком на оси ln ki равен ln A. Отсюда, т.к. 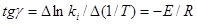 , то
, то 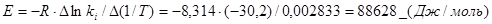 , а A = 3,2522∙108.
, а A = 3,2522∙108.
По найденному значению энергии активации и значению константы скорости, находим значение энтропии активации, например для опыта 7, по формуле (3.23):
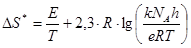 (3.23)
(3.23)
Где NA – число Авогадро, h – постоянная Планка. Следовательно, имеем:
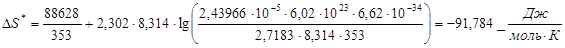
Полученное положительное значение энтропии активации подтверждает предположение о бимолекулярном механизме реакции.
С учётом полученных активационных параметров кинетическая модель реакции будет иметь вид:
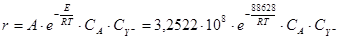 (3.24)
(3.24)
|
из
5.00
|
Обсуждение в статье: Определение влияния температуры на константу скорости реакции. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

