 |
Главная |
Высаливание и денатурация белков.
|
из
5.00
|
Денатурация белка .
• Обратимая денатурация.
-частичное разрушение пространственной структуры белка (Возможен обратный процесс .
РЕНАТУРАЦИЯ).Обратимая денатурация происходит в результате высаливания –осаждения белка (-выделение белка из раствора добавлением соли) или коагуляции (-нарушение структуры гидратных оболочек макромолекул белка ,
приводящее к выпадению гелеобразного осадка)
• Необратимая денатурация
-полное разрушение пространственной структуры белка, приводящее к потере биологической активности( ренатурация невозможна !)
Высаливание — это добавление к раствору белка нейтральных солей (Na2SO4, (NH4)2SO4). Механизм высаливания заключается во взаимодействии анионов (SO42-) и катионов (Na+, NH4+) с зарядами белка (группы NH4+ и COO-). В результате заряд исчезает, и соответственно, исчезает взаимоотталкивание молекул. Одновременно резко уменьшается гидратная оболочка. Все это приводит к «слипанию» молекул и осаждению.
Так как белки плазмы крови отличаются по размерам, заряду, строению, то можно подобрать такие количества соли, которые вызовут осаждение менее устойчивых белков, пока другие еще будут растворены.
Например, раньше в диагностических целях так определяли соотношение белковых фракций альбумины/глобулины в плазме крови. Альбумины, как более полярные молекулы, остаются в растворенном состоянии при 50 % насыщении раствора нейтральными солями, в то время как глобулины в этих условиях уже осаждаются. В норме соотношение альбумины/глобулины в плазме крови равно 1,2-1,8.
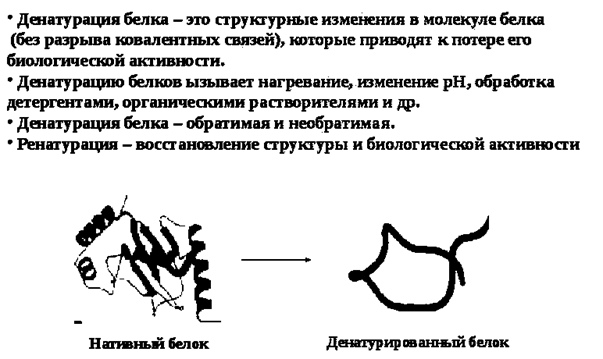
Денатурация белка
1. Обратимая – после устранения воздействия денатурирующего агента белок восстанавливает свою активность (произошла ренатурация).
2. Необратимая денатурация (происходит необратимое нарушение первичной структуры белка).

Классификация белков
По структуре белки делят на простые и сложные.
Простые белки состоят только из аминокислот. В состав сложных белков входит небелковый компонент, название которого включается в название сложного белка. Это нуклеопротеины, липопротеины, гликопротеины, металопротеины, фосфопротеины, хромопротеины (окрашенные белки), дикомпонентные ферменты.
По физико – химическим свойствам:
а) - фибрилярные белки. Имеют упорядоченную, регулярную структуру (повторяемость в пространстве одинаковых участков молекулы). Они образуют огромной величины и молекулярной массы агрегаты (фибриллы). Например, коллаген, масса которого составляет около 30% от общего количества тканевых белков. Коллаген основной белок межклеточного пространства, хрящей, сухожилий, костей, зубов (в пищевом отношении это неполноценный белок, поскольку содержит мало незаменимых аминокислот). Коллаген отличается высоким содержанием глицина (35%), аланина (11%), пролина и оксипролина (21%). Белок имеет трехцепочечную спиральну структуру, обладает большой механической прочностью (у тропо- коллагена – прочность такая же как и у стальной проволоки).
б) - глобулярные белки – имеют глобулярную структуру, водорастворимые, гидрофильные. Структура этих белков наименее регулярная (повторяемая). в)- мембранные белки – “живут” в мембранах, они частично либо полностью гидрофобные, обладают в большей или меншей степени регулярной структурой.
По функциям
Функции белков. Белки выполняют в организме большинство функций и с ними связаны практически все проявления жизни. Белки делят на такие группы:
1. Каталитические белки. Это специализованный класс белков – ферменты.
2. Сократительные белки. Выполняют функцию движения ( актин и миозин).
3. Защитные белки (антитела, другие антимикробные факторы; защита от кровопотери – фибриноген, факторы свертывания крови т.д.)
4. Регуляторные белки. Сигнальные белки и олигопептиды, гормоны, рецепторы и т.д.
5. Транспортные белки (транспорт веществ в крови, через мембраны). Сейчас известно свыше 6 тысяч транспортных белков.
6. Структурные белки – мембраные, соединительной ткани (коллаген, эластин т.д.), волос (α– кератин) т.д.
7. Пищевые – содержатся в продуктах питания.
8. Запасные и т.д.
4. По генам, которые отвечают за структуру белков. Это наиболее современная классификация белков.
Альбумины: обнаружены во многих тканях (главным образом в цитоплазме клеток, в мышцах – миоальбумины; в молоке – лактальбумины; нервная ткань – содержит нейроальбумины, высокое содержание в сыворотке крови – 40-50г/л), имеют сходные свойства. Молекулярная масса – до 70000, это кислые белки, ИЭТ около 4,7, содержат много глутаминовой кислоты, имеют глобулярную структуру, растворимы в воде. Альбумины крови синтезируются в печени, обуславливают онкотическое давление крови (при снижении альбуминов возникают отеки). Альбумины крови это основные транспортные белки в организме, они обеспечивают транспорт водо- и жирорастворимых витаминов, билирубина, лекарств.
Глобулины – имеют большую массу (выше 150000 Да), плохо растворимы в воде и легче аль- буминов, осаждаются солями, электрофорезе глобулины крови разделяются на несколько фракций (α-, β- и γ-глобулины), в которых обнаруживаются такие белки как – протромбин, церуллоплазмин, иммуноглобулины. Протамины и гистоны: ядерные белки (в ядре клетки связаны с нуклеиновыми кислотами), содержат много аргинина и лизина (гистоны до 30%, а протамины до 60%), которые обуславливают положительный заряд этих белков (катионные белки), ИЭТ в щелочной среде.
Проламины и глутелины – растительного происхождения белки (глутелин – белок пшеницы, зеин – выделен из кукурузы), содержать недостаточные количества незаменимых аминокислот, поэтому в пищевом отношении это неполноценные белки.
Пептиды – выделяют несколько груп пептидов ( нейропептиды - эндорфины, энкефалины), пептиды кининовой системы и др.
Простые (однокомпонентные) ферменты – пепсин, трипсин.
Сократительные белки - актин, миозин.
Белковоподобные вещества (склеропротеины)



|
из
5.00
|
Обсуждение в статье: Высаливание и денатурация белков. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

