 |
Главная |
Доказательство наличия двух карбоксильных групп в винной кислоте
|
из
5.00
|
В пробирку поместите 1 каплю 15% раствора винной кислоты и 2 капли 5% раствора гидроксида калия. Потрите внутреннюю стенку пробирки стеклянной палочкой до начала выпадения белого кристаллического осадка. Добавьте в пробирку еще 4-5 капель раствора гидроксида калия. Что вы наблюдаете? Сделайте вывод о растворимости кислого и среднего тартрата калия. Напишите схемы проведенных реакций.
Раствор тартрата калия сохраните для следующего опыта.
Доказательство наличия гидроксильных групп в винной кислоте
В пробирку поместите по 2 капли 2% раствора сульфата меди (II) и 10% раствора гидроксида натрия. К полученному голубому осадку гидроксида меди (II) добавьте раствор тартрата калия, полученный в предыдущем опыте. Что вы наблюдаете? О наличии какого фрагмента в молекуле винной кислоты свидетельствует данная реакция? Запишите её схему.
Продукт данной реакции носит название реактива Фелинга и применяется для обнаружения глюкозы в моче.
Блок информации
Граф 16
Классификация кислород- и азотсодержащих гетерофункциональных соединений
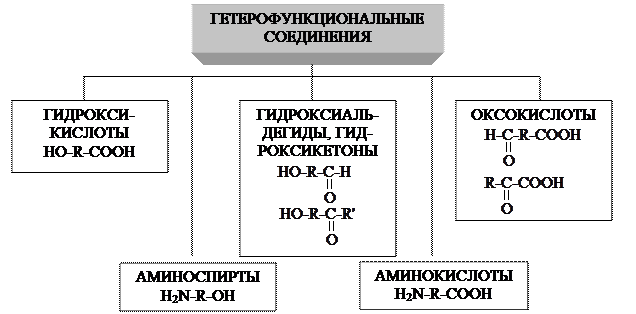
Граф 17
Свойства α-гидроксикислот

H2SO4, to
(R’CO)2O
NaOH
[O]
R’OH, H+
Граф 18
Специфические свойства α-, β-, γ-гидроксикислот

to
α -H2O β -H2O γ -H2O
Граф 19
Свойства α-аминокислот
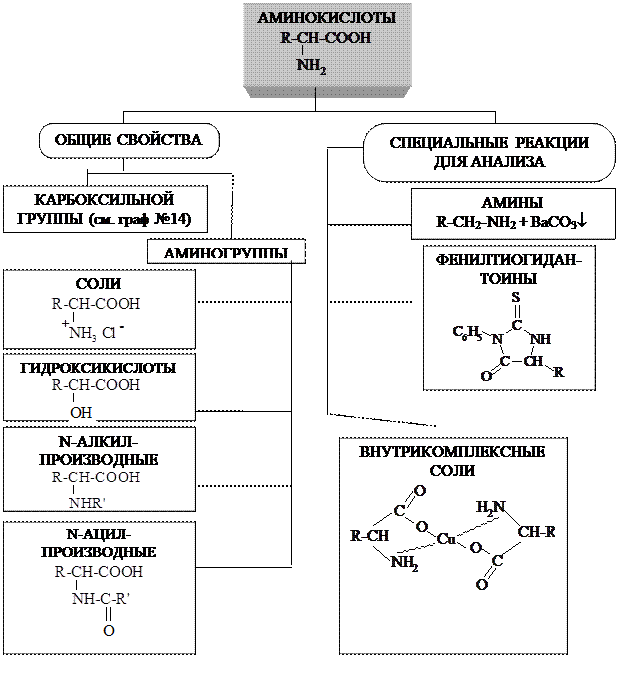
Ba(OH)2
to
HCl C6H5N=C=S
HNO2 Cu(OH)2
R’-Cl
(R’CO)2O
Граф 20
Специфические свойства α-, β-, γ-аминокислот

to
α -H2O β -NH3 γ -H2O

Приложение
Вопросы для тестового контроля
УКАЖИТЕ СООТВЕТСТВИЯ!
1.
Тривиальное название IUPAC
1. молочная кислота а) 2-оксипропионовая г) 3-аминопентановая
2. β-аминомасляная кислота б) 2-оксипропановая д) 3-аминобутановая
в) 2-аминобутановая
2. 
а) β-оксимасляная
б) γ-оксимасляная
в) винная
г) яблочная
д) лимонная
е) молочная
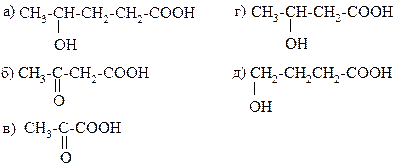 3.
3.
1. γ-оксимасляная кислота
2. ацетоуксусная кислота
 4.
4.
Название кислоты по IUPAC
а) пировиноградная г) 4-аминобутановая
б) 2-оксопропановая д) ацетоуксусная
в) γ-аминомасляная е) 2-оксипропановая
 5.
5.
1. норадреналин
2. адреналин
6. IUPAC Тривиальное название
1. 2-гидроксипропановая кислота а) яблочная г) винная
2. 4-аминобутановая кислота б) молочная д) β-аминомасляная
в) γ-аминовалериановая е) γ-аминомасляная
7.

 8.
8.
9.
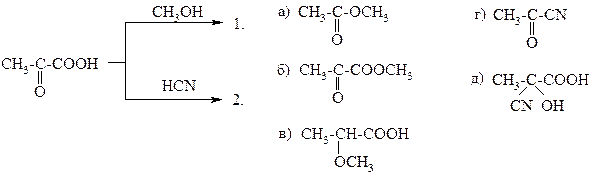
10.
 | ||
 |
11.
12.

13.

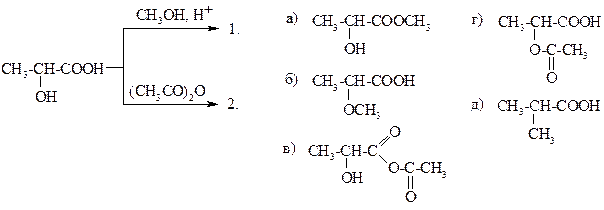
14.
 15.
15.
 16.
16.
 |
17.
 |
18.
19.
соединение продукт, полученный при нагревании
1. α-оксикислота а) лактид г) α,β-непредельная кислота
2. γ-аминокислота б) лактам д) дикетопиперазин
в) лактон
20.
соединение продукт, полученный при нагревании
1. α-аминокислота а) лактид г) α,β-непредельная кислота
2. β-оксикислота б) лактам д) дикетопиперазин
в) лактон
21.
соединение продукт, полученный при нагревании
1. α-оксикислота а) лактид г) α,β-непредельная кислота
2. γ-оксикислота б) лактам д) дикетопиперазин
в) лактон
22.
соединение продукт, полученный при нагревании
1. α-аминокислота а) лактид г) α,β-непредельная кислота
2. β-аминокислота б) лактам д) дикетопиперазин
в) лактон
23.
соединение продукт, полученный при нагревании
1. β-аминокислота а) лактид г) α,β-непредельная кислота
2. γ-аминокислота б) лактам д) дикетопиперазин
в) лактон
24.
таутомер щавелевоуксусной соединения, с которыми он
кислоты вступает в реакцию
1. кето-таутомер а) HCN в) Br2/H2O
2. енольный таутомер б) FeCl3 г) NH2NH2
 |
25.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
26.
ТАУТОМЕРНЫЕ ФОРМЫ АЦЕТОУКСУСНОГО ЭФИРА:
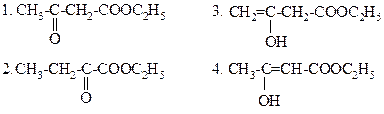 |
27.
ТАУТОМЕРНЫЕ ФОРМЫ ЩАВЕЛЕВОУКСУСНОЙ КИСЛОТЫ:
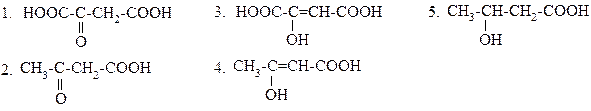
28.
ПРИ НАГРЕВАНИИ МОЛОЧНОЙ КИСЛОТЫ
С КОНЦЕНТРИРОВАННОЙ H2SO4 ОБРАЗУЮТСЯ:
 |
 29.
29.
В РЕЗУЛЬТАТЕ РЕАКЦИИ ОБРАЗУЕТСЯ:

30.
В РЕЗУЛЬТАТЕ ЩЕЛОЧНОГО ГИДРОЛИЗА γ-БУТИРОЛАКТОНА ОБРАЗУЕТСЯ:
 |
 31.
31.
ОСНОВНЫМ ПРОДУКТОМ РЕАКЦИИ ЯВЛЯЕТСЯ:
 |
32.
ПРИ НАГРЕВАНИИ α-ОКСИМАСЛЯНОЙ КИСЛОТЫ
С КОНЦЕНТРИРОВАНОЙ H2SO4 ОБРАЗУЮТСЯ:
 |
33.
В РЕЗУЛЬТАТЕ КИСЛОТНОГО (HCl) ГИДРОЛИЗА γ-БУТИРОЛАКТАМА
ОБРАЗУЕТСЯ:
 |
34.
ПРИ НАГРЕВАНИИ α-АМИНОПРОПИОНОВОЙ КИСЛОТЫ
В ПРИСУТСТВИИ Ba(OH)2 ОБРАЗУЕТСЯ:
1. метиламин 3. пропиламин 5. пропеновая кислота
2. этиламин 4. изопропиламин
35.
ПРИ НАГРЕВАНИИ α-ОКСИМАСЛЯНОЙ КИСЛОТЫ ОБРАЗУЕТСЯ:
 |
 36.
36.
В РЕЗУЛЬТАТЕ РЕАКЦИИ ОБРАЗУЕТСЯ:

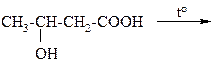 37.
37.
ОСНОВНЫМ ПРОДУКТОМ РЕАКЦИИ
ЯВЛЯЕТСЯ
 |
38.
К «КЕТОНОВЫМ ТЕЛАМ» ОТНОСЯТ:
1. ацетон 4. β-оксимасляную кислоту
2. ацетоуксусную кислоту 5. α-оксимасляную кислоту
3. щавелевоуксусную кислоту
39.
ДЛЯ КАЧЕСТВЕННОГО ОБНАРУЖЕНИЯ ВИННОЙ КИСЛОТЫ
ИСПОЛЬЗУЮТ РЕАКЦИИ С:
1. CaCl2 3. KOH 5. NaOH
2. Cu(OH)2 4. конц. H2SO4
40.
ПРОЕКЦИОННАЯ ФОРМУЛА МЕЗОВИННОЙ КИСЛОТЫ:
 |
41. РАЦЕМИЧЕСКАЯ СМЕСЬ – ЭТО:
1. смесь равных количеств энантиомеров
2. смесь равных количеств диастереомеров
3. оптически неактивный стереоизомер
4. смесь мезоформ
 42. КОЛИЧЕСТВО ХИРАЛЬНЫХ ЦЕНТРОВ
42. КОЛИЧЕСТВО ХИРАЛЬНЫХ ЦЕНТРОВ
В ДАННОЙ МОЛЕКУЛЕ:
1. один 3. три
2. два 4. четыре
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО (ЦИФРУ)!
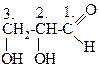 43.
43.
ХИРАЛЬНЫЙ ЦЕНТР МОЛЕКУЛЫ ОБОЗНАЧЕН ЦИФРОЙ
_______.
 44.
44.
СОЕДИНЕНИЕ СУЩЕСТВУЕТ В ВИДЕ
______ СТЕРЕОИЗОМЕРОВ.
45.
СТЕРЕОИЗОМЕРЫ, ПОХОЖИЕ КАК ПРЕДМЕТ И НЕСОВМЕСТИМОЕ С НИМ ЗЕРКАЛЬНОЕ ОТРАЖЕНИЕ, НАЗЫВАЮТСЯ __________________________ .
 46.
46.
В МОЛЕКУЛЕ ДАННОГО СОЕДИНЕНИЯ ______ ХИРАЛЬНЫХ ЦЕНТРА.
ЭТО СОЕДИНЕНИЕ СУЩЕСТВУЕТ В ВИДЕ ______ СТЕРЕОИЗОМЕРОВ.
УКАЖИТЕ СООТВЕТСТВИЯ!
 47.
47.
а) D-молочная кислота
б) L-молочная кислота
в) D-винная кислота
г) L-винная кислота
д) мезовинная кислота
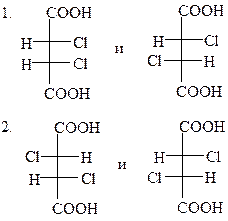 48.
48.
а) энантиомеры
б) диастереомеры
в) мезоформа
г) не являются стереоизомерами
Занятие № 10
ГЕТЕРОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ БЕНЗОЛЬНОГО РЯДА. БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ
ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
Мотивация цели.Гетерофункциональные соединения ароматического и гетероциклического рядов являются родоначальниками важнейших групп биологически активных соединений, в том числе лекарственных препаратов. На их основе получены жаропонижающие средства (ацетилсалициловая кислота, фенацетин, парацетамол, амидопирин), антибактериальные препараты (сульфаниламиды), анестетики и анальгетики (анестезин, новокаин, анальгин). Структурной основой многих витаминов, аминокислот, гормонов, антибиотиков, алкалоидов также являются гетерофункциональные производные бензольного и гетероциклического ряда.
Цель самоподготовки. Необходимо усвоить строение и свойства важнейших гетерофункциональных производных бензольного ряда и пятичленных гетероциклов, а также их значение для биологии и медицины.
План изучения темы
1. п-Аминофенол и его производные (Самостоятельная работа
№ 5).
2. п-Аминобензойная кислота и её производные (Самостоятельная работа № 6).
3. Сульфаниловая кислота и её производные.
3.1. Кислотно-основные свойства сульфаниловой кислоты.
3.2. Строение амида сульфаниловой кислоты. Общая структура сульфаниламидов.
3.3. Биологическая роль сульфаниламидов. Объяснение механизма их антимикробного действия.
4. Салициловая кислота и её производные. Объяснение повышенных кислотных свойств салициловой кислоты в сравнении с бензойной.
4.1. Получение лекарственных препаратов – салицилата натрия, метилсалицилата, фенилсалицилата, ацетилсалициловой кислоты. Их медицинское применение.
4.2. Определение доброкачествености ацетилсалициловой кислоты.
4.3. п-Аминосалициловая кислота – противотуберкулёзное средство.
5. Определение понятия «гетероциклические соединения». Классификация гетероциклов.
6. Общая характеристика реакционной способности пятичленных гетероциклов с одним гетероатомом.
6.1. Строение пиррола, фурана и тиофена. Их ароматичность. Понятие «π-избыточные системы».
6.2. Сравнение активности этих гетероциклов и бензола в реакциях электрофильного замещения. Ацидофобные свойства. Особенности реакций нитрования и сульфирования.
7. Пиррол и его производные.
7.1. Кислотно-основные свойства.
7.2. Реакции гидрирования пиррола. Основные свойства продуктов гидрирования.
7.3. Тетрапиррольные производные (порфин, гем). Их биологическая роль.
7.4. Индол (бензопиррол). Кислотно-основные свойства. Окислительное (до серотонина) и неокислительное (до триптамина) окисление триптофана.
8. Производные фурана.
8.1. Фурфурол. Свойства как альдегида.
8.2. Получение фурацилина (семикарбазона 5-нитрофурфурола) из фурфурола. Биологическое действие препаратов – производных
5-нитрофурана.
9. Общая характеристика реакционной способности пятичленных гетероциклов с двумя гетероатомами (азолов).
9.1. Строение пиразола, имидазола, тиазола. Их ароматичность.
9.2. Кислотно-основные свойства. Прототропная таутомерия пиразола и имидазола.
10. Биологически важные производные пиразолона-3(5). (Самостоятельная работа № 7).
11. Производные имидазола (гистидин, гистамин) и бензимидазола (дибазол).
12. Реакция гидрирования тиазола. Тиазолидин – структурный фрагмент пенициллинов.
Рекомендуемая литература
А - с. 271-297.
А* - с. 271-290
А** - с. 255-274.
Б – тема 2.2, обучающая задача 1 (с. 160-163), тема 2.3, обучающая задача 1 (с. 164-166).
Вопросы для самоконтроля(задания, обозначенные *, обязательны для выполнения в письменном виде)
1. Приведите строение биполярного иона сульфаниловой кислоты.
2. 
 Приведите общую структурную формулу сульфаниламидов и формулу норсульфазола.
Приведите общую структурную формулу сульфаниламидов и формулу норсульфазола.
4*. Приведите схемы реакций получения натрия салицилата, метилсалицилата, фенилсалицилата.
5. Приведите схему реакции получения ацетилсалициловой кислоты. Какая реакция может с ней протекать при хранении при повышенной влажности? Как проверяют доброкачественность ацетилсалициловой кислоты?
6*. Объясните, почему пиррол, порфин, имидазол, пиразол являются ароматическими соединениями. Сравните поведение имидазола и пиррола в присутствии конц. серной кислоты.
7. Приведите схемы реакций окислительного и неокислительного декарбоксилирования триптофана, декарбоксилирования гистидина.
Назовите полученные биогенные амины.
План работы на предстоящем занятии.
1. Разбор основных вопросов темы, выполнение упражнений.
2. Тестовый контроль.
3. Выполнение лабораторной работы:
- Гидролиз ацетилсалициловой кислоты.
4. Оформление лабораторного журнала, контроль выполнения лабораторной работы.
Лабораторная работа
|
из
5.00
|
Обсуждение в статье: Доказательство наличия двух карбоксильных групп в винной кислоте |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

