 |
Главная |
Основные определения и термины
|
из
5.00
|
Имея дело с растворами, удобно называть один из компонентов растворителем, а другие компоненты – растворенными веществами. Рассмотрим пример: при смешении хлорида натрия (твердое вещество) с водой получается жидкий раствор. Поэтому вода – растворитель, хлорид натрия – растворенное вещество.
Таким образом, растворителем называют компонент раствора, сохраняющий свое физическое состояние при образовании раствора. Если все компоненты раствора до перемешивания находятся в одинаковой фазе, растворителем называют тот компонент, который содержится в наибольшем количестве; остальные вещества называют растворенными веществами. Растворимость твердых веществ с повышением температуры большей частью увеличивается.
Под концентрацией понимают количество вещества, растворенного в заданном объеме раствора или растворителя. Концентрацию раствора можно охарактеризовать качественно и количественно. Для качественного описания концентрации используются такие понятия, как разбавленный, концентрированный, ненасыщенный, насыщенный и пересыщенный раствор.
Мерой растворимости вещества служит его концентрация его насыщенного раствора при данной температуре. Количественно растворимость принято выражать числом граммов вещества, которое при данной температуре можно растворить в 100 г растворителя. Это число называется коэффициентом растворимости или растворимостью вещества. Например, растворимость NaCl в воде при 20 оС составляет 36,0 г. Если при этой температуре в указанный раствор добавить еще некоторое количество NaCl, то добавленный избыток не растворится, а останется в виде осадка. Такой раствор называется насыщенным.
Раствор, содержащий растворимое вещество в меньшем количестве, чем его содержится в насыщенном растворе (меньше, чем его растворимость), называется ненасыщенным. Пересыщенный раствор – раствор, в котором растворено количество вещества больше, чем его растворимость.
О растворе с низкой концентрацией растворенного вещества принято говорить, как о разбавленном. Концентрированный раствор – раствор с высоким содержанием растворенного вещества.
Растворы характеризуются молярной концентрацией, молярной, массовой, объемной долей растворимого вещества.
В химических расчетах чаще всего применяется молярная концентрация. Молярную концентрацию раствора определяют как количество вещества, моль, растворенного в литре раствора:
 .
.  (3.1)
(3.1)
Единица молярной концентрации – моль/л.
Молярная доля компонента раствора определяется уравнением
 . (3.2)
. (3.2)
Массовая доля – отношение массы растворенного вещества к объему раствора. Математическое определение массовой доли компонента раствора дается уравнением
 . (3.3)
. (3.3)
Объемная доля – количество объемов растворенного вещества в 100 объемах раствора. Например, указано, что растворимость водорода равна 0,0125; это означает, что в 100 л раствора содержится 0,0125 л водорода, или 12,5 мл.
Единицы молярной, массовой, объемной доли – %, ‰, млн–1.
Для обозначения молярной доли раствора обычно используется символ Х с индексом, указывающим компонент, о котором идет речь. Например, молярная доля НСl в растворе соляной кислоты записывается как ХНС1. Сумма молярных долей всех компонентов раствора должна быть равна единице.
Моляльность определяется как количество растворенного вещества в килограмме растворителя.
 . (3.4)
. (3.4)
Единица моляльности – моль/кг.
Иногда концентрацию раствора выражают через его плотность. Определенной плотности раствора чистого вещества при данной температуре соответствует определенное (известное) содержание вещества в нем. Например, раствор серной кислоты пл. 1,170 г/см3 при 20 оС содержит 24 % H2SO4. для определения концентрации раствора по его плотности пользуются справочными таблицами (прил. 1).
Зная плотность раствора, по справочнику находят долю растворенного вещества в нем. Вычисляют концентрацию раствора.
Для перехода от массы к объему можно воспользоваться формулой
V = m / d , (3.6)
где V, m , d – соответственно объем, масса и плотность.
Вопросы для самостоятельной подготовки и контроля
1. Что такое растворитель? Растворенное вещество?
2. Как меняется растворимость большинства твердых веществ с повышением температуры?
3. Какие растворы называются насыщенными, ненасыщенными и пересыщенными?
4. Объясните, какие растворы называют разбавленными и концентрированными.
5. Что такое концентрация раствора? Как можно выразить концентрацию раствора?
6. Дайте определение массовой и объемной доли. Чем отличается массовая доля от объемной?
7. Какие растворы называются молярными?
8. Что означает молярная доля компонента раствора и как она определяется?
9. Что называется плотностью раствора? В каких единицах выражается плотность раствора?
10. Одинакова ли плотность растворов соляной кислоты различной концентрации?
11. Как, зная плотность раствора, определить долю вещества в нем?
Решение типовых задач
Задача 1.В 80 г воды растворено 4 г соли. Определить массу, г, в 100 г раствора и растворимость этой соли.
Решение. Находим массу раствора: 80+4=84 г.
1. Определение массы соли в 100 г раствора:
| в 84 г содержится 4 г соли в 100 « х « | 
|
2. Определение растворимости соли в 100 г раствора:
| 80 г воды растворяют 4 г соли 100 г « х « | 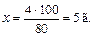
|
Задача 2.Вычислить массу и моляльность водного раствора H2SO4, плотность которого при 20 оС равна 1,303 г/см3.
Решение. По справочной таблице (прил. 1) находим, что такой раствор содержит 40 % H2SO4; литр этого раствора весит 1303 г. Для вычисления массы H2SO4 составляем пропорцию:
| 100 г раствора содержат 40 г H2SO4 1303 г « х | 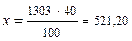 г. г.
|
Для вычисления моляльности раствора нужно вычислить число граммов H2SO4 в 1000 г воды (растворителя). Поскольку дан 40 %-й раствор, 40 г H2SO4 содержится в 60 г воды. Отсюда составляем пропорцию:
| 60 г воды содержат 40 г H2SO4 1000 г « х | 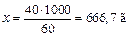 . .
|
Так как 1 моль H2SO4 равен 98 г и в 1000 г (1 кг) раствора содержится 666,7 г H2SO4, то моляльность раствора: 666,7/98=6,8 моль/кг.
Задача 3. В 250 мл раствора гидроксида кальция содержится 3,705 г Са(ОН)2. Вычислить молярную концентрацию этого раствора.
Решение. Сначала вычислим, сколько граммов содержится
в 1000 мл раствора. Составим пропорцию:
| 3,075 г Са(ОН)2 содержится в 250 мл х Са(ОН)2 « 1000 мл |  г. г.
|
Молярную концентрацию определяем из следующего соотношения:
| 74,10 г/л – 1 моль 14,82 г/л – х |  моль/л. моль/л.
|
Задача 4.Вычислите молярную долю HCl в растворе с массовой долей HCl 36%.
Решение. Допустим, что имеется 100 г раствора. Тогда в растворе должно содержаться 36 г HCl и 64 г Н2О.
| 1 л раствора концентрации 1 моль/л содержит 36,5 г HCl х « 36 г HCl |  . .
|
| Масса 1 моль воды раствора 18 г х « 64 г |  моль/л. моль/л.
|
Молярная доля, %, вычисляется по формуле (3.5)
ХНС1= 
|
из
5.00
|
Обсуждение в статье: Основные определения и термины |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

