 |
Главная |
Модели идеализированных реакторов
|
из
5.00
|
Математическая модель – это система уравнений, которая устанавливает взаимосвязь между входными и выходными параметрами реактора. Математическая модель реактора должна содержать минимальное количество уравнений при сохранении качественных и количественных характеристик реактора. Математическую модель реактора рассматривают по четырём уровням:
1. Молекулярный уровень. Рассматривается межмолекулярное взаимодействие, определяемое закономерностями химической кинетики, учитываются стехиометрические соотношения и законы равновесия.
2. Уровень малого объёма. Рассматривается зерно катализатора, единичный элемент насадки и т.д. На этом уровне ранее определённые закономерности дополняются законами тепло- и массопереноса.
3. Уровень рабочей зоны реактора. Рабочую зону реактора представляют как совокупность элементов малого объёма, поэтому в математическую модель добавляют описание характера движения потоков реагентов.
4. Уровень реактора, включающего несколько рабочих зон.
Таким образом, математическая модель рабочей зоны реактора или реактора, состоящего из одной рабочей зоны, должна содержать четыре уравнения:
1. Уравнение материального баланса.
2. Уравнение теплового баланса.
3. Кинетическое уравнение (или уравнения, если в реакторе протекает несколько реакций).
4. Уравнение, описывающее гидродинамическую обстановку в реакторе.
Для упрощения математической модели вводят допущения, которые существенно упрощают математический аппарат, при этом не изменяют сущность рассматриваемого объекта. Применительно к химическому реактору, наибольшую сложность представляют уравнения, описывающие гидродинамическую обстановку в реакторе. Поэтому были созданы модели идеализированных реакторов, в которых характер движения реагентов ограничивается двумя режимами:: полного смешения и идеального вытеснения.
При рассмотрении модели полного смешения устанавливаются следующие допущения:
1. Значения параметра во всех точках реакционного объёма одинаково.
2. Значение параметра на выходе из реактора равно значению параметра в объёме реактора.
3. Изменение значения параметра начального до конечного значения происходит за нулевой промежуток времени. Диапазон изменения параметра определяется объёмом реактора (Рисунок 6.1).
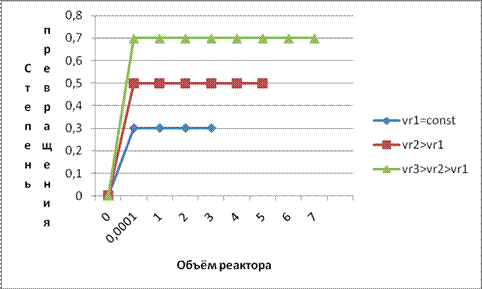
Рисунок 6.1. Изменение степени превращения в РПС при разном объёме реактора.
По модели полного смешения могут рассматриваться как проточные реактора, так и реактора периодического действия.
Модель идеального вытеснения предполагает, что реактор представляет собой вытянутый канал, то есть один из геометрических размеров которого (длина или высота) много больше другого геометрического размера (диаметра): L>>D или H>>D. Модель идеального вытеснения предполагает «поршневой» режим движения реагентов. То есть поток реагентов можно разбить на N слоёв бесконечно малой длины, каждый из которых продвигается в направлении от входа в реактор к выходу, выталкивая впереди идущий слой. Таким образом, в модели идеального вытеснения запрещено перемешивание в направлении оси потока, но разрешено радиальное перемешивание. В отличие от модели полного смешения, в реакторе идеального вытеснения (РИВ) изменение всех параметров происходит плавно по длине реактора (Рисунок 6.2). По модели РИВ могут рассматриваться только проточные реактора.
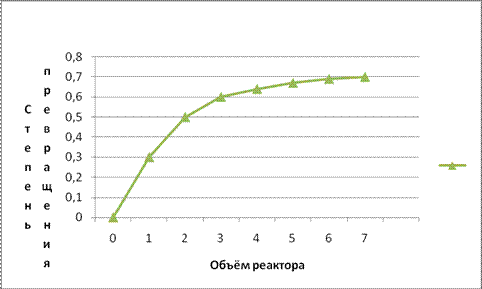
Рисунок 6.2.Изменение степени превращения в РИВ.
Для составления математической модели необходимо выбирать элементарный объём и элементарный промежуток времени.
Элементарный объём – это объём, выделяемый внутри реактора, в пределах которого можно пренебречь неравномерностью распределения концентраций и температуры. Элементарный объём неподвижен относительно стенок реактора и бесконечно мал во всех измерениях.
Элементарный промежуток времени - это промежуток времени, в течение которого можно пренебречь неравномерность распределения концентраций и температур в границах элементарного объёма.
Если в реакторе протекает модельная реакция
aA+bB=cC+dD (6.1)
изменение количества вещества А в границах элементарного объёма может происходить по трём причинам:
1. Конвективный перенос, вызванный движением потока со скоростью w за счёт какого-либо внешнего воздействия.
2. Диффузионный перенос, обусловленный неравномерностью распределения вещества А в пространстве. Вследствие выравнивания концентраций происходит изменение количества вещества А в границах элементарного объёма.
3. Расход или образование вещества А в результате химического превращения, пропорциональный скорости реакции.
Таким образом, накопление или убыль вещества в границах элементарного объёма есть сумма трёх слагаемых: конвективной составляющей, диффузионной составляющей и химической реакции. В стационарных условиях накопление или убыль вещества равны нулю.
Согласно уравнению (4.2.3) в стационарных условиях уравнение теплового баланса для элементарного объёма можно представить:
dQ01 ± dQх.р ± dQт.о - dQ02 ± dQф.п - dQп = 0 (6.2)
Если пренебречь величинами тепловых потерь и теплотой фазовых превращений, можно записать:
dQ01 ± dQх.р ± dQт.о - dQ02 = 0 (6.3)
Следовательно, можно выделить три температурных режима:
1. Изотермический режим, характеризующийся постоянством температуры во всех точках реактора. То есть вся теплота, выделяющаяся или поглощаемая в результате реакции полностью компенсируется за счёт использования теплообменных устройств.
dQ01 = dQ02 , dQх.р = dQт.о , Т=const (6.4)
2. Адиабатический режим, характеризующийся отсутствием теплообмена с окружающей средой. Вся теплота выделяющаяся (поглощаемая) в результате реакции идёт на разогрев (охлаждение) реакционной смеси.
dQ01 ± dQх.р - dQ02 = 0 (6.5)
3. Политермический режим (режим с частичной компенсацией теплового эффекта). Тепловой баланс описывается уравнением (6.3).
Таким образом, математическая модель РПС в изотермическом температурном режиме выглядит следующим образом.
t=ZNA*XA/(U*S) (6.6)
где: t - время контакта (с), численно равное отношению объёма реактора и расхода реакционной смеси.
t=Vr/Vc (6.7)
ZNA- мольная доля ключевого компонента в исходной смеси,
XA- степень превращения ключевого компонента,
S- множитель, величина которого определяется размерностью скорости реакции. Если размерность скорости кмоль/(м3*с), то S=22,4; если размерность скорости моль/(м3*с), то S=22,4*10-3; если размерность скорости м3/(м3*с), то S=1.
Окончательно математическая модель в изотермическом температурном режиме выглядит:
Vr= Vc*ZNA*XA/(U*S) (6,8)
Математическая модель РИВ в изотермическом температурном режиме:
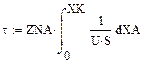 (6.9)
(6.9)
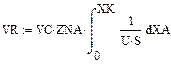 (6.10)
(6.10)
В адиабатическом температурном режиме тепловой баланс реактора независимо от вида идеализированной модели имеет вид
T=T0+L*XA (6.11)
Где:
Т0- температура смеси на входе в реактор,
L – адиабатический коэффициент, максимальное изменение температуры реакционной смеси при полном превращении ключевого компонента.
L=ZNA*q /cp (6.12)
Где:
q- удельный тепловой эффект химической реакции.
ср - средняя изобарная теплоёмкость реакционной смеси при температуре 298 К.
Для модельной реакции (6.1) удельный тепловой эффект рассчитывается:
q=-∆H0/a (6.13)
cp=cpa*ZNA+cpb*ZNB+….+cpi*ZNI (6.14)
Тогда математические модели для реакторов в адиабатическом температурном режиме будут выглядеть следующим образом:
Для РПС
t=ZNA*XA/(U*S)
T=T0+L*XA (6.15)
Для РИВ
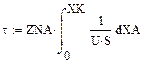
T=T0+L*XA (6.16)
Пример 1
Рассчитать объём реактора полного смешения в изотермическом температурном режиме и производительность по хлору при проведении реакции окисления газообразного хлороводорода кислородом воздуха при следующих исходных данных:
-состав исходной смеси (мольные доли): хлороводород – 0,25, остальное – воздух.
-кинетическое уравнение:
U=k+*(PHCl/PH2O)*(PO2/PCl2)0,75-k-*(PCL2)0,75*PH2O0,5)/PHCl2
-кинетические параметры: k0+=982 моль HCl/(м3*с),
Е+=19800 дж/моль, k0-=1,13*105 моль HCl/(м3*с),
Е+=46500 дж/моль,
-Давление 0,1 МПа, температура 500 К, степень превращения хлороводорода 0,6, расход исходной газовой смеси 30000 м3/ч.
Решение:
Рассчитаем начальную мольную долю кислорода в исходной смеси:
ZNO2=(1-ZNHCl)*0,21 ZNO2=(1-0,25)*0,21=0,158
Рассчитаем мольные доли компонентов реакционной смеси при степени превращения хлороводорода:
W=1-0,25*ZNHCl*XHCl W=1-0,25*0,25*0,6=0,963
ZHCl=ZNHCL*(1-XHCl)/W ZHCl=0,25*(1-0,6)/0,969=0,104
ZO2=(ZNO2-0,25*ZNHCl* XHCl)/W
ZO2=(0,158-0,25*0,25*0,6)/0,963=0,125
ZCl2=(ZNCL2+0,5* ZNHCl* XHCl)/W
ZCl2=(0+0,5*0,25*0,6)/0,963=0,078
ZH2O=(ZNH2O+0,5* ZNHCl* XHCl)/W
ZH2O=(0+0,5*0,25*0,6)/0,963=0,078
Определим величину скорости процесса при заданных условиях:
k+=982*exp(-19800/(8,31*500))=8,36 моль HCl/(м3*с),
k-=1,13*105*exp(-46500/(8,31*500))=1,56 моль HCl/(м3*с),
При давлении 0,1 МПа (1атм), величины парциальных давлений компонентов численно равны мольным долям соответствующих компонентов.
U=8,36*(0,104/0,078)*(0,125/0,078)0,75-1,56*0,0780,75*0,0780,5/0,1042
U=9,93 моль HCl/(м3*с)
Объём реактора:
Vp=30000/3600*0,25*0,5/(9,93*22,4*10^-3)=5,62 м3.
Производительность по хлору:
VCl2=Vc*( ZCl2- ZNCl2)
VCl2=30000/3600*(0,078-0)=0,65 м3/с
Пример 2.
Рассчитать величину адиабатического коэффициента при проведении реакции окисления диоксида серы и температуру реакционной смеси на выходе из реактора, если:
-степень превращения диоксида серы 0,8;
-температура реакционной смеси на входе в реактор 600 К;
-состав исходной смеси (мольные доли): диоксид серы 0,11, кислород 0,09, триоксид серы 0,01, остальное – азот.
Решение:
Вычисляем тепловой эффект реакции окисления диоксида серы при температуре 298 К.
2SO2+O2=2SO3
∆H0=2*∆H0(SO3)-2*∆H0(SO2)- ∆H0(O2)
∆H0=2*(-395,86)-2*(-296,9)-2*0=-197,9 КДж
Удельный тепловой эффект:
q=-∆H0/2
q=-(-197,9)/2=98,96 КДж/моль
Средняя изобарная теплоёмкость исходной реакционной смеси при температуре 298 К:
cp=cpSO2*ZNSO2+ cpO2*ZNO2+ cpSO3*ZNSO3+ cpN2*ZNN2
ср= 39,87*0,11+29,37*0,09+50,09*0,01+29,12*(1-0,11-0,09-0,01)
cp=30,53 Дж/(моль*К)
Адиабатический коэффициент
L=q*ZNSO2/cp
L=98960*0,11/30,53=356,6 K
Температура реакционной смеси на выходе из реактора:
T=T0+L*XSO2
T=600+356,6*0,8=885 K
Пример 3.
|
из
5.00
|
Обсуждение в статье: Модели идеализированных реакторов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

