 |
Главная |
Мономолекулярное нуклеофильное замещение
|
из
5.00
|
Третичные алкилгалогениды реагируют по механизму SN1 (мономолекулярное нуклеофильное замещение).
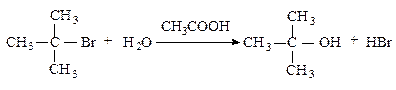
Cтадии процесса.Реакция протекает в две стадии. Первая стадия - гетеролитический разрыв связи углерод-галоген - медленная.
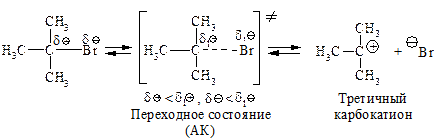
Вторая стадия - образовавшийся карбокатион практически мгновенно взаимодействует с нуклеофилом - молекулой воды.

В отличие от механизма SN2, разрыв связи С–Х и образование новой связи С–Nu протекает не одновременно, а последовательно.
Электрофильный катализ. Соли тяжелых металлов, в частности, серебра, ртути, меди катализируют SN1-реакции. Функция иона тяжелого металла состоит в образовании комплекса за счет неподеленных электронов галогена, вследствие чего уходящей группой становится галогенид металла, а не галогенид-анион.
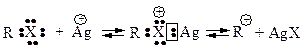
Энергетическая диаграмма реакцииизображает изменение потенциальной энергии в ходе двухстадийного мономолекулярного замещения (рис.11.4).

Рис. 11.4. График изменения потенциальной энергии в ходе
мономолекулярного нуклеофильного замещения. SN1-двухстадийный процесс
Скорость реакции.В медленной стадии, определяющей скорость реакции, принимает участие только одна молекула, поэтому механизм называют мономолекулярным замещением. Скорость реакции зависит только от концентрации галогеналкана и определяется по формуле v= k[R-Hal].
Концентрация нуклеофильного реагента. Скорость реакции не должна зависеть от концентрации нуклеофила.
Перегруппировка.В медленной стадии реакции образуется карбокатион - частица, способная к перегруппировке. Галогеналканы могут реагировать по механизму SN1 через стадию перегруппировки первоначально образующегося карбокатиона: если в результате 1,2-сдвига отрицательно заряженной частицы образуется более устойчивый карбокатион, то происходит перегруппировка.
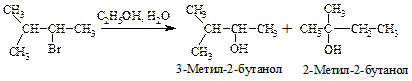
Механизм перегруппировки.
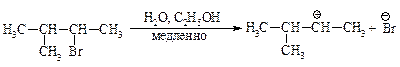


Перегруппировка считается признаком SN1-механизма.
Растворитель. Переходное состояние SN1-реакции более полярно, чем исходное состояние. Увеличение полярности растворителя способствует усилению сольватации переходного состояния по сравнению с сольватацией исходного соединения. Это приводит к росту скорости реакции (рис. 11.5).
При проведении SN1-реакции используют протонные растворители с высокой диэлектрической проницаемостью, способные образовывать водородные связи. Водородная связь возникает за счёт электростатического притяжения между электроотрицательным атомом одной молекулы и атомом водорода другой молекулы, который связан с электроотрицательным атомом, оттягивающим на себя электронное облако и оставляющим открытым ядро водорода. Атом водорода служит мостиком между двумя электроотрицательными атомами, причём с одним из них он связан ковалентной связью, а с другим – электростатическими силами притяжения.
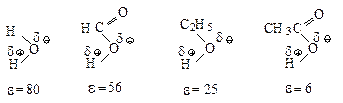
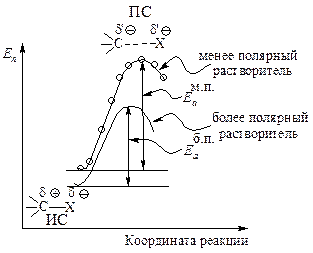
Рис. 11.5. Влияние полярности растворителя на скорость реакции
|
из
5.00
|
Обсуждение в статье: Мономолекулярное нуклеофильное замещение |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

