 |
Главная |
Обратимость в ГМФК силанолов
|
из
5.00
|
Граббом и Лясоцким с соавторами установлено, что ГМФК R2Si(OH)2 в среде метанола является обратимым процессом , , Ошибка! Закладка не определена. скорость которого описывается уравнением:
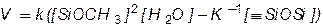
где 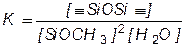
Однако это уравнение справедливо только до 50% конверсии мономера, так как далее скорость процесса резко падает из-за уменьшения реакционной способности олигосилоксандиолов.
Для кислотно катализируемой ГМФК Me2Si(OH)2 К= 17.5 (25оС). В случае основного катализа для замещенных метилфенилсиландиолов значение константы равновесия находится в интерва
ле 40 ¸ 54 (25оС) и очень мало зависит от природы заместителей Ошибка! Закладка не определена.. Показано, что константа равновесия не зависит от начальных концентраций компонентов реакционной системы Ошибка! Закладка не определена..
В случае проведения ГМФК R2Si(OH)2 в среде диоксана процесс является неравновесным, протекающим до конца. Однако при этом не указывается критерий установления равновесия. Выдвигается предположение, что неравновесный характер ГМФК R2Si(OH)2 в среде диоксана обусловлен повышенной основностью силанолов в сравнении с образующимися олигосилоксандиолами. Причиной увеличения основности силанолов может быть специфическая их сольватация диоксаном.
ГМФК триорганосиланолов в водно—диоксановом растворе, катализируемая HCl является равновесным процессом. Так константа равновесия Me3SiOH в присутствии HCl равна 130 ± 10 независимо от способа достижения равновесного состояния . В отличие от ГМФК R2Si(OH)2 в среде метанола (с КОН) значения констант равновесия для органодиметилсиланолов сильно зависят от природы заместителей у атома кремния.Для арилсиланолов характерны низкие значения К (2 ¸ 7), для галоидзамещенных силанолов проявляется сильное влияние галоида на К (ClCH2 - 24, BrCH2 - 86). На основе значений констант равновесия и констант скорости прямых реакции были рассчитаны константы обратных реакций ( расщепления ºSiOSiº ), которые проверены для ряда соединений экспериментально. Расчет констант расщепления силоксанов проведен в предположении, что скорость расщепления органосилоксана зависит от концентрации воды в первой степени, хотя это и не доказано:
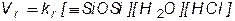
Оказалось, что корреляция констант расщепления силоксанов (kr) с индукционными и стерическим характеристиками заместителей практически не соблюдается ни в кислотном, ни в основном катализе. Не наблюдается корреляция и с данными по основности гексаорганодисилоксанов. Авторы отмечают, что все же просматривается тенденция уменьшения kr с увеличением электроноакцепторных и стерических свойств заместителей. Предполагается, что относительный суммарный вклад индукционного и стерического
влияния заместителей различен в прямой и обратной реакциях. Отмечается также, что стадия депротонирования является быстрой, вероятно вследствие низкой основности серединного атома кислорода.
Здесь необходимо отметить, что по данным Воронкова и Жагаты кислотный гидролиз гексаорганодисилоксанов является реакцией второго порядка по воде . На основании этого авторы предполагают, что гидролитическое расщепление связи ºSiOSiº протекает через промежуточный шестичленный активный комплекс, содержащий две молекулы воды, одна из которых протонирована:
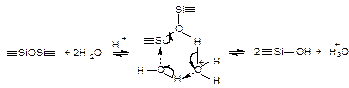
Время установления равновесия сокращается с увеличением концентрации катализатора.Аналогичный механизм предлагается и для расщепления силоксанов протонными кислотами . Эта схема интересна и с той точки зрения, что она представляет альтернативный схеме 2 маршрут или механизм конденсации силанолов. Конкуренция двух механизмов химической сборки олигоорганосилоксанов может быть причиной наблюдаемых концентрационных колебаний органосиланолов. В этой связи можно предположить также, что отсутствие корреляции константы расщепления гексаорганодисилоксанов kr в исследованиях немецких ученых обусловлено, тем, что расщепление связи ºSiOSiº протекает не только по схеме 2, но и по уравнению 2.6,.
В заключение раздела необходимо отметить, что проблема обратимости ГМФК является сложной (впрочем, как и обратимости реакции гидролиза органохлорсиланов). Можно предположить, что наличие в равновесной смеси как исходных, так и конечных продуктов реакции реализуется в результате не одной обратимой реакции, а двух или более, протекающих по разным механизмам. Возможно проблема обратимости химических стадий в процессе гидролитической поликонденсации органохлорсиланов является одной из важнейших проблем, возникающих при исследовании ГПК органохлорсиланов.
|
из
5.00
|
Обсуждение в статье: Обратимость в ГМФК силанолов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

