 |
Главная |
Дифференциального кинетического уравнения
|
из
5.00
|
Определим константы дифференциального кинетического уравнения для следующей реакции:
аА + bB → продукты.
Зависимость скорости от концентраций выражается уравнением (4.3):
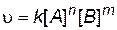 .
.
Прологарифмируем это выражение
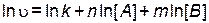 . .
| (4.4) |
Так как величины k, n и m для рассматриваемой реакции (при T=const) являются постоянными и не зависят от концентрации реагентов, то для их нахождения достаточно определить зависимость скорости реакции от концентрации одного из реагентов при фиксированной концентрации другого реагента.
Пусть в трех опытах концентрация вещества А будет постоянной и равной [A]0.
Тогда в уравнении (4.4) сумма ( 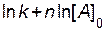 ) будет тоже величиной постоянной.
) будет тоже величиной постоянной.
Обозначим ее 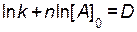 .
.
Тогда уравнение (4.4) можно переписать как
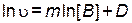 . .
| (4.5) |
Зависимость (4.5) представляет собой в координатах ln[B] – 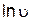 уравнение прямой линии, тангенс угла наклона которой к оси абсцисс численно равен порядку реакции по веществу В.
уравнение прямой линии, тангенс угла наклона которой к оси абсцисс численно равен порядку реакции по веществу В.
По экспериментальным данным строят график зависимости 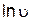 от ln[B] (рис. 4.2) и находят порядок реакции по веществу B
от ln[B] (рис. 4.2) и находят порядок реакции по веществу B
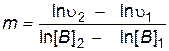 .
.
В последующих опытах определяют скорость реакции при различных исходных концентрациях вещества А и постоянной концентрации [B]0.
Находят порядок реакции по веществу А
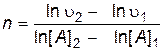 .
.
Из уравнения (4.3) с учетом найденных порядков реакции по веществам А и В рассчитывают константу скорости
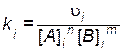 ,
,
где 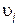 , [A]i, [B]i – экспериментальные данные, относящиеся к одному опыту.
, [A]i, [B]i – экспериментальные данные, относящиеся к одному опыту.
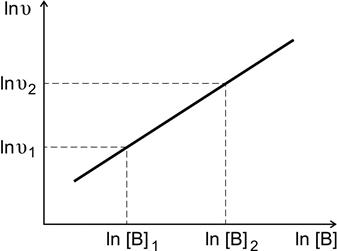
Рис. 4.2. Определение порядка реакции по веществу В
Зависимость концентрации реагирующих веществ
От времени для реакции первого порядка.
Интегральное кинетическое уравнение
На практике чаще всего интересует не само значение скорости химической реакции, а то, сколько вещества израсходовано или образовалось к определенному моменту времени после начала реакции.
Рассмотрим эту задачу на примере реакции первого порядка:
А ® продукты.
Скорость такой реакции выражается следующим уравнением:
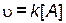 . .
| (4.6) |
В дифференциальном виде
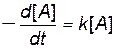 . .
| (4.7) |
Перепишем это уравнение в следующем виде:
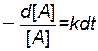
и возьмем определенный интеграл от обеих частей уравнения от исходного состояния ([A]0, t0 = 0) до текущего момента ([A]t, t):

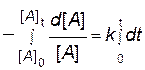 .
.
Решение этого уравнения приводит к следующей зависимости:
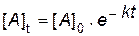
| (4.8) |
или
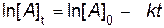 . .
| (4.9) |
Соотношения (4.8) и (4.9) являются интегральными кинетическими уравнениями реакции первого порядка.
Зная исходную концентрацию вещества [A]0 и константу скорости реакции k, можно рассчитать концентрацию [A]t через любое время t после начала реакции.
Если же известны исходная концентрация [A]0 и концентрация реагирующего вещества [A]t через какое-то время t после начала реакции, то можно рассчитать константу скорости этой реакции
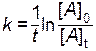 . .
| (4.10) |
|
из
5.00
|
Обсуждение в статье: Дифференциального кинетического уравнения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

