 |
Главная |
Относительная реакционная способность алкенов по отношению к реакции бромирования
|
из
5.00
|
(растворитель – метанол)
| Соединение | Н2С=СН2 | СН3СН2СН=СН2 | цис-СН3СН2СН=СНСН3 | (СН3)2С=С(СН3)2 |
| Относительная скорость реакции | 103 | 105 | 107 |
v Радикальное галогенирование. При радикальном присоединении брома к алкенам (механизм АR) на стадии инициирования молекула галогена распадается на атомы.

Далее свободные радикалы гомолитически разрывают p-связь, присоединяясь к одному из атомов углерода двойной связи. Реакция преимущественно протекает через более стабильный радикал. Например, вторичный алкильный радикал (1) более устойчив, чем первичный радикал (2). Дальнейшее взаимодействие с молекулой галогена дает продукт присоединения и генерируется новый радикал.

Активность галогенов в реакциях радикального присоединения к алканам снижается в ряду Cl2 > Br2 > I2. Особенно инертен в этих реакциях иод из-за низкой его активности в атомарном состоянии.
8.5.3. Механизмы реакции электрофильного присоединения*
v Механизм АЕ. Прежде чем познакомиться с другими реакциями присоединения к алкенам, следует рассмотреть механизм, который реализуется в большинстве таких реакций. Полагают, что присоединение кислого реагента HZ включает стадию образования карбкатиона и происходит в две стадии.
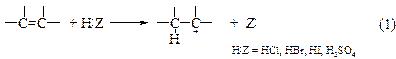

Стадия (1) заключается в переносе протона к алкену с образованием карбкатиона; это переход протона от одного основания к другому:

Эта стадия протекает медленно и ее скорость в значительной степени или полностью определяет общую скорость присоединения. Т. к. протон – типичный электрофильный реагент, то и реакцию называют электрофильным присоединением. Соответственно механизм реакции обозначают как АЕ или AdE (А – от англ. addition – присоединение, Е – электрофил).
Далее карбкатион может присоединять отрицательный ион с образованием галогенида, гидросульфата, спирта и т. п. При этом электронодефицитный атом углерода получает пару электронов. Вторая стадия в большинстве случаев – это ионная реакция, она протекает практически мгновенно.
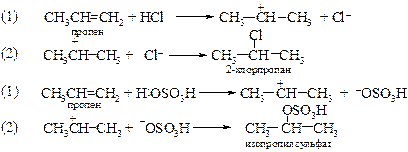

v Другие механизмы реакций присоединения. Для присоединения биполярных молекул Xd+Yd- возможно протекания реакции через циклический катион.

У ранее рассмотренных процессов присоединения молекул типа HZ такой механизм не может реализоваться, так как атом водорода не имеет свободной электронной пары, за счет которой происходит циклизация.
§ Третий возможный механизм присоединения AЕ3, включает согласованное взаимодействие алкена и двух молекул реагента. Реакция протекает через шестицентровое переходное состояние.

|
из
5.00
|
Обсуждение в статье: Относительная реакционная способность алкенов по отношению к реакции бромирования |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

