 |
Главная |
Строение гидроксильной группы
|
из
5.00
|
Выполнение упражнений.
2Дайте названия по систематической номенклатуре:
| а) | СН3 | — | СН2 | — | СН | — | СН3 | б) | С2Н5 | — | СН | (ОН) | — | С2Н5 | в) | СН2 | — | СН2 | — | СН2 | — | СН3 | ||
| | | | | |||||||||||||||||||||||
| ОН | НО | |||||||||||||||||||||||
| г) | СН3 | — | СН | — | СН2 | — | СН | — | СН3 | д) | Br | — | CH | = | CH | — | CH | = | С | — | CH2 | ОН | ||
| | | | | | | ||||||||||||||||||||||
| СН3 | ОН | СF3 | ||||||||||||||||||||||
| е) | СН2 | — | СН | — | СН | = СН | ж) | С6Н5 | — | СН | — | СН | = | СН | ||||||||||
| | | | | | | | | | | ||||||||||||||||||||
| Cl | OH | Cl | ОН | Cl |
3.1. Напишите формулы веществ:
а) 3-этилпентанол-3; в) 1,4-дибромобутен-3-ол-2;
б) 3-бром-2-метилпентадиен-2,4-ол-1; г) 2-фенил-3-хлоропропен-2-ол-1.
3.2. Напишите формулы изомерных спиртов состава С5Н11ОН и назовите их.
3.3. С какими из перечисленных веществ реагирует этиловый спирт: водород, гидроксид натрия, кислород, калий, медь, оксид кальция, хлороводород? Напишите уравнения соответствующих реакций и укажите условия их протекания.
3.4. Напишите уравнения реакций с помощью которых можно осуществить превращения:
а) С2Н4→А → В → С2Н5–О–С2Н5
б) С2Н5ОН → С2Н4 → С2Н5Сl → С2Н5ОН
в) С2Н4 → С2Н5ОН → СН2=СН–СН=СН2
г) СН4 → С2Н2 → С2Н4 → С2Н5ОН
ж) этан →хлорэтан → этен → этанол → диэтиловый эфир;
з) карбон (II) оксид → метанол → хлорметан → этан → карбон (IV) оксид;
4. Решение задач
4.1 Какой объем этана можно получить из этанола массой 92 г?
4.2 Найти молекулярную формулу вещества, при полном сгорании 13,8 г которого получилось 26,4 г углекислого газа и 16,2 г воды. Плотность пара этого вещества по водороду равна 23.
Программа саморазвития
1. Заполните пропуски:
а) изомером этанола является ______;
б) пропанол не образует третичных спиртов, потому что ___________;
в) 2,2-диметилбутанол-1 является изомером ________;
г) кислотно-основные свойства спиртов обусловлены наличием ______;
д) в ряду 2-хлорэтанол-1; 2,2-дихлорэтанол-1; 2,2,2-трихлорэтанол-1 кислотные свойства (усиливаются или ослабевают), потому, что _____;
е) натрия металят имеет формулу ______. Его можно получить при взаимодействии ________ с ________ ;
ж) вода разлагает алкоголяты потому, что она ________, чем спирты;
з) гидролизный спирт получают из _____;
и) метилпропиловый эфир получают из _______ .
2. При нагревании галогенпроизводных алканов с водными растворами щелочей образуются спирты. Напишите уравнения реакций получения спиртов из иодметана, хлорэтана и бромпропана. Укажите роль щелочей в данных химических реакциях
3. Напишите уравнения реакций с помощью которых можно осуществить превращения:
д) С2Н5–О–С2Н5ã äСН2=СН–СН=СН2
С2Н4 ÙС2Н5ОНÚ С2Н5ONа
СН3СНОå æС2Н5Сl
е) СН3–СНО ↔ С2Н5ОН ↔ С2Н5Сl ↔ С2Н4
и) метан → этан → этен → этанол → карбон (IV) оксид;
Дополнительные(высокий уровень)
ж) С2Н4  А
А  В
В  С
С  D;
D;
з) пропанол–1 → А → В → 2,3–диметилбутан.
4. Решить задачи
4.1 При сжигании 2,3 г вещества было получено 4,4 г углекислого газа и 2,7 г воды. Плотность газа по воздуху составляет 1,59. Найти молекулярную формулу вещества.
Дополнительная(высокий уровень)
4.2 Натрий массой 12г поместили в этанол объемом 23 мл и плотностью 0,8г/мл. Массовая доля воды в этаноле составляла 5%. Какой объем водорода выделился?
Конспект
ГИДРОКСИСОЕДИНЕНИЯ
К органическим гидроксисоединениям относятся вещества, содержащие одну или более гидроксильных групп –ОН, связанных с углеводородным радикалом.
В зависимости от характера углеводородного радикала эти соединения подразделяют на две большие группы:
· спирты R–OH
· фенолы Ar–OH,
где R – алкил (алифатический углеводородный радикал);
Ar – арил(ароматический радикал, свободная валентность которого принадлежит атому углерода бензольного кольца, например, радикал фенил C6H5–).
Радикал бензил C6H5–CH2– является арилалкилом (свободная валентность находится при насыщенном атоме углерода), поэтому соединение C6H5–CH2–ОН относится к спиртам.
Классификация спиртов
Спирты классифицируют по различным структурным признакам.
1. По числу гидроксильных групп спирты подразделяются на
o одноатомные (одна группа -ОН),
o многоатомные (две и более групп -ОН).
Современное название многоатомных спиртов - полиолы (диолы, триолы и т.д). Примеры:
o двухатомный спирт – этиленгликоль (этандиол)
HO–СH2–CH2–OH
o трехатомный спирт – глицерин (пропантриол-1,2,3)
HO–СH2–СН(ОН)–CH2–OH
Двухатомные спирты с двумя ОН-группами при одном и том же атоме углерода R–CH(OH)2 неустойчивы и, отщепляя воду, сразу же превращаются в альдегиды R–CH=O. Спирты R–C(OH)3 не существуют.
2. В зависимости от того, с каким атомом углерода (первичным, вторичным или третичным) связана гидроксигруппа, различают спирты
o первичные R–CH2–OH,
o вторичные R2CH–OH,
o третичные R3C–OH.
Например:

В многоатомных спиртах различают первично-, вторично- и третичноспиртовые группы. Например, молекула трехатомного спирта глицерина содержит две первичноспиртовые (HO–СH2–) и одну вторичноспиртовую (–СН(ОН)–) группы.
3. По строению радикалов, связанных с атомом кислорода, спирты подразделяются на
o предельные, или алканолы (например, СH3CH2–OH)
o непредельные, или алкенолы (CH2=CH–CH2–OH)
o ароматические (C6H5CH2–OH).
Непредельные спирты с ОН-группой при атоме углерода, соединенном с другим атомом двойной связью, очень неустойчивы и сразу же изомеризуются в альдегиды или кетоны. Например, виниловый спирт CH2=CH–OH превращается в уксусный альдегид CH3–CH=O (см. реакция Кучерова).
Номенклатура спиртов
Систематические названия даются по названию углеводорода с добавлением суффикса -ол и цифры, указывающей положение гидроксигруппы (если это необходимо). Например:

Нумерация ведется от ближайшего к ОН-группе конца цепи.
Цифра, отражающая местоположение ОН-группы, в русском языке обычно ставится после суффикса "ол". Это разгружает словесную часть названия от цифр (например, 2-метилбутанол-1). В англоязычной литературе цифру ставят перед названием главной цепи: 2-метил-1-бутанол. Правила IUPAC разрешают учитывать особенности национального языка.
По другому способу (радикально-функциональная номенклатура) названия спиртов производят от названий радикалов с добавлением слова "спирт". В соответствии с этим способом приведенные выше соединения называют: метиловый спирт, этиловый спирт, н-пропиловый спирт, изопропиловый спирт.
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами -диол (две ОН-группы), -триол (три ОН-группы) и т.д. Например:

Фенолы
Фенолы – гидроксисоединения, в молекулах которых ОН-группы связаны непосредственно с бензольным ядром.

В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные:
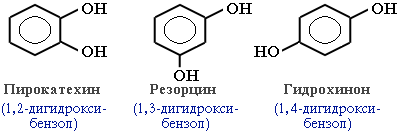
Как видно из приведенных примеров, фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы).
Строение гидроксильной группы
Свойства спиртов и фенолов определяются строением гидроксильной группы, характером ее химических связей, строением углеводородных радикалов и их взаимным влиянием.
Связи О–Н и С–О – полярные ковалентные. Это следует из различий в электроотрицательности кислорода (3,5), водорода (2,1) и углерода (2,4). Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:

Дипольный момент связи С–О составляет 0,70D, а связи О–Н – 1,51D. Разрыв таких связей происходит преимущественно гетеролитически (по ионному механизму).
 Атому кислорода в спиртах свойственна sp3-гибридизация. В образовании его связей с атомами C и H участвуют две 2sp3-атомные орбитали, валентный угол C–О–H близок к тетраэдрическому (около 108°). Каждая из двух других 2sp3-АО кислорода занята неподеленной парой электронов.
Атому кислорода в спиртах свойственна sp3-гибридизация. В образовании его связей с атомами C и H участвуют две 2sp3-атомные орбитали, валентный угол C–О–H близок к тетраэдрическому (около 108°). Каждая из двух других 2sp3-АО кислорода занята неподеленной парой электронов.
В фенолах под влиянием π-электронной системы бензольного кольца для атома кислорода предпочтительней sp2-гибридизация. При этом одна из неподеленных электронных пар находится на негибридной р-орбитали и может участвовать в сопряжении с ароматической π-системой.

Электронные эффекты ОН-группы. Гидроксигруппа проявляет отрицательный индуктивный эффект (–I-эффект) по отношению к углеводородному радикалу и в спиртах выступает как электроноакцепторный заместитель. В фенолах, где ОН-группа находится при sp2-атоме углерода, кроме того, она проявляет положительный мезомерный эффект (+M), предоставляя неподеленную электронную пару кислорода в π-систему сопряжения бензольного кольца (анимация, 6 Kб). Вследствие большей подвижности p-электронов +М-эффект сильнее, чем -I-эффект, т.е. гидроксигруппа в фенолах является электронодонорным заместителем (отрицательный заряд на атоме кислорода в феноле ниже, чем в предельных одноатомных спиртах).
Сравните распределение электронной плотности (зарядов на атомах) в молекулах метанола и фенола.
|
из
5.00
|
Обсуждение в статье: Строение гидроксильной группы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

