 |
Главная |
Аналитическое выражение II закона термодинамики
|
из
5.00
|
Для обратимого цикла Карно имеем:
 ,
,
тогда 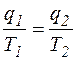 или
или  .
.
Если учесть в этом соотношении, чтоq1 >0 (теплота подводится к рабочему телу) и q2<0 (теплота отводится от рабочего тела), то
 или
или  (6.6)
(6.6)
Отношение подводимой или отводимой теплоты к соответствующей абсолютной температуре называется приведенной теплотой. Выражение (6.6) показывает, что алгебраическая сумма приведенных теплот для обратимого цикла Карно равна нулю, т.е.
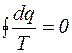 . (6.7)
. (6.7)
Отношение  считают полным дифференциалом функции состояния
считают полным дифференциалом функции состояния 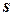 , называемой энтропией. Т.к. dq = Tds, то
, называемой энтропией. Т.к. dq = Tds, то
 (6.8)
(6.8)
Таким образом, алгебраическая сумма приведенных теплот для любого обратимого цикла равна нулю. Энтропия рабочего тела в результате совершения произвольного обратимого цикла не изменяется.
Уравнение (6.8), выведенное Клаузиусом в 1854 году, представляет собой аналитическое выражение II закона термодинамики для произвольного обратимого цикла и называется первым интегралом Клаузиуса.
В цикле с необратимыми процессами при прочих равных условиях работа, совершаемая рабочим телом меньше, чем в цикле с обратимым процессом, и при одинаковх температурах источника теплоты и холодильника
h tнеобр<ht
Поэтому при наличии в цикле необратимых процессов:
 <0 (6.9)
<0 (6.9)
или после интегрирования по контуру
 <0(6.10)
<0(6.10)
Это неравенство представляет собой аналитическое выражение II закона термодинамики для произвольного необратимого цикла и называется вторым интегралом Клаузиуса.
Объединяя (6.7) и (6.10), можно записать одно уравнение II закона термодинамики для обратимых (=) и необратимых (<) циклов:
 £0 (6.11)
£0 (6.11)
Энтропия есть функция состояния рабочего тела, поэтому изменение энтропии как для обратимого, так и необратимого процессов будет одним и тем же.
Для элементарного необратимого процесса
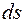 >
>  (6.12)
(6.12)
В общем виде для любого процесса изменение энтропии удовлетворяет соотношению
 , (6.13)
, (6.13)
где dq - количество теплоты, полученное телом от источника теплоты; Т- абсолютная температура источника теплоты. Знак равенства относится к обратимым, знак неравенства - к необратимым процессам.
Следует различать понятия энтропия тела и энтропия системы.
Энтропия не является функцией состояния системы, состоящей из нескольких тел (рабочее тело, холодильники и источники теплоты), каждое из которых характеризуется своими параметрами. Поэтому на изменение энтропии системы влияет характер процесса теплообмена между рабочим телом и источником теплоты. При протекании обратимых процессов энтропия системы остается постоянной; при необратимых процессах энтропия системы возрастает.
Если в адиабатной изолированной системе протекают только обратимые процессы, то
ds = dq/T,
для адиабатной системы это уравнение принимает вид: dq = Tds = 0
Так как Т ¹ 0, то для всей системы ds = 0 и s = const.
Таким образом, если в изолированной адиабатной системе протекают только обратимые процессы, то энтропия всей системы остается величиной постоянной.
Для адиабатной системы при наличии в ней необратимых процессов:
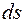 >
>  .
.
Т.к.dq = 0, то для адиабатной изолированной системы ds ³ 0, т.е. происходит увеличение энтропии.
В термодинамике большое значение имеет понятие работы, которую совершает система при изменении своего состояния и условий, при которых получается максимальная работа.
Получение работы возможно только от такой системы, которая не находится в равновесном состоянии с окружающей средой. По мере совершения работы система будет приближаться к равновесному состоянию со средой. Тепловая энергия, переданная в окружающую среду, становится полностью неработоспособной, т.к. при этом происходит выравнивание температур источника и приемника. Очевидно, наибольшая работа в системе может быть совершена при достижении в ней равновесного состояния путем обратимых процессов.
Максимальная работоспособность системы, получаемая в обратимом цикле Карно в температурном интервале от 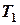 до
до  , называется эксергией (ex).
, называется эксергией (ex).
 . (6.14)
. (6.14)
Работа необратимого цикла Карно, в котором теплота  передается рабочему телу при температуре
передается рабочему телу при температуре 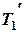 ниже температуры нагревателя
ниже температуры нагревателя 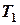 :
:
 . (6.15)
. (6.15)
Потеря работы :
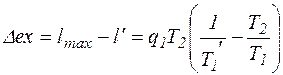 . (6.17)
. (6.17)
Эксергия является обобщенной качественной и количественной характеристикой для потока теплоты и потока вещества, зависящей одновременно от параметров системы и окружающей среды. В отличии от энергии в реальных процессах, эксергия количественно не сохраняется. Всякая необратимость в системе приводит к уменьшению работоспособности, т.е. к потерям энергии. Уменьшение работы ведет к увеличению энтропии  :
:
 . (6.18)
. (6.18)
Уравнение (6.18) называют уравнением Гюи-Стодолы.
|
из
5.00
|
Обсуждение в статье: Аналитическое выражение II закона термодинамики |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

