 |
Главная |
Методом в природных и сточных водах
|
из
5.00
|
Фосфор является необходимым элементом для жизни. Являясь важнейшим биогенным элементом, именно фосфор чаще всего лимитирует развитие продуктивности водоемов. Поэтому поступление избытка соединений фосфора с водосбора в виде минеральных удобрений с поверхностным стоком полей (с гектара орошаемых земель может выносится 0,4–0,6 кг фосфора), со стоками ферм (0,01–0,05 кг/сут. на одно животное), с недоочищенными или неочищенными бытовыми сточными водами (0,003–0,006 кг/сут. на одного жителя), а также с некоторыми производственными расходами приводит к резкому неконтролируемому приросту растительной биомассы водного объекта. Особенно характерен данный процесс для малопроточных и непроточных водоемов. Происходит изменение трофического статуса водоема, сопровождающееся перестройкой всего водного сообщества и ведущее к преобладанию гнилостных процессов (и, соответственно, возрастанию мутности, солености, концентрации бактерий).
В природных и сточных водах фосфор может присутствовать в разных видах. В растворенном состоянии (иногда говорят - в жидкой фазе анализируемой воды) он может находиться в виде ортофосфорной кислоты (Н3РО4)и ее анионовв виде мета-, пиро- и полифосфатов (эти вещества используют для предупреждения образования накипи, они входят также в состав моющих средств). Кроме того, существуют разнообразные фосфорорганические соединения - нуклеиновые кислоты, нуклеопротеиды, фосфолипиды и др., которые также могут присутствовать в воде, являясь продуктами жизнедеятельности или разложения организмов. К фосфорорганическим соединениям относятся также некоторые пестициды.
Минерализация приводит к превращению в ортофосфаты все, даже труднорастворимые, формы фосфатов в воде. Таким образом, определяется содержание общего фосфора в любой воде (этот показатель можно определять как для растворенных фосфатов, так и для нерастворимых соединений фосфора). Однако для природных вод, не содержащих или содержащих незначительное количество трудногидролизующихся фосфатов в твердой фазе, минерализации обычно не требуется, и полученный при анализе гидролизованной пробы результат с хорошим приближением может быть принят за содержание общего фосфора.
ПДК полифосфатов (триполифосфат и гексаметафосфат) в воде водоемов составляет 3,5 мг/л в пересчете на ортофосфат-анион РО43-, лимитирующий показатель вредности – органолептический.
Диапазон определяемых концентраций ортофосфатов в воде при визуально-колориметрическом определении – от 0,2 до 7,0 мг/л, при фотометрическом определении – 0,01–0,4 мг/л. Определение визуально-колориметрическим методом возможно и при концентрации ортофосфатов более 7,0 мг/л после соответствующего разбавления пробы чистой водой.
Метод основан на получении восстановленной фосфорномолибденовой гетерополикислоты – "молибденовой сини".
При взаимодействии фосфатов с молибдатом (VI) в кислой среде образуется фосфорно-молибденовая гетерополикислота Н7Р(Мо2О7)6, которая восстанавливается аскорбиновой кислотой в присутствии сурьмяно-виннокислого калия до фосфорно-молибденового комплекса, окрашенного в голубой цвет.
Оптическую плотность образованного фосфорно-молибденового комплекса определяют на фотоэлектроколориметре при красном светофильтре. Содержание фосфора фосфатов в пробе определяют по показаниям прибора, пересчитанным по предварительно построенному градуировочному графику.
Цель работы – определение фосфат-иона в пробах природных вод.
Оборудование и реактивы:
– фотоколориметр;
– весы аналитические;
– весы технические;
– колбы мерные вместимостью 50, 100 см3;
– цилиндры мерные вместимостью 50, 100 см3;
– колбы конические плоскодонные вместимостью 100 см3;
– смешанный реактив – смесь …..;
– смесь аскорбиновой и серной кислот.
Ход работы
1. В коническую плоскодонную колбу вместимостью 100 см3 отбирают 50,0 см3 отфильтрованной исследуемой пробы воды. Объем отбирают пипеткой вместимостью 50 см3. К пробе добавляют 10,0 см3 смешанного реактива, и раствор хорошо перемешивают.
2. Через 10 мин на фотоэлектроколориметре измеряют оптическую плотность раствора при красном светофильтре в кювете с толщиной оптического слоя 5 см, используя в качестве сравнения дистиллированную воду.
3. Если исследуемая проба воды окрашена или слегка мутная, отдельно измеряют ее оптическую плотность относительно дистиллированной воды при красном светофильтре в кювете с толщиной оптического слоя 5 см, добавив к пробе 10 см3 смеси серной и аскорбиновой кислот вместо смешанного индикатора.
4. По градуировочной характеристике полученному значению оптической плотности ставят в соответствие значение концентрации фосфат-ионов в исходной пробе воды. Содержание фосфатов (Сх) в мг/дм3 находят по формуле 3.12.
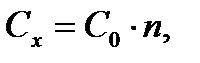
| (3.10) |
где Со – концентрация фосфат-ионов, найденная по градуировочной характеристике, мг/дм3;
n – степень разбавления исходной пробы воды (в случае, если исследуемую пробу не разбавляли, n = 1).
Форма записи результатов определения фосфат иона в пробах природных вод представлена в таблице 7.3.
Таблица 7.3. Форма записи результатов определения фосфат-иона
в пробах природных вод
| Проба | Место отбора | Показания прибора (D) | Содержание фосфат-иона, найденного по градуировочному графику мг/дм3 | Содержание фосфат-иона с учетом разбавления, мг/дм3 |
| 1. | ||||
| 2. | ||||
| Среднее |
5. Сделать выводы и предложить проект снижения фосфат-ионов в природных водах.
|
из
5.00
|
Обсуждение в статье: Методом в природных и сточных водах |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

