 |
Главная |
Абсорбция. Общие сведения о процессе и область его применения. Принципиальная схема абсорбционно-десорбционной установки
|
из
5.00
|
В системе, состоящей из газа и соприкасающейся с ним жидкости, молекулы газа, ударяющиеся о поверхность жидкости, растворяются в ней. Эти растворяемые молекулы, продолжая двигаться, частично возвращаются в газовую фазу, а частично остаются в жидкой фазе. Растворение молекул газа в жидкости будет продолжаться до достижения состояния равновесия. Концентрация газа, растворенного в жидкой фазе, зависит от парциального давления над поверхностью жидкости.
Согласно правилу фаз Гиббса система, состоящая из жидкости и растворенного в ней газа, имеет две степени свободы
С=К+2-Ф=2+2-2=2 (6.84)
Следовательно, состояние системы определяется температурой и давлением. При постоянной температуре растворяемость газа зависит от давления системы.
По закону Генри растворимость газа в жидкости прямо пропорциональна его парциальному давлению
 , (6.85)
, (6.85)
 , (6.86)
, (6.86)
где хг - концентрация газа, растворенного в жидкости (в мольных долях);
 - парциальное давление газа над жидкостью;
- парциальное давление газа над жидкостью;
 - const Генри;
- const Генри;
 - коэффициент, зависящий от свойств газа и жидкости.
- коэффициент, зависящий от свойств газа и жидкости.
Из основного уравнения равновесия (закона Дальтона)
 , (6.87)
, (6.87)
где yА - концентрация поглощаемого компонента А в газе (в мольных долях);
 - парциальное давление компонента А над жидкостью;
- парциальное давление компонента А над жидкостью;
Р – общее давление.
 , (6.88)
, (6.88)
где хА - концентрация поглощаемого компонента А в жидкости (в мольных долях);
 - коэффициент распределения или const фазового равновесия
- коэффициент распределения или const фазового равновесия
 (6.89)
(6.89)
С повышением температуры константа m как правило, увеличивается, следовательно, растворимость газа снижается. (Исключение составляют растворимости азота и водорода в углеводородах, у которых растворимость увеличивается с повышением температуры)
Абсорбция – процесс разделения газовых смесей путем избирательного поглощения отдельных компонентов смеси жидким поглотителем – абсорбентом.
Поглощение газа может происходить либо за счет его растворения в абсорбенте, либо в результате его химического взаимодействия с абсорбентом. В первом случае процесс называют физической абсорбцией, а во втором – хемосорбцией. Возможно также сочетание обоих механизмов процесса. Поглощаемые компоненты газовой смеси условимся называть абсорбтивом, непоглощаемые инертами.
В химической технологии абсорбция используется
- для получения целевых продуктов (абсорбция газообразного HCl водой в производстве соляной кислоты и т.д.)
- для выделения ценных компонентов газовых смесей (бутан-бутиленовой фракции из контактного газа в производстве СК, ацетилена из газов крекинга и т.д.);
- для удаления вредных примесей из газовых смесей.
Механизм процесса абсорбции состоит в следующем. На поверхности раздела фаз имеются два пограничных слоя – жидкий и газообразный. Молекула газа, прежде чем проникнуть в толщу жидкости, должна пройти эти два слоя. Перемещение молекул через газовую и жидкую пленку может происходить только путем диффузии; скорость диффузии зависит от разности парциальных давлений газа в общей массе и в пленке. Эта разность является движущей силой процесса абсорбции.
Если парциальное давление или концентрация компонента в газовой фазе будет больше чем жидкости – процесс абсорбции; если концентрация компонентов в жидкой фазе больше, чем в газовой – процесс десорбции.
Сравним процессы абсорбции и ректификации.
Общее между ними:
- применяются для разделения смесей;
- относятся к массообменным процессам;
движущая сила – разность парциальных давлений или концентраций.
Различия:
- ректификация – двухсторонний массообменный процесс: паровая фаза обогащается НКК, а жидкая ВКК.
- абсорбция – основной массообменный процесс за счет перехода каких-то компонентов из газовой фазы в жидкую. При этом считаем, что летучесть абсорбента мала, т.е. нет перехода компонентов из жидкой фазы в газовую.
- абсорбция является процессом избирательным. Каждый абсорбент обладает способностью в заметных количествах поглощать одни компоненты, тогда как другие компоненты поглощаются незначительно или вовсе не поглощаются. Большое влияние на процесс абсорбции оказывают также температура и давление.
- в процессе абсорбции газов жидкостью выделяется тепло, называемое теплотой абсорбции. При отсутствии химического взаимодействия между абсорбентом и абсорбируемым газом теплота абсорбции численно равна скрытой теплоте конденсации. В случае химического взаимодействия необходимо также учитывать теплоту реакции. Теплоту абсорбции необходимо отводить, т.к повышение температуры абсорбентов резко ухудшает процесс абсорбции.
На рисунке 6.27 изображена принципиальная схема абсорбционно-десорбционной установки

1-абсорбер; 2-десорбер; 3-холодильник; 4-конденсатор; 5-нагреватель; 6-теплообменник
Рисунок 6.27 - Принципиальная схема абсорбционно–десорбционной установки
Расчёт процессов абсорбции-десорбции ведётся по относительным концентрациям, т.е. определяя составы как жидкой, так и газовой фаз по отношению к входящим потокам.
Введём обозначения
 - расход газового сырья;
- расход газового сырья;
 - относительная концентрация извлекаемого компонента в сырье;
- относительная концентрация извлекаемого компонента в сырье;
 - расход абсорбента;
- расход абсорбента;
 - относительная концентрация извлекаемого компонента в абсорбенте;
- относительная концентрация извлекаемого компонента в абсорбенте;
 - расход насыщенного абсорбента;
- расход насыщенного абсорбента;
 - расход инертов;
- расход инертов;
 - относительная концентрация извлекаемого компонента в инертах;
- относительная концентрация извлекаемого компонента в инертах;
 - расход десорбирующего агента;
- расход десорбирующего агента;
 - относительная концентрация извлекаемого компонента в десорбирующем агенте;
- относительная концентрация извлекаемого компонента в десорбирующем агенте;
Выразим относительные концентрации через обычные
 , (6.90)
, (6.90)
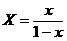 , (6.91)
, (6.91)
 , (6.92)
, (6.92)
 , (6.93)
, (6.93)
 (6.94)
(6.94)
 , (6.95)
, (6.95)
 , (6.96)
, (6.96)
 (6.97)
(6.97)
Основные показатели абсорбции
Основными показателями абсорбции являются коэффициент извлечения и эффективность извлечения.
Коэффициент извлечения  - отношение количества поглощенного компонента к его содержанию в исходной смеси
- отношение количества поглощенного компонента к его содержанию в исходной смеси
 (6.98)
(6.98)
При полном извлечении  . Тогда
. Тогда  . Во всех остальных случаях
. Во всех остальных случаях  <1.
<1.
Эффективность извлечения 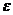 - отношение количества поглощенного компонента к теоретическому, достигаемому в условиях равновесия между уходящим из абсорбента газом и вводимым абсорбентом
- отношение количества поглощенного компонента к теоретическому, достигаемому в условиях равновесия между уходящим из абсорбента газом и вводимым абсорбентом
 , (6.99)
, (6.99)
где Y0 – относительная концентрация извлекаемого компонента в газовом потоке, равновесном входящему абсорбенту.
С учётом уравнения (6.89) можно записать
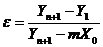 , (6.100)
, (6.100)
Х0 показывает степень регенерации. Если регенерация 100%, то Х0=0.
При Х0=0; Y=0, то ε=φ. Во всех других случаях ε>φ.
Абсорбенты, применяемые в процессе абсорбции, должны обладать высокой абсорбционной способностью, быть избирательными, иметь низкое давление паров, быть нетоксичными, огне- и взрывобезопасными, иметь низкую стоимость и т.д.
Абсорбенты выбирают по растворимости в них поглощаемых компонентов.
Растворимость зависит от физико – химических свойств газа и жидкости, темпе-
ратуры системы и давления.
|
из
5.00
|
Обсуждение в статье: Абсорбция. Общие сведения о процессе и область его применения. Принципиальная схема абсорбционно-десорбционной установки |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

