 |
Главная |
Основные фармакологические эффекты опиоидных анальгетиков на примере морфина (МФ)
|
из
5.00
|
Обезболивающее действие. Анальгезия, вызываемая морфином, обусловлена стимуляцией всех типов опиатных рецепторов без утраты сознания. Обезболивающее действие МФ и других опиоидов основано на прямом торможении афферентных ноцицептивных путей, идущих от задних рогов спинного мозга, и активацией эфферентных антиноцицептивных путей, идущих из среднего мозга через продолговатый мозг к задним рогам спинного мозга. По ходу этих путей (в околоводопроводном сером веществе, РФ, срединных и большом ядрах шва ствола мозга, спинном мозге) обнаружены опиоидные рецепторы. Стимуляция МФ этих рецепторов приводит к увеличению выхода из нейронов ионов калия, уменьшению входа ионов кальция, что обусловливает развитие гиперполяризации клетки и торможению постсинаптических нейронов. Кроме того, МФ угнетает выброс нейромедиаторов боли.
Подкрепляющее действие и настроение. На фоне действия МФ и его аналогов повышается переносимость боли. Модуляция восприятия боли и эйфория, наблюдаемые на фоне введения в организм МФ, по-видимому, осуществляется в пределах лимбической системы головного мозга (передняя височная, лобная кора головного мозга, некоторые отделы гипоталамуса). Именно в лимбической системе выявлена наибольшая плотность опиатных рецепторов, таких как μ -, κ - и σ – рецепторы. Эти рецепторы в лимбической системе регулируют функционирование дофаминергической системы. Т.н. подкрепляющий эффект морфина и других опиоидных анальгетиков связывают с усилением выброса медиатора дофамина в лимбической системе, в коре больших полушарий и гипоталамусе. Экспериментально показано, что появление положительных эмоций, безмятежности, чувства покоя, истомы, а также эйфории связано со стимуляцией μ - и σ - рецепторов, а применение препаратов, обладающих тропностью к κ-рецепторам (напр., пентазоцин, налоксон) вызывает обратные эффекты – дисфорию (апатия, сонливость, психические переживания, тоска, скорбь и страх), так как κ - рецепторы угнетают выброс дофамина.
Другие центральные эффекты. Опиатные рецепторы, являющиеся мишенями для эффектов опиоидных анальгетиков, находятся практически во всех отделах нервной системы, поэтому спектр их центральных эффектов весьма широк. Опиоиды, как и сам МФ, влияют на центр терморегуляции гипоталамуса. Они тонизируют центр теплоотдачи и снижают установочную температуру, тем самым (особенно в высоких токсических дозах) вызывают гипотермию. Морфин снижает выделение гипоталамических рилизинг – гормонов, в частности гонадолиберинов (стимулирующих высвобождение ФСГ и ЛГ аденогипофизом) и кортиколиберина (стимулирующего синтез и секрецию АКТГ аденогипофизом). В результате, косвенно снижается плазменная концентрация гормонов коры надпочечников и половых гормонов.
37)Внутриклеточные (молекулярно-генетические) механизмы формирования химических форм наркотической зависимости: роль транскрипционных факторов CREB и дельта-focB в явлениях «привыкания» и «сенситизации» (наркотического срыва).
Транскрипционные факторы (ТФ), участвующие в формировании наркотической зависимости (влияют на процессы считывания информации с генома – ДНК). cAMP response element-binding protein (CREB) (ТФ); Белок дельта-fosB (ТФ); CDK5 = циклин-зависимая киназа 5 (cyclin-dependent kinase 5) - белок, входящий в семейство циклин-зависимых киназ. CDK5 необходима для нормального развития мозга, участвует в процессах нейронального созревания и нейромиграции. Участвует в регуляции внутриклеточных реакций на ДФ сигналы (разрастание шипикового аппарата). Циклины - семейство белков-активаторов циклин-зависимых протеинкиназ (CDK) (англ. CDK, cyclin-dependent kinases) - ключевых ферментов, участвующих в регуляции клеточного цикла эукариот.
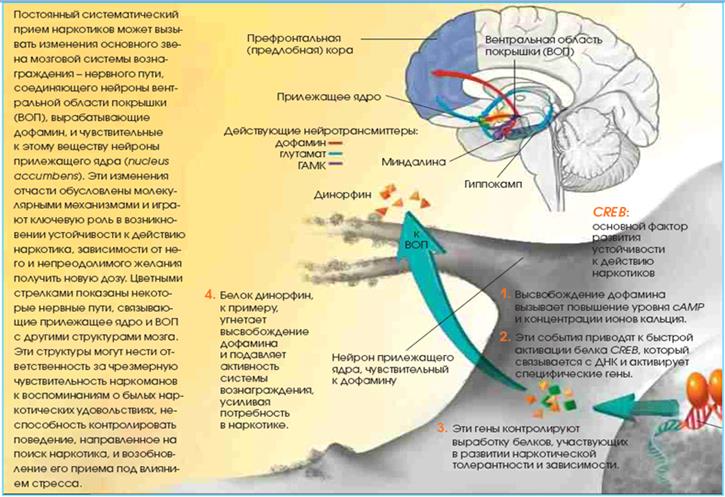
Наркотический срыв. Неослабевающая тяга сохраняется и после длительных периодов воздержания. И тут речь идет о другом факторе транскрипции – дельта-fosB. Дельта-fosB связан с развитием наркотического привыкания совсем иначе, нежели CREB. В опытах на мышах и крысах было установлено, что постоянное систематическое потребление наркотиков приводит к постепенному и стабильному увеличению концентрации этого белка в прилежащем ядре и других структурах головного мозга. Кроме того, поскольку дельта-fosB отличается необычайной устойчивостью, он остается активным в нейронах этих структур спустя недели и месяцы после приема препаратов. Такая активность вполне могла бы позволить белку поддерживать изменения в экспрессии генов еще долгое время после прекращения приема наркотиков. Как показывают исследования мутантных мышей с чрезмерной выработкой дельта-fosB в прилежащем ядре, эти животные сверхчувствительны к наркотикам. Они с необычайной легкостью возобновляли прием препарата после его длительной отмены. Интересно отметить, что дельта-fosB вырабатывался у экспериментальных мышей и в ответ на повторные вознаграждения ненаркотической природы (например, быстрый бег в беличьем колесе или потребление сахара). Наркотический срыв. Неослабевающая тяга сохраняется даже после длительных периодов воздержания. Чтобы понять природу сенситизации, необходимо в первую очередь выяснить, какие молекулярные изменения могут сохраняться в течение периода, превышающего несколько дней. И тут речь идет о другом факторе транскрипции – дельта-fosB. Дельта-fosB связан с развитием наркотического привыкания совсем иначе, нежели CREB. В опытах на мышах и крысах было установлено, что постоянное систематическое потребление наркотиков приводит к постепенному и стабильному увеличению концентрации этого белка в прилежащем ядре и других структурах головного мозга. Кроме того, поскольку дельта-fosB отличается необычайной устойчивостью, он остается активным в нейронах этих структур спустя недели и месяцы после приема препаратов. Такая активность вполне могла бы позволить белку поддерживать изменения в экспрессии генов еще долгое время после прекращения приема наркотиков. Как показывают исследования мутантных мышей с чрезмерной выработкой дельта-fosB в прилежащем ядре, эти животные сверхчувствительны к наркотикам. Они с необычайной легкостью возобновляли прием препарата после его длительной отмены. Интересно отметить, что дельта-fosB вырабатывался у экспериментальных мышей и в ответ на повторные вознаграждения ненаркотической природы (например, быстрый бег в беличьем колесе или потребление сахара).
38) Роль дофаминергической и опиоидной систем мозга в формировании химических и нехимических форм аддиктивного поведения.
В вентральной области покрышки содержатся нейроны, которые высвобождают дофамин в прилежащее ядро и орбитальную лобную кору. Предполагается, что нарушения дофаминергической передачи в системе награды лежат в основе любой аддикции. Недостаток дофамина приводит к поиску веществ или действий (азартные игры, наркотики), при котором происходит высвобождение дофамина и возникает ощущение удовольствия (Zack, Poulos, 2009).
Эндогенные опиоидные и каннабиноидные системы играют ключевую роль, определяющую подкрепляющее действие пищи: они отвечают за гомеостатическую и гедонистическую стороны пищевого поведения
При сниженном уровне эндорфинов избыточное переедание, как и голодание, приводит к усилению их выброса, что обеспечивает положительное подкрепление
Любая аддикция формируется на последовательном чередовании специфических психологических состояний, когда переживание напряжения, эмоциональной боли, чувства одиночества сменяется сильным положительным ощущением и запоминается путь приобретения этого опыта устранения неприятностей. Аддиктивное поведение развивается как субъективная фиксация на том, что человек считает для себя безопасным и успокаивающим.
Сейчас выявлен целый ряд структур, имеющих подобное подкрепляющее значение. К ним относятся обонятельные луковицы, префронтальная кора, nucleus accumbens (прилежащее ядро), хвостатое ядро, скорлупа, некоторые та-ламические ядра, ретикулярная формация среднего мозга, черная субстанция, голубое пятно (Olds, Fobes, 1981). Однако наибольший подкрепляющий эффект отмечен при помещении электродов в медиальный переднемозговой пучок. Его волокна идут от среднего мозга через латеральный гипоталамус в направлении базального переднего мозга. Среди его аксонов есть дофаминергические, но-радренергические и серотонинергические, причем доказано особое участие до-фаминергических нейронов в процессе подкрепления
Многочисленные эксперименты с использованием веществ, усиливающих или имитирующих действие дофамина (агонистов) и веществ, препятствующих действию или ослабляющих его (антагонистов), подтвердили участие дофаминергических нейронов в процессах подкрепления. Например, введение препаратов, блокирующих дофаминовые рецепторы, выявило невозможность процесса подкрепления.
· В многочисленных исследованиях была продемонстрирована важнейшая роль опиоидных
· систем мозга в патогенетических процессах, ведущих к формированию наркотической и
· алкогольной зависимости
· В многочисленных исследованиях была продемонстрирована важнейшая роль опиоидных
· систем мозга в патогенетических процессах, ведущих к формированию наркотической и
· алкогольной зависимости
· В многочисленных исследованиях была продемонстрирована важнейшая роль опиоидных
· систем мозга в патогенетических процессах, ведущих к формированию наркотической и
· алкогольной зависимости
Опиоидная система – одна из нейроэндокринных систем, вырабатывающая более 40 нейрогормонов (опиоидных пептидов). Главное ее назначение - защита от стрессорных повреждений, обезболивание и координация работы систем органов и тканей на уровне организма в целом.
В биологический механизм аддикции могут быть включены некоторые участки мозга. Наиболее примечательным является механизм высвобождения дофамина в Nucleus accumbens, который запускается многими наркотическими веществами, что укрепляет зависимость[23]. Выделение дофамина является естественным процессом стимулирующего действия, свойственным, например, питанию или сексу. Наркотики действуют аналогично. В частности, некоторые наркотикиувеличивают выработку и высвобождение дофамина в мозге в 5—10 раз, что позволяет людям, которые их употребляют, получать чувство удовольствия искусственным образом[24][25][26]. Так, амфетамин напрямую стимулирует выброс дофамина, воздействуя на механизм его транспортировки[27]. Другие наркотики, например, кокаин и психостимуляторы, блокируют естественные механизмы обратного захвата дофамина, увеличивая его концентрацию в синаптическом пространстве[28]. Морфий и никотин имитируют действие натуральных нейромедиаторов[28], а алкоголь блокирует действие антагонистов дофамина[29]. Начавшись в лимбической дофаминергической системе процесс затем модифицирует другие части мозга, например, вентральную область покрышки[30].
Механизмы, с помощью которых осуществляется этот процесс, включают в себя проникновение дополнительных AMPA-рецепторов в постсинаптическую мембранудофаминергических нейронов. Исследования на мышах показывают, что воздействие кокаина в течение двух недель служит причиной долговременных изменений в вентральной области покрышки. Более того, эффект удовольствия от наркотика усиливает поведение, связанное с его получением и приёмом, пока это не формируется в привычку. Первоначально процесс проходит в вентральной части стриатума, главным образом в центре подкрепления (англ. Nucleus accumbens), но затем изменения развиваются в верхней части стриатума (dorsal striatum). Предположительно, связанные с аддикцией модификации нейронов идут по дорсально каскадной последовательности взаимных соединений между двумя вышеупомянутыми областями[31].
На предрасположенность к появлению наркотической зависимости оказывают влияние несколько факторов. Возможно, она связана с предфронтальной корой головного мозга, которая отвечает за суждения, решения рисковать, контроль импульсивности. Это объяснило бы, почему дети более предрасположены к наркомании. Отдельные исследования показывают, что дети в возрасте от 10 до 12 лет, те, которые проявляют наименьшее торможение в поведении, находятся в максимальной зоне риска для появления аддикции к наркотическим веществам[
|
из
5.00
|
Обсуждение в статье: Основные фармакологические эффекты опиоидных анальгетиков на примере морфина (МФ) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

