 |
Главная |
Примеры решения заданий
|
из
5.00
|
Пример 1. Укажите степень окисления (СО) подчеркнутых атомов элементов в предложенных частицах, а также их высшую и низшую степени окисления. Объясните, какую роль могут выполнять указанные частицы в окислительно-восстановительных реакциях: только окислитель (Ox), только восстановитель (Red), окислитель и восстановитель (Ox и Red).
Cr2O3, С lO4–, Zn, H2S
Cr2O3 2х + 3·(-2) = 0 CO = +3
Хром – элемент VI группы, следовательно, высшая степень окисления его +6, т. к. хром является металлом, то его низшая степень окисления 0. В данном случае хром проявляет промежуточную степень окисления, следовательно, в окислительно-восстановительных реакциях данная частица может быть и окислителем и восстановителем (Ox и Red).
С lO4– х + 4·(-2) = –1 CO = +7
Хлор – элемент VII группы, следовательно, высшая степень окисления его +7, хлор – неметалл, следовательно низшая степень окисления его 7 - 8 = -1. В окислительно-восстановительных реакциях С lO4– может быть только окислителем (Ox).
Zn CO = 0
Цинк – элемент II группы, следовательно, высшая степень окисления его +2, цинк – металл, низшая степень окисления 0. В окислительно-восстановительных реакциях Zn может быть только восстановителем (Red).
H2S 2·(-1) + х = 0 CO = -2
Сера – элемент VI группы, значит, его высшая степень окисления +6, низшая степень окисления серы 6 – 8 = -2, следовательно, в окислительно-восстановительных реакциях H2S может быть только восстановителем (Red).
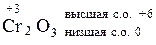 Ox и Red
Ox и Red
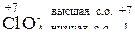 Ox
Ox
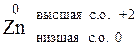 Red
Red
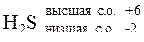 Red
Red
Пример 2. Составьте уравнение полуреакций в заданной среде:
Cr2O72– ® Cr3+ (кислая);
Cr2O3 ® CrO42– (щелочная);
Br2 ® BrO– (нейтральная);
MnO4– ® MnO2 (нейтральная).
Алгоритм составления уравнения полуреакции.
1. Рассчитывают степени окисления атомов элементов, которые ее изменяют.
2. Уравнивают их количество (при необходимости).
3. В соответствии с правилами среды уравнивают количество атомов кислорода и водорода.
4. Указывают количество отданных или принятых электронов.
Cr2O72– ® Cr3+
1. Степень окисления изменяет хром: с +6 в Cr2O72– до +3 в Cr3+;
2. Уравнивают количество атомов хрома:
Cr2O72– ® 2 Cr3+
3. В правую часть для восполнения недостатка 7 атомов кислорода запишем 7 Н2О; в левую часть для уравнивания водорода запишем 14 Н+:
Cr2O72– + 14 Н+ ® 2 Cr3+ + 7 Н2О
4. Степень окисления изменяет хром с +6 до +3, принимая 3ē, учитывая что в полуреакции участвует 2 атома хрома, принимается 6ē:
Cr2O72– + 14 Н+ + 6ē ® 2 Cr3+ + 7 Н2О
Cr2O3 ® CrO42–
1. Степень окисления изменяет хром: с +3 в Cr2O3 до +6 в CrO42–;
2. Уравнивают количество атомов хрома:
Cr2O3 ® 2 CrO42–
3. В левой части недостаток 5 атомов кислорода, добавим 10 ОН –;
в правую часть для уравнивания водорода и кислорода запишем 5 Н2О:
Cr2O3 + 10 ОН –® 2 CrO42– + 5 Н2О
4. Степень окисления изменяет хром с +3 до +6, отдавая 3ē, учитывая, что в полуреакции участвует 2 атома хрома, отдается 6ē:
Cr2O3 + 10 ОН – – 6ē ® 2 CrO42– + 5 Н2О
Br2 ® BrO–
1. Степень окисления изменяет бром: с 0 в Br2 до +1 в BrO–;
2. Уравнивают количество атомов брома:
Br2 ® 2 BrO–;
3. Разница по кислороду в обеих частях (с учетом коэффициента) составляет 2 атома, следовательно, в левую часть необходимо записать 2 Н2О, при этом кислород в обеих частях уравнивается, следовательно, необходимо уравнять в правой части водород, добавив 4Н+:
Br2 + 2 Н2О ® 2 BrO– + 4Н+;
4. Степень окисления изменяет бром с 0 до +1, отдавая 1ē, учитывая, что в полуреакции участвует 2 атома брома, отдается 2ē:
Br2 + 2 Н2О – 2ē ® 2 BrO– + 4Н+;
MnO4– ® MnO2
1. Степень окисления изменяет марганец: с +7 в MnO4– до +4 в MnO2;
2. Количество атомов марганца в обеих частях одинаково, коэффициенты не требуются.
3. Разница по кислороду в обеих частях составляет 2 атома, следовательно, в левую часть необходимо записать 2 Н2О, при этом кислород в обеих частях не уравнялся, следовательно, необходимо уравнять его, добавив в правой части 4 ОН–:
MnO4– + 2 Н2О ® MnO2 + 4 ОН–;
4. Степень окисления изменяет марганец с +7 до +4, принимая 3ē:
MnO4– + 2 Н2О + 3ē ® MnO2 + 4 ОН–;
Пример 2. Запишите электронно-ионные уравнения полуреакций, ионное и молекулярное уравнения реакции, соответствующее данному превращению:
+5 +4 0 +6
КIO3 + Na2SO3 + Н2SO4 ® I2, SO42–
Ox Red среда
К+ + IO3– + 2 Na+ +SO32– + 2 Н+ + SO42– ® I2, SO42–

 2 IO3– + 12Н + + 10ē ® I2 + 6Н2О 2 1
2 IO3– + 12Н + + 10ē ® I2 + 6Н2О 2 1
 SO32– + Н2О - 2ē ® SO42– + 2Н + 10 5
SO32– + Н2О - 2ē ® SO42– + 2Н + 10 5
2 IO3– + 12Н + + 5SO32– + 5Н2О ® I2 + 6Н2О + 5SO42– + 10Н +
2 IO3– + 2Н + + 5SO32– ® I2 + Н2О + 5SO42–
2K+ SO42– 10Na+ 10Na+ 2K+ SO42-
2КIO3 + 5Na2SO3 + Н2SO4 ® I2 + H2O + 5Na2SO4 + K2SO4.
|
из
5.00
|
Обсуждение в статье: Примеры решения заданий |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

