 |
Главная |
Физические и химические свойства
|
из
5.00
|
Введение
Способы получения
1. Получение циклогексанона при окислении циклогексана.
СН2 СО
/ \ / \
Н2С СН2 +0,5О2 Н2С СН2
 | | | |
| | | |
Н2С СН2 Н2С СН2
\ / \ /
СН2 СН2
Циклогексан содержится в нефти, и его можно извлекать из легких нефтяных фракции экстрактивной перегонкой, фракционной кристаллизацией и т.п. На практике циклогексан преимущественно получают каталитическим гидрированием бензола. Это объясняют трудностями, связанными с выделением чистого циклогексана из нефтяного сырья.
Окисление циклогексана можно осуществлять как в паровой, так и в жидкой фазе – некаталитическим путем или в присутствии катализатора.
Главным первичным продуктом окисления является гидроперекись циклогексила:
СН2 СН2
/ \ / \
Н2С СН2 +0,5О2 Н2С СН – ООН
 | | | |
| | | |
Н2С СН2 Н2С СН2
\ / \ /
СН2 СН2
Каталитическое окисление циклогексана проводится в жидкой фазе воздухом или техническим кислородом при повышенном давлении и температуре. Катализаторами являются поливалентные металлы, например кобальт или медь в виде солей. Суммарный выход циклогексанола и циклогексанона достигает 85 %.
Наряду с циклогексанолом и циклогексаноном образуюся продукты более глубокого окисления, главным образом дикарбоновые кислоты (адипиновая, глутаровая и янтарная кислоты).
2. Дегидрирование (окисление) циклогексанола.
Циклогексанол тоже можно перевести в циклогексанон окислением или дегидрированием.
Циклогексанон получают из циклогексанола окислением (окислительным дегидрированием)
СНОН СО
/ \ / \
Н2С СН2 +0,5О2 Н2С СН2
 | | | |
| | | |
Н2С СН2 Н2С СН2
\ / \ /
СНОН СН2
или дегидрированием:
СНОН СО
/ \ / \
Н2С СН2 Н2С СН2
 | | | |
| | | |
Н2С СН2 –Н2 Н2С СН2
\ / \ /
СНОН СН2
Процесс дегидрирования циклогексанола достаточно хорошо освоен в промышленности.
Его проводят при 450 – 4600С над катализатором (оцинкованное железо). Кроме дегидрирования, при этом протекает побочная реакция дегидратации циклогексанола с образованием циклогексена
СНОН СН
/ \ / \\
Н2С СН2 Н2С СН2
 | | | |
| | | |
Н2С СН2 –Н2О Н2С СН2
\ / \ /
СНОН СН2
а также происходит частичное расщепление молекулы циклогексанола с выделением углерода, водорода и воды.
На этом способе снован первый из осуществленных в промышленности методов синтеза циклогексанона – из фенола с предварительном гидрированием его в циклогеканол:
ОH ОH О
| | ||
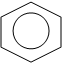

 + 3Н2
+ 3Н2


– Н2
3. Из анилина через циклогексиламин:
NH2 NH2 NH2 О

 | | || ||
| | || ||
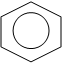


 + 3N2 + Н2О
+ 3N2 + Н2О



– Н2 – NH3
Ввиду меньшего числа стадий и потребности в дополнительных реагентах заслуживает предпочтение метод получения циклогексанона окислением циклогексана.
Физические и химические свойства
Циклогексанон (или кетогексаметилен или пимелинкетон) – это бесцветная жидкость, молекулярная масса 98,15; плотность 0,94; температура плавления – 450 С; температура кипения 1560 С. Растворим в воде (2,431), этаноле, эфире.
Для циклогексанона (представителя кетонов) характерны реакции присоединения.
1. Реакции восстановления.
а. гидрирование в паровой фазе (использование молекулярного водорода)
О ОН
|| |

 Ni, Co
Ni, Co
 + Н2
+ Н2
Pt, Pd
б. восстановление в присутствии амальгамы цинка
О
||

 Н+, Zn, Hg
Н+, Zn, Hg


2. Нуклеофильное присоединение
а. взаимодействие с аммиаком:
О NН
|| |


 + NН3 + Н2О
+ NН3 + Н2О
б. реакция с гидроксиламином (применяется для количественного определения кетонов):
О N – ОН
|| ||


 + NН2ОН + Н2О
+ NН2ОН + Н2О
в. реакция с гидразином:
О N – NН2
|| ||


 + Н2N – NН2 + Н2О
+ Н2N – NН2 + Н2О
г. реакция с PCl5:
СО CCl2
/ \ / \
Н2С СН2 Н2С СН2
 | | + PCl5 | | + POCl3
| | + PCl5 | | + POCl3
Н2С СН2 Н2С СН2
\ / \ /
СН2 СН2
3. Реакции с расширением цикла
а. реакция взаимодействия с диазометаном:
СО CО
/ \ / \
Н2С СН2 Н2С СН2
 | | + СН2NН2 | | + N2
| | + СН2NН2 | | + N2
Н2С СН2 Н2С СН2
\ / | |
СН2 Н2С – СН2
Применение
Циклогексанон используют для производства капрлактама – исходного вещества для получения синтетического волокна капрон:
ОH NОH
| ||

 перегруппировка Бекмана
перегруппировка Бекмана



 N NН
N NН
/ \\ / \\
 Н2С С ОН Н2С С = О
Н2С С ОН Н2С С = О
| | | |

 Н2С СН2 Н2С СН2
Н2С СН2 Н2С СН2
| | | |

 Н2С СН2 Н2С СН2
Н2С СН2 Н2С СН2
При энергичном окислении циклогексанона образуется адипиновая кислота, которую используют для получения синтетического волокна нейлона.
Вывод: Циклогексанон – это циклический кетон. Весьма реакционноспосоден. Применим для производства волокон.
Таблица 1. Данные материального баланса
| Производительность реактора П, т/год | 9700 | |
| Число дней работы реактора в году, n | 332 | |
| Технологический выход продукта f, % | 96 | |
| Молярное соотношение исходных реагентов, А : В | 1 : 2 | |
| Степень превращения ХА, % | 85 | |
| Селективность основной реакции Ф, % | 98 | |
| Состав исходного реагента А, % масс.: | С6Н12 
| 91 |
| примесь С6Н6 | 9,0 | |
| Состав исходного реагента В, % масс.: | О2 | 21 |
| примесь N2 | 79 | |
Реакции синтеза:
Основная реакция

Побочная реакция

|
из
5.00
|
Обсуждение в статье: Физические и химические свойства |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

