 |
Главная |
Определим теплоты сгорания веществ находящихся в жидком состоянии по уравнению Караша
|
из
5.00
|
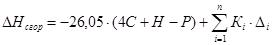
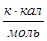
а) для С6Н12
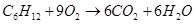
С=6
Н=12
Р=0
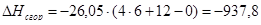
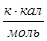
б) для С6Н10О
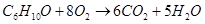
С=6
Н=10
Р=1
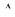 = – 6,5
= – 6,5
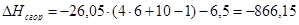
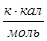
в) для С6Н12О
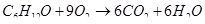
С=6
Н=12
Р=1
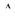 = – 13
= – 13
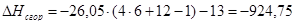
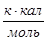
г) для С6Н6
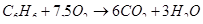
С=6
Н=6
Р=0
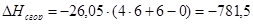
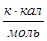
Результаты расчетов сводим в таблицу:
Таблица 12. Результаты расчета теплот сгорания по Карашу
| Вещество | 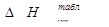
| 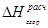
| 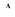
|
| С6Н12 | -944,79 | -937,80 | 0,7 |
| С6Н10О | -866,15 | ||
| С6Н12О | -890,70 | -924,75 | 3,8 |
| С6Н6 | -789,08 | -781,50 | 0,9 |
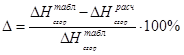
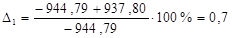
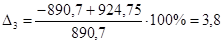
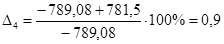
Определение теплоты образования веществ при стандартных условиях в газообразном состоянии по энергиям связи
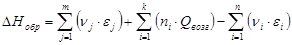
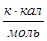
Q воз (С)=125 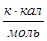
а) для С6Н12
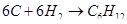
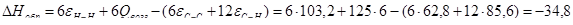
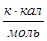
б) для С6Н10О
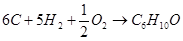
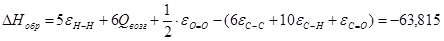
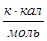
в) для С6Н12О
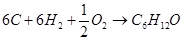
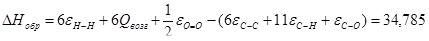
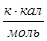
г) для С6Н6
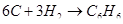
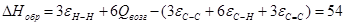
Результаты расчетов сводим в таблицу:
Таблица 13. Результаты расчета теплот образования по энергиям связи
| Вещество | 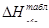
| 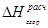
| 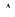
|
| С6Н12 | -29,43 | -34,8 | 18 |
| С6Н10О | -63,815 | ||
| С6Н12О | -83,45 | 34,785 | 141 |
| С6Н6 | -19,82 | 54 | 172 |
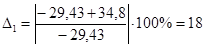
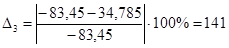
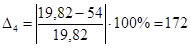
Вывод: Таким образом, в ходе проведенных расчетов установили что из проведенных методов более точным методом расчета теплот сгорания является определение теплот сгорания веществ находящихся в газообразном состоянии по уравнению Коновалова.
Так как в данном методе для молекул имеющих несколько связей одного и того же типов все связи считать равнозначными, и определенные таким образом величины энергии связи представляют собой некоторые средние значения и не соответствуют величинам энергий, которые необходимо затратить на то чтобы оторвать от молекулы данный атом.
VII . Кинетически расчет
Кинетическими уравнениями обычно называют уравнения, выражающие зависимость скорости реакции от различных макроскопических параметров системы. Кинетические уравнения реакций, протекающих в изобарно-изотермических условиях, содержат лишь концентрации компонентов системы и некоторые константы – константы скорости и порядки реакции относительно отдельных компонентов системы.
Для элементарных реакций порядок обычно совпадает с молекулярностью. Молекулярность реакции равна числу молекул соответствующего исходного компонента, участвующему в элементарном акте химического взаимодействия.
Упорядоченная совокупность элементарных актов химической и физической природы некоторой химической реакции составляет механизм химической реакции, или кинетическую модель процесса. Исследование механизма химических реакций в существенной мере основано на детальном исследовании кинетики реакций.
Задание: Определить порядок реакции аналитическим и графическим методами, величину энергии активации графически-аналитическим методом и составить полное кинетическое уравнение.
Дано:
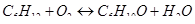
Таблица 15. Исходные данные

| 0 | 0,52 | 1,10 | 1,73 | 2,44 | 3,24 | 4,16 | 5,23 | 6,52 | 8,16 |
| СА,0 | 0,1 | 0,091 | 0,083 | 0,075 | 0,067 | 0,059 | 0,051 | 0,043 | 0,035 | 0,027 |
Таблица 16. Исходные данные
| Температура, К | 713 | 753 | 793 | 833 |
| Константа, с-1 | 3,17.10-2 | 6,73.10-2 | 0,132 | 0,243 |
|
из
5.00
|
Обсуждение в статье: Определим теплоты сгорания веществ находящихся в жидком состоянии по уравнению Караша |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

