 |
Главная |
Диссоциация кислот, оснований и солей в водных растворах
|
из
5.00
|
I . Кислоты – это электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода.
HCl <=>H+ + Cl-
Многоосновные кислоты диссоциируют ступенчато:
I ступень: 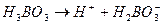 Ка I = 7.3 ×10 -10
Ка I = 7.3 ×10 -10
II ступень: 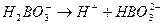 Ка II = 1.8 ×10 -13
Ка II = 1.8 ×10 -13
III ступень: 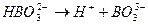 Ка III = 1.6 ×10 -14
Ка III = 1.6 ×10 -14
Ка I ; Ка II ; Ка III называются константами диссоциации по I, II и III ступеням.
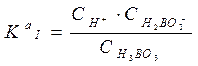 = 7.3 ×10-10;
= 7.3 ×10-10; 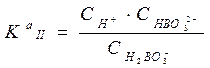 = 1.8 ×10-13
= 1.8 ×10-13
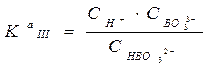 = 1.6 ×10-14
= 1.6 ×10-14
Общий ион H + , придает окраску индикаторам.
II. Основания – это электролиты, при диссоциации которых в качестве анионов образуются только гидроксид - ионы ОН−.
NaOH <=> Na+ + ОН−
Многокислотные основания диссоциируют ступенчато:
Iступень: 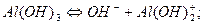
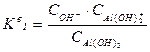 ,
,
I Iступень: 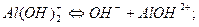
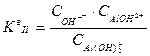 ,
,
I I Iступень: 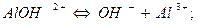
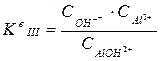 ,
,
Где Кв I ; Кв II ; Кв III - константы диссоциации по I, II и III ступеням.
Анионы ОН− придают окраску индикаторам.
III . Соли –это электролиты, при диссоциации которых образуются катионы металла и анионы кислотного остатка.
Средние соли: NaCl <=> Na+ + Cl-
Кислые соли: NaHSO4<=> Na+ + HSO4-; HSO4- <=> H+ + SO42-
Основные соли: BaOHCl<=> BaOH++ Cl-; BaOH+ <=>Ba2++ ОН−
Общих ионов нет, индикаторы не изменяют окраску.
Процесс электролитической диссоциации веществ в водных растворах количественно характеризуется двумя величинами:
1. степенью электролитической диссоциации - a,
2. константой диссоциации - Кдис.
I . Степень диссоциации (a ) – это отношение числа молекул, распавшихся на ионы к общему числу молекул электролита.
Факторы, влияющие на степень диссоциации:
1. Природа растворенного вещества, тип связи (чем полярнее связь, тем легче идет диссоциация).
2. Природа растворителя (чем больше величина диэлектрической проницаемости ε, тем легче идет диссоциация).
3. Концентрация (при разбавлении a увеличивается; a = 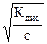 ).
).
4. Температура (с увеличением температуры a растет до определенной величины, затем уменьшается).
5. Влияние одноименного иона (вводимый в систему одноименный ион подавляет диссоциацию слабого электролита).
По величине степени диссоциации электролиты делятся на:
1. Сильные, у которых α > 30% : соли, некоторые кислоты - HClO4, H2SO4, HNO3, HI, HBr, HCl, гидроксиды щелочных металлов, гидроксиды щелочно-зельных металлов: кальция, стронция и бария.
2. Средние, у которых 30% <a<5% : H3PO4.
3. Слабые, у которых a<5% : H2O, HCN, NH4OH.
II . Константа диссоциации (Кдис) – это константа равновесия процесса диссоциации.
Рассмотрим равновесие в растворе слабого электролита.
KA « K + + A -
Пусть концентрация слабого электролита в растворе С моль/л, a- степень диссоциации. Тогда концентрация недиссоциированных молекул [KA]= с(1-a), а концентрация каждого из ионов [K+]=[ A-]= сa. Выражение для константы диссоциации имеет вид:
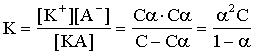
Это уравнение представляет собой закон разбавления Оствальда. Оно позволяет определять степень диссоциации при разных концентрациях электролита, если известна его константа диссоциации; а также константу диссоциации электролита, если известна его степень диссоциации при какой-либо концентрации.
Для растворов, в которых диссоциация электролита очень мала, a<<1, уравнение примет следующий вид:
Кдис @ a2·с или a= 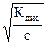 .
.
Таким образом, степень диссоциации возрастает при разбавлении раствора.
|
из
5.00
|
Обсуждение в статье: Диссоциация кислот, оснований и солей в водных растворах |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

