 |
Главная |
РАССЛАИВАНИЕ В РЕГУЛЯРНЫХ РАСТВОРАХ
|
из
5.00
|
Для того чтобы прийти к более конкретным заключениям, необходимо знать зависимость коэффициентов активности от независимых переменных Т, р и х2.
Мы рассмотрим случай, при котором коэффициенты активности γ1и γ2 определяются соотношениями
 (34)
(34)
где α — постоянная величина,
αi – активность компонента i ,
xi – мольная доля компонента,
γi – коэффициент активности, 
Как будет показано ниже, такая зависимость коэффициентов активности от состава и температуры характерна для класса растворов, называемых строго регулярными растворами и исследованных в частности Гильдебрандом и Фаулером и Гуггенгеймом.
Физический смысл (34) будет рассмотрен ниже, пока же мы можем выяснить, к каким результатам приводит применение условий устойчивости в данном частном случае. Аналогичные расчеты можно произвести, исходя из любых других уравнений для коэффициентов активности, установленных экспериментально или выведенных теоретически.
При выполнении (34) с учетом что
 ,
,
где  - стандартный химический потенциал компонента i,
- стандартный химический потенциал компонента i,
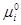 - химический потенциал компонента i в чистом состоянии.
- химический потенциал компонента i в чистом состоянии.
тогда химические потенциалы имеют форму
 (35)
(35)
 (36)
(36)
где функции  и
и  по определению равны химическим потенциалам чистых компонентов 1 и 2, находящихся в том же физическом состоянии, что и в растворе. Поэтому если система распадается на две
по определению равны химическим потенциалам чистых компонентов 1 и 2, находящихся в том же физическом состоянии, что и в растворе. Поэтому если система распадается на две
фазы, то  имеет одно и то же значение в обоих слоях, и это же справедливо по отношению
имеет одно и то же значение в обоих слоях, и это же справедливо по отношению  .
.
Дифференцируя (35), получим
 (37)
(37)
Для того чтобы система находилась в равновесном состоянии, устойчивом по отношению к разделению на две фазы, в соответствии с


необходимо и достаточно, чтобы
 (38)
(38)
Если величина  положительна и достаточно велика, то это неравенство не может выполняться при всех концентрациях. Поскольку максимальным значением х2(1- х2) является 0,25, минимальное значение
положительна и достаточно велика, то это неравенство не может выполняться при всех концентрациях. Поскольку максимальным значением х2(1- х2) является 0,25, минимальное значение  равно 4. Поэтому для всех значений
равно 4. Поэтому для всех значений  должна существовать область концентраций, в которой (38) не выполняется. В этой области система уже не находится в состоянии устойчивого равновесия и распадается на две фазы.
должна существовать область концентраций, в которой (38) не выполняется. В этой области система уже не находится в состоянии устойчивого равновесия и распадается на две фазы.
Прежде всего, используя уравнения (2), можно рассчитать положение критической точки при данном давлении р. Если Тс и ( x 2 ) c — соответственно критическая температура и критический состав, то
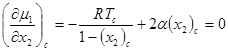 (39)
(39)
 (40)
(40)
Откуда
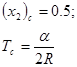 (41)
(41)
Итак, уравнения (34) для коэффициентов активности приводят к критической точке, соответствующей эквимолекулярной смеси двух компонентов. Кроме того, в этом случае мы всегда имеем дело с верхней критической температурой растворения, так как при Т > Тс неравенство (38) всегда выполняется и фаза является устойчивой, независимо от ее состава.
Найдем теперь границу, отделяющую метастабильные состояния от неустойчивых. В соответствии с (6) и (37) уравнением этой границы является
 (42)
(42)
 или, после сочетания с (41),
или, после сочетания с (41),
 (43)
(43)
Риг.11.  -Диаграмма двойной смеси вблизи критической точки.
-Диаграмма двойной смеси вблизи критической точки.

Рис.12. Расслоение фаз в регулярном растворе при постоянном р.
Наконец, нам необходимо знать кривую сосуществования двух слоев в истинном равновесии. На этой кривой должны выполняться условия
 и
и  (44)
(44)
или (см. (35) и (36))
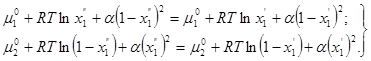 (45)
(45)
Функции  взаимно уничтожаются, и если
взаимно уничтожаются, и если  т. е. если кривая симметрична, уравнения (45) становятся тождественными. Поэтому два уравнения (45) эквивалентны одному независимому уравнению. Выбирая первое из этих уравнений и исключая
т. е. если кривая симметрична, уравнения (45) становятся тождественными. Поэтому два уравнения (45) эквивалентны одному независимому уравнению. Выбирая первое из этих уравнений и исключая  , получим
, получим
 (46)
(46)
откуда (см. (41))
 (47)
(47)
Положение критической точки и кривых (43) и (47) схематически изображено на рис.12.
|
из
5.00
|
Обсуждение в статье: РАССЛАИВАНИЕ В РЕГУЛЯРНЫХ РАСТВОРАХ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

