 |
Главная |
Лабораторная работа 15-16
|
из
5.00
|
Тема: Вычисления в весовом анализе
Цель:
Обучающая– формирование умений проведения вычислений в весовом анализе
Развивающая – глубокое изучение различных явлений и законов по данной теме ;
Воспитательная – приобщать обучающихся к активности, самостоятельности на лабораторных занятиях
Форма урока:практическая работа
Ход урока:
1. Объяснение типовой задачи - 20 минут
2.Решение задачи у доски - 25 минут
3.Самостоятельное решение - 50 минут
Расчет массы навески (mнав) анализируемого образца (пробы) проводят по схеме проведения гравиметрического анализа по методу осаждения (1.1) исходя из заданной массы весовой формы с учетом возможной массовой доли определяемого компонента в пробе w(В) и характера получаемого осадка.
В результате многочисленных исследований оптимальной массой весовой формы принято считать для аморфных осадков 0,1-0,2 г, для кристаллических – 0,1-0,5 г. Такая масса весовой формы обеспечивает относительную погрешность её взвешивания на аналитических весах менее 0,1%, что соответствует точности гравиметрического анализа.
Таким образом, в соответствии со стехиометрическими коэффициентами в (1.1):
 или:
или:
 (2.1)
(2.1)
с учетом  получим:
получим:  (2.2)
(2.2)
Формула (2.2) пригодна для расчета массы навески анализируемого образца (пробы) в методе отдельных навесок, когда вся навеска вещества целиком используется для анализа. Если масса навески очень мала и относительная погрешность её взвешивания на аналитических весах превышает 0,1%, то в этом случае следует применять метод аликвотных частей (пипетирования) и тогда расчет навески проводится по формуле (2.3):
 (2.3)
(2.3)
где: Vмк– объём мерной колбы, мл; Vп- объём пипетки (аликвоты), мл.
Следует отметить, что расчет массы навески носит ориентировочный характер и не требует высокой точности вычислений (достаточно двух значащих цифр), однако, брать для анализа нужно точную навеску, взвешивая её на аналитических весах до четвертого знака после запятой (±0,0001 г).
Растворение анализируемого образца при применении метода отдельных навесок проводят в высоком химическом стакане из термостойкого стекла, накрытого часовым стеклом для избежания разбрызгивания раствора и потери вещества, при перемешивании стеклянной палочкой. В этом же стакане проводят осаждение определяемого компонента. При применении метода пипетирования навеску пробы растворяют в мерной колбе, а затем её аликвотную часть с помощью калиброванной пипетки переносят в стакан для осаждения. Вся стеклянная посуда должна быть тщательно вымыта (см.разд. II.1).
В качестве растворителя в гравиметрии чаще всего используют воду или водные растворы кислот; возможно также применение водных растворов щелочей и комплексообразователей. Органические растворители в весовом анализе не применяют.
Пример 1.. В лекарственном препарате фуросемиде содержится по массе около 11% серы. Какую навеску препарата надо взять при его анализе, чтобы после перевода серы в сульфат-ион получить 0,50 г прокаленного осадка BaSO4? Возможно ли в этом случае применение метода отдельных навесок?
Решение: S®SO42-®ВаSO4 то есть n(S) = n(BaSO4) и b=c= 1, тогда, используя примененные при выводе формул (2.1) и (2.2) рассуждения, получим:

Относительная погрешность взвешивания на аналитических весах такой навески равна:
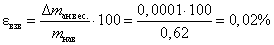
Так как 0,02% < 0,1%, то метод отдельных навесок в данном случае применить возможно.
Пример 2. Какой объем физиологического раствора, содержащего около 0,9% (по массе) хлорида натрия ( r=1 г/мл), следует взять для анализа, чтобы масса весовой формы AgCl составила 0,36 г?
Решение: NaCl ®AgCl, то есть n(NaCl) = n(AgCl) и в уравнении (2.2) (см. вывод выше) b=c= 1, тогда масса раствора хлорида натрия:

и объём раствора хлорида натрия будет равен:

Пример 3.Какую массу вещества, содержащего около 20% хлорида натрия и 30% хлорида калия, следует растворить в мерной колбе вместимостью 100 мл, чтобы из аликвоты полученного раствора объёмом 10 мл получить 0,50 г весовой формы AgCl?
Решение: NaCl®AgClи KCl®AgCl, то есть n(NaCl) + n(KCl) = n(AgCl), тогда:
 или:
или: 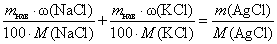 ,
,
а с учетом аликвоты:.  Следовательно:
Следовательно:

Отсюда масса навески вещества равна:
Пример 4.Сколько миллилитров 0,10 М раствора ВаС12 потребуется для осаждения серы в виде BaSO4 из навески 1,0 г продукта, содержащего 90% (по массе) лекарственного препарата дихлотиазида — M(C13H18O4N3S2Cl) = 379,5 г/моль, и индифферентные примеси, если осадитель добавляют: а) в стехиометрическом количестве; б) в полуторократном избытке?
Решение:C13H18O4N3S2Cl ®2SO42-®2BaCl2, т.е. n(BaCl2) = 2n(C13H18O4N3S2Cl) и в уравнении (3.1) а = 2, а b= 1. Тогда:
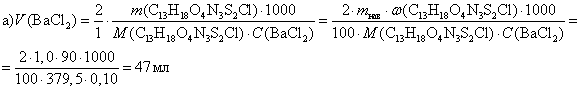
б) V’(BaCl2) = 1,5∙V(BaCl2) = 1,5∙47 = 70,5 мл
Пример 5.Навеску анализируемого образца массой 5,0 г, содержащего около 3% никеля, растворили в мерной колбе вместимостью 200,0 мл. Какой объём спиртового раствора диметилглиоксима С4H6(NOH)2 (М = 116,1 г/моль) с массовой долей 1,0% (r= 0,93г/мл) потребуется для осаждения диметилглиоксимата никеля из 20,00 мл раствора при 50% избытке осадителя?
Решение: из уравнения реакции Ni2++ 2С4H6(NOH)2 ®[Ni{С4H6NO(NOH)}2]¯n(С4H6(NOH)2) = 2n(Ni), то есть в уравнении (3.2) а = 2, а b= 1. Тогда:
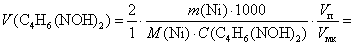
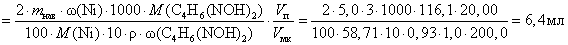
В задаче задан 50% избыток осадителя (полуторократный избыток), поэтому:
V’(С4H6(NOH)2) = 1,5∙ V(С4H6(NOH)2) =1,5∙6,4 = 9,6 мл
Пример 6.Рассчитать относительную погрешность определения, вызванную промыванием 225,3 мг осадка BaSO4 250 мл воды (при условии полного насыщения воды солью).
Решение:
BaSO4 «Ba2+ + SO42-
[Ba2+] = [SO42-] = S, тогдаKS(BaSO4) = [Ba2+]∙[SO42-] = S∙S = S2 или 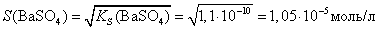
, тогдапоуравнению(4.1):
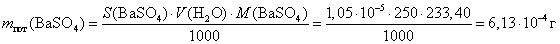
и по уравнению (4.2): 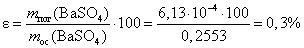
Пример 7.Какова будет потеря массы осадка PbSO4 при промывании его 200 мл 0,01 М раствора сульфата аммония?
Решение:
PbSO4 «Pb2+ + SO42-
(NH4)2SO4 ®2NH4+ + SO42-
[Pb2+] = S, a [SO42-] = S + C[(NH4)2SO4] »C[(NH4)2SO4] = 0,01 моль/л(S<<C[(NH4)2SO4]),
тогдаKS(PbSO4) = [Pb2+]∙[SO42-] = S∙C[(NH4)2SO4] = S∙0,01 или
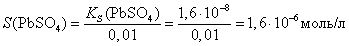 , тогда по уравнению (4.1):
, тогда по уравнению (4.1):
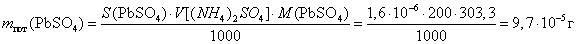
Пример 8.Вычислить концентрацию оксалата аммония, которую нужно создать в промывной жидкости, чтобы в 250 мл ее терялось не более 0,1% осадка СаС2О4, масса которого 0,10 г.
Решение: СаС2О4 «Са2+ + С2О42-
(NH4)2C2O4®2NH4++ C2O42-
[Ca2+] = S, a [C2O42-] = S + C[(NH4)2C2O4] »C[(NH4)2C2O4] (S<<C[(NH4)2C2O4]),
тогдаKS(CaC2O4) = [Ca2+]∙[C2O42- ] = S∙C[(NH4)2C2O4]
из уравнения (4.2): 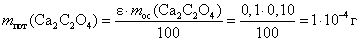 ,
,
тогда из уравнения (4.1):  и
и

Расчет результатов анализа без учета влажности анализируемого образца. Расчет массы определяемого вещества m(B) и его массовой доли в анализируемом образце w(В) проводят по схеме проведения гравиметрического анализа по методу осаждения (1.1), используя для расчета точно измеренную массу весовой формы m(C):

или:
 (6.1)
(6.1)
 (6.2)
(6.2)
где: FB/C– гравиметрический фактор пересчета;
mнав– масса навески анализируемого вещества, г/мл
При проведении анализа методом аликвотных частей в формулы (6.1) и (6.2) следует ввести множитель, учитывающий объём используемых мерной колбы (Vмк) и пипетки (Vп):
 (6.3)
(6.3)
 (6.4)
(6.4)
Пример 9.Рассчитать массовую долю железа в препарате, если из его навески массой 0,5000 г получили 0,3989 г прокаленного осадка Fe2O3.
Решение:2Fe®Fe2O3, то есть n(Fe) = 2n(Fe2O3) и в уравнении (6.1) b= 2, ac= 1,
тогда по уравнению (6.1):

а по уравнению (6.2):

Пример 10.Из 25,00 мл раствора меди сульфата получен осадок CuSCN массой 0,2144 г. Вычислить титр и молярную концентрацию анализируемого раствора.
Решение: СuSO4®CuSCN, то есть n(Cu2+) = n(CuSCN) и в уравнении (6.1) b= c= 1,
тогда:
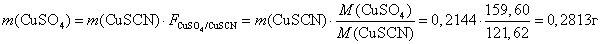 ,
,
следовательно: 

Пример 11.Навеску препарата массой 2,6340 г растворили в мерной колбе объёмом 250,0 мл. В 50,00 мл этого раствора осадили магний в виде MgNH4PO4и прокалили осадок до Mg2P2O7, масса которого оказалась равной 0,3062 г. Рассчитать массовую долю магния в анализируемом препарате.
Решение:2Mg®2 MgNH4PO4®Mg2P2O7, то есть n(Mg) = 2n(Mg2P2O7), следовательно с учетом аликвотной части по уравнению (6.3) имеем:
 и
и

Пример 12.Для анализа смеси химически чистых СаСО3 и SrCО3 была взята навеска 0,7860 г и обработана избытком серной кислоты. Масса прокаленного осадка (CaSO4 + SrSO4) составила 1,0210 г. Вычислить массовые доли карбонатов кальция и стронция в исходной смеси.
Решение: СаСО3 ®СаSO4, и SrCO3 ®SrSO4, то есть n(СаСО3) =n(CaSO4) и n(SrCO3) = n(SrSO4). Если m(CaCO3) = x,то m(SrCO3) = 0,7860 – х, следовательно:
 и
и 
Тогда:  или:
или:

Решая полученное уравнение получим: х = m(CaCO3) = 0,3716 г и 
Тогда: w(SrCO3) = 100 - w(CaCO3) = 100 – 47,28 = 52,72%
Расчет результатов анализа с учетом влажности анализируемого образца. Во влажном или воздушно-сухом состоянии в веществе присутствует внешняя (гигроскопическая) влага. Удаляя эту влагу высушиванием при 100-120°С получают сухое (абсолютно сухое) вещество. Внешняя влага обуславливает влажность образца w(Н2О) (в %), которая рассчитывается по формуле:
 (6.5)
(6.5)
где: m(Н2О) – масса внешней влаги в образце, г
mвл.нав – масса навески влажного образца,г
|
из
5.00
|
Обсуждение в статье: Лабораторная работа 15-16 |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

